Хими́ческий исто́чник то́ка
( аббр.
ХИТ
) — источник тока, в котором энергия протекающих в нём химических реакций непосредственно превращается в электрическую энергию.


То́пливный элеме́нт
, ТЭ
( англ.
) — это электрохимическое
устройство, электрохимический источник тока, непосредственно преобразующий химическую энергию топлива в электрическую энергию.
Текущая версия страницы пока не проверялась
опытными участниками и может значительно отличаться от версии
, проверенной 30 марта 2016 года; проверки требуют 18 правок
.

2:Поток электронов
3:Нагрузка 4: Кислород
5:Катод 6: Электролит
7:Анод 8:Вода 9: Гидроксид-ионы
Щелочной топливный элемент
— ( англ.
alkaline fuel cell, AFC
), наиболее изученная технология топливных элементов
.
НАСА
использует щелочные топливные элементы с середины 60-х годов, в серии аппаратов Аполлон
и Спейс Шаттл
. Щелочные топливные элементы потребляют водород и чистый кислород, и производят воду, тепло, и электричество. Они являются самыми эффективными из топливных элементов, коэффициент полезного действия
их доходит до 70 %
Химические
источники тока, устройства, вырабатывающие
электрическую энергию за счёт прямого
преобразования химической энергии
окислительно-восстановительных реакций.
Первые Х. и. т. созданы в 19 в. ( Вольтов
столб, 1800; элемент Даниела — Якоби, 1836;
Лекланше элемент, 1865, и др.). До 60-х гг. 19
в. Х. и. т. были единственными источниками
электроэнергии для питания электрических
приборов и для лабораторных исследований.
Основу Х. и. т. составляют два электрода
(один — содержащий окислитель, другой
— восстановитель), контактирующие с
электролитом. Между электродами
устанавливается разность потенциалов
— электродвижущая сила (эдс), соответствующая
свободной энергии окислительно-восстановительной
реакции. Действие Х. и. т. основано на
протекании при замкнутой внешней цепи
пространственно разделённых процессов:
на отрицательном электроде восстановитель
окисляется, образующиеся свободные
электроны переходят по внешней цепи
(создавая разрядный ток) к положительному
электроду, где участвуют в реакции
восстановления окислителя.
В
зависимости от эксплуатационных
особенностей и от электрохимической
системы (совокупности реагентов и
электролита) Х. и. т. делятся на
гальванические элементы (обычно
называются просто элементами), которые,
как правило, после израсходования
реагентов (после разрядки) становятся
неработоспособными, и аккумуляторы, в
которых реагенты регенерируются при
зарядке — пропускании тока от внешнего
источника (см. Зарядное устройство).
Такое деление условно, т.к. некоторые
элементы могут быть частично заряжены.
К важным и перспективным Х. и. т. относятся
топливные элементы (электрохимические
генераторы), способные длительно
непрерывно работать за счёт постоянного
подвода к электродам новых порций
реагентов и отвода продуктов реакции.
Конструкция резервных химических
источников тока позволяет сохранять
их в неактивном состоянии 10—15 лет (см.
также Источники тока).
27)
Кинетика электродных процессов при
электролизе. Явление поляризации,
перенапряжение. Потенциал
разложения.
Электролиз
– это
окислительно-восстановительная реакция,
протекающая на электродах под действием
электрического тока
.
Впервые
предложен механизм электродных процессов
электролиза расплава KF.
nHF,
сопровождающийся одновременным про-
теканием
на катоде нескольких реакций. Сначала
идет разряд ионов H+
,
а затем, после достижения соответ-
ствующего
напряжения, в выделении водорода
участвуют ионы K+
.
Основной результат электролиза
обеспечивается окислени-
ем
на аноде ионов (HF)nF−
до
молекулярного фтора, а на катоде −
восстановление ионного комплекса K+
молекулярного
водорода. Механизм обоснован
термодинамическим анализом возможных
суммарных электрохимических ре-
акций,
подтверждается теоретическими
представлениями об электропроводности
электролитов и объясняет аномальные
явле-
ния
электролиза расплава KF.
nHF.
Расчетные значения равновесных напряжений
наиболее вероятных суммарных электродных
реакций,
обеспечивающих основной результат
электролиза расплава KF.
nHF,
равны 3,51 В для KF.
2HF
при 363 К и 3,13 В для
HF
при 523 К
28)
Электролиз солей с растворимым и
нерастворимым анодом.
При
электролизе растворов солей , содержащих
ионы , расположенные в ряду напряжений
левее Аl3+, на катоде выделяется водород;
если ион расположен правее водорода,
то выделяется металл.
При
электролизе растворов солей, содержащих
ионы, расположенные между Аl3+ и Н+ на
катоде могут протекать конкурирующие
процессы как восстановления катионов,
так и выделения водорода. При электролизе
водного раствора соли активного металла
кислородсодержащей кислоты (например,
КNО3)
ни катионы металла, ни ионы кислотного
остатка не разряжаются. На катоде
выделяется водород, а на аноде — кислород,
и электролиз раствора нитрата калия
сводится к электролитическому разложению
воды.
Отметим,
что электролиз растворов электролитов
проводить энергетически выгоднее, чем
расплавов, так как электролиты плавятся
при очень высоких температурах.
- Типы топливных элементов
- Воздушно-алюминиевый электрохимический генератор
- Применение топливных элементов
- Техническое регулирование в области производства и использования топливных элементов
- Пример водородно-кислородного топливного элемента
- Анодные и катодные материалы и катализаторы
- Аналогии в живой природе
- Преимущества и недостатки
- Преимущества водородных топливных элементов
- Проблемы топливных элементов
- История исследований в СССР и России
- Некоторые виды химических источников тока
- Виды химических источников тока Химическими источниками тока (ХИТ) называются электрохимические устройства, в результате работы которых химическая энергия окислительно-восстановительных процессов превращается в электрическую энергию постоянного тока. К ним относятся гальванические элементы, аккумуляторы, топливные элементы. Во всех видах химических источниках тока используются электролиты – водные, неводные, твердые. К достоинствам современных ХИТ относятся относительно высокие КПД (до 0,8) и высокая удельная мощность (количество энергии, отдаваемое в единицу времени единицей массы ХИТ), что позволяет им конкурировать с другими источниками тока. Основным их недостатком является ограниченный срок службы. Среди большого разнообразия гальванических элементов можно выделить три основных типа. Первый тип . Пластины из двух различных металлов находятся в растворах солей, содержащих собственные ионы. К этому типу относится медно-цинковый гальванический элемент (элемент Даниэля – Якоби ). Второй тип. Пластины из двух различных металлов находятся в растворе одного электролита. Примером может служить элемент Вольта, состоящий из двух пластин (Zn и Cu), погруженных в раствор серной кислоты. При его работе происходят следующие процессы: (-) А: Zn Zn 2+ + 2 — окисление (анодный процесс) (+) К: 2Н + + 2 Н 2 — восстановление (катодный процесс) Выделяющийся водород насыщает поверхность катода (меди), в результате чего получается электрод другого состава (не медный, а водородный). Схема гальванического элемента Вольта: (-) Zn / Zn 2+ H 2 SO 4 2H + / H 2 (Cu) (+) В скобках справа указывается (Сu) — место выделения водорода. Третий тип . Гальванические элементы составлены из двух совершенно одинаковых по природе электродов (например, медных), погруженных в растворы одного и того же электролита, но различной концентрации. Такие элементы называются концентрационными . Схема медного концентрационного гальванического элемента: (-) Cu / CuSO 4 CuSO 4 / Cu (+) , C 1 < С 2 где C 1 и С 2 — концентрация раствора электролита, моль/л. Роль анода выполняет электрод, находящийся в более разбавленном растворе, так как его электродный потенциал имеет более низкое значение по сравнению со вторым электродом. Э ДС такого гальванического элемента зависит только от соотношения концентраций потенциалопределяющих ионов (в данном случае от концентрации CuSO 4 ). Практического значения как источники электрической энергии концентрационные гальванические элементы не имеют. Аккумуляторы – гальванические элементы, которые на основе обратимых электрохимических реакций могут многократно накапливать химическую энергию и отдавать ее для потребления в виде электрической энергии постоянного тока. Аккумуляторы — устройства многоразового действия, сочетающие в себе гальванический элемент и электролизер. Под воздействием внешнего постоянного тока в них аккумулируется (накапливается) химическая энергия, которая затем превращается в электрическую в результате окислительно-восстановительной реакции. Процесс накопления химической энергии называют зарядом аккумулятора , процесс ее превращения в электрическую — разрядом аккумулятора . В первом случае аккумулятор работает как электролизер, во втором – как гальванический элемент. Устройство и принцип действия всех аккумуляторов одинаков. Основное отличие состоит в материале электродов и типе электролита. На аноде как при разряде, так и при заряде протекает процесс окисления, на катоде – процесс восстановления. Наиболее распространенными являются кислотные и щелочные аккумуляторы. Кислотный аккумулятор ( свинцовый аккумулятор ) представляет собой пластины в виде отливок из хартблея (твердого свинца с примесью сурьмы) ячеистой структуры, собранные в батареи и помещенные в баки из эбонита или полипропилена с электролитом. В ячейки пластин предварительно запрессовывается смесь оксида свинца (PbO) с глицерином, обладающая способностью затвердевать в виде глицерата свинца. Электролитом служит раствор серной кислоты (35 — 40 % раствор H 2 SO 4 ). При взаимодействии оксида свинца с H 2 SO 4 образуется PbSO 4 . При первичной и последующих зарядах аккумулятора, когда он работает как электрохимическая ячейка, PbSO 4 на катоде превращается в свинец (Pb), а аноде — в диоксид свинца (PbO 2 ), которые и являются электродами: (-) К : PbSO 4(тв) + 2 Pb ( тв) + SO (р-р) (+) А : PbSO 4(тв) +2 Н 2 О PbО 2(тв) + 2 + 4 Н + + SO (р-р) 2PbSO 4(тв) + 2H 2 O Pb (тв) + PbO 2(тв) + 2 H 2 SO 4(р-р) ЭДС заряженного аккумулятора приблизительно равна 2 В (если 6 таких аккумуляторов последовательно соединить, получается обычный автомобильный аккумулятор с ЭДС = 12В). При работе аккумулятора – его разрядке, когда он работает как химический источник тока, на электродах протекают электродные процессы в обратном направлении. По мере его разрядки расходуются материалы катода (PbО 2 ) , анода (Pb) и электролит — серная кислота. Напряжение на зажимах аккумулятора падает и его необходимо заряжать. Для зарядки аккумулятор подключают к внешнему источнику тока, направление тока противоположно разрядному. Токообразующие и электродные реакции в свинцовом аккумуляторе можно представить в виде: Pb ( тв ) + SO (р-р) PbSO 4(тв) + 2
- 4(тв) + 2
- │H
AFC
являются самыми дешевыми из топливных элементов в производстве. Катализаторы, необходимые для электродов, изготавливаются из химических веществ, которые недороги по сравнению с тем, которые требуются для других типов топливных элементов.
Коммерческие перспективы лежат в основном AFC
с недавно разработанной версии этой технологии с биполярной пластиной, значительно превосходящей по производительности более ранние версии моно-плит.
Первый в мире корабль на топливных элементах HYDRA
использует систему AFC
с 5 кВт выходом электроэнергии.
Другим недавним событием является появление твердотельного щелочного топливным элементом, с использованием анионообменных щелочных мембран вместо жидкости. Это решает проблему отравления и позволяет развивать щелочные топливные элементы, способные работать на более безопасных богатых водородом носителях, таких как жидкие растворы мочевины или металло-аминовые комплексы.
- Квасников Л. А., Тазетдинов Р. Г.
Регенеративные топливные элементы. — Тираж 1600 экз. — М., Атомиздат
, 1978 г. — 168 с. - Анисимов В. М.
Топливные элементы и перспективы применения их на железнодорожном транспорте. — Москва, Транспорт
, 1971 г. — 72 с. - Топливные элементы. — Перевод с английского. — М., Иностранная литература
, 1963 г. — 216 стр. - Топливные элементы. Некоторые вопросы теории. — Наука
, 140 страниц; 1964 г.
Из-за этого эффекта отравления, используют два основных варианта AFC
: со статическим и проточным электролитом. Статические или иммобилизованные ячейки, электролитного типа, устанавливаемые в космическом корабле Apollo и Space Shuttle, обычно используют асбестовый сепаратор, насыщенный в гидроксиде калия. Производство воды контролируется путём испарения с анода, как показано на рисунке выше, который производит чистую воду, которая может быть освобождена для других целей. Эти топливные элементы используют платиновые катализаторы для достижения максимальных показателей объемной и массовой эффективности.
Проточные конструкции ячеек используют более открытую матрицу, которая позволяет электролиту течь либо между электродами (параллельно) или через электроды в поперечном направлении (типа ASK
или EloFlux
топливного элемента). В параллельно-проточных конструкциях смены электролита, полученная вода удерживается в электролите, и старый электролит может быть заменен на свежий, по методике, похожей на замену масла в автомобиле. Между электродами требуется дополнительное место для прохождения потока, это приводит к увеличению внутреннего сопротивления ячеек, уменьшению выходной мощности по сравнению с иммобилизованными конструкциями. Еще одна технологическая проблема заключается в постоянном блокировании катода с помощью K 2
CO 3
; некоторые опубликованные отчёты показали тысячи часов работы в воздухе(?). В этих конструкциях использовали как платину, так и металлические катализаторы из неблагородных металлов, что приводит к повышению эффективности и увеличению стоимости.
Конструкция EloFlux
, с поперечным потоком электролита, имеет преимущество с низким уровнем затрат на сменный электролит, но до сих пор только была продемонстрирована с использованием кислорода.
Электроды состоят из структуры двойного слоя: активный электрокатализаторной слой и гидрофобный слой. Активный слой состоит из органической смеси, которая является основанием, а затем прокатывают при комнатной температуре с образованием сшитого самонесущего листа. Гидрофобная структура предотвращает утечки электролита в реагентные каналы газовых потоков и обеспечивает диффузию газов к месту реакции. Эти два слоя затем прижимают проводящую металлическую сетку, и спекание завершает процесс.
Дальнейшие вариации щелочного топливного элемента включают металл-гидридный топливный элемент и прямой бор-гидридный топливный элемент
Типы топливных элементов
Воздушно-алюминиевый электрохимический генератор
Воздушно-алюминиевый электрохимический генератор
использует для производства электроэнергии окисление
алюминия
кислородом
воздуха
. Токогенерирующую реакцию в нём можно представить в виде
- 4 Al(OH)3,}}}»>
а реакцию коррозии — как
- 2 Al(OH)3 + 3 H2}}}»>
.
Эти два электрода разделены пористой матрицей, насыщенной водным раствором щелочи, обычно гидроксидом калия (KOH). Водные щелочные растворы поглощают углекислый газ (CO 2
), таким образом, топливный элемент может стать «отравленным» путём преобразования KOH в карбонат калия (K 2
CO 3
). Из-за этого щелочные топливные элементы, как правило, работают на чистом кислороде, или, по крайней мере, на очищенном от двуокиси углерода воздухе, и должны включать в конструкцию «скруббер» для удаления максимально возможного количества двуокиси углерода. Так как требования к производству и хранения кислорода делают чистый кислород дорогим, есть несколько компаний, занимающихся активным продвижением технологии. Существует, однако, некоторые дебаты в научном сообществе по поводу того, является ли отравление постоянным или обратимым. Основные механизмы отравления блокируют поры в катоде с K 2
CO 3
, которая не является обратимым, и уменьшение ионной проводимости электролита, который может быть обратимым, возвращая KOH к своей первоначальной концентрации. Альтернативный способ включает в себя простую замену KOH, который возвращает топливную ячейку в исходное состояние.
Когда углекислый газ реагирует с электролитом, образуются карбонаты. Карбонаты могут осаждаются на порах электродов, которые в конечном итоге блокируют их. Было обнаружено, что работа AFC при более высокой температуре не показывает снижение производительности, в то время как на уровне около комнатной температуры, было замечено значительное падение производительности. Карбонатное отравление при температуре окружающей среды, как полагают, является результатом низкой растворимости K 2
CO 3
при комнатной температуре, что приводит к осаждению K 2
CO 3
, который блокирует поры электрода. Кроме того, эти осадители постепенно уменьшают гидрофобность электрода опорного защитного слоя, ведущий к структурной деградации и забиванию электрода.
С другой стороны, несущие заряд ионы гидроксила в электролите могут вступать в реакцию с диоксидом углерода из продуктов окисления органического топлива (т.е. метанола, муравьиной кислоты) или воздуха с образованием карбонатных соединений.
Образование карбонатов истощает гидроксильные ионы из электролита, уменьшает проводимость электролита и, следовательно, производительность топливных ячеек. Также может уменьшать производительность изменение объёма электролита, давление водяного пара в ячейке, и другие факторы.
Применение топливных элементов
Топливные элементы первоначально применялись только в космической отрасли
, однако в настоящее время сфера их применения непрерывно расширяется. Их применяют в стационарных электростанциях
, в качестве автономных источников тепло- и электроснабжения зданий, в двигателях транспортных средств, в качестве источников питания ноутбуков
и мобильных телефонов
. Часть этих устройств пока не покинула стен лабораторий, другие уже коммерчески доступны и давно применяются.
Широко используются высокомощные энергетические установки на базе топливных элементов. В основном такие установки работают на основе элементов на базе расплавленных карбонатов, фосфорной кислоты и твёрдых оксидов. Как правило, такие установки используют не только для выработки электроэнергии, но и для получения тепла.
Большие усилия прилагаются для разработки гибридных установок, в которых высокотемпературные топливные элементы комбинируются с газовыми турбинами
. К ПД таких установок может достигать при усовершенствовании газовых турбин.
Активно выпускаются и маломощные установки на базе топливных элементов.
Техническое регулирование в области производства и использования топливных элементов
В 19 августа 2004 года Международной электротехнической комиссией
(МЭК, IEC) был выпущен первый международный стандарт IEC 62282-2 «Технологии топливных элементов. Часть 2, Модули топливных элементов». Это был первый стандарт серии IEC 62282, разработка которой осуществляется Техническим комитетом «Технологии топливных элементов» (TC/IEC 105); в состав Технического комитета ТС/IEC 105 входят постоянные представители из 17 стран и наблюдатели из 15 стран мира.
TC/IEC 105 разработал и издал 14 международных стандартов серии IEC 62282, охватывающих широкий спектр тематики, связанной со стандартизацией энергоустановок на основе топливных элементов. Федеральное агентство по техническому регулированию и метрологии Российской Федерации (РОССТАНДАРТ) является коллективным членом Технического комитета ТС/IEC 105 на правах наблюдателя. Координационную деятельность с МЭК со стороны Российской Федерации осуществляет секретариат РосМЭК ( Росстандарт
), а работы по имплементации стандартов МЭК производятся национальным Техническим комитетом по стандартизации ТК 029 «Водородные технологии», Национальной ассоциацией водородной энергетики (НАВЭ) и ООО «КВТ».
В настоящее время Росстандарт принял следующие национальные и межгосударственные стандарты, идентичные международным стандартам IEC:
- ГОСТ Р 56188.1-2014/IEC/TS 62282-1:2010 «Технологии топливных элементов. Часть 1. Терминология»;
- ГОСТ Р МЭК 62282-2-2014 «Технологии топливных элементов. Часть 2. Модули топливных элементов»;
- ГОСТ Р МЭК 62282-3-100-2014 «Технологии топливных элементов. Часть 3-100. Стационарные энергоустановки на топливных элементах. Безопасность»;
- ГОСТ Р МЭК 62282-3-200-2014 «Технологии топливных элементов. Часть 3-200. Стационарные энергоустановки на топливных элементах. Методы испытаний для определения рабочих характеристик»;
- ГОСТ IEC 62282-3-201-2016 «Технологии топливных элементов. Часть 3-201. Стационарные энергоустановки на топливных элементах. Методы испытаний для определения рабочих характеристик систем малой мощности»;
- ГОСТ IEC 62282-3-300-2016 «Технологии топливных элементов. Часть 3-300. Стационарные энергоустановки на топливных элементах. Монтаж»;
- ГОСТ IEC 62282-5-1-2016 «Технологии топливных элементов. Часть 5-1 Портативные энергоустановки на топливных элементах. Безопасность»
- ГОСТ IEC 62282-7-1-2016 «Технологии топливных элементов. Часть 7-1: Методы испытаний единичных элементов для топливных элементов с полимерным электролитом».
По возможности или невозможности повторного использования химические источники тока делятся на:
- гальванические элементы
(первичные ХИТ), которые из-за необратимости протекающих в них реакций невозможно перезарядить; - электрические аккумуляторы
(вторичные ХИТ) — перезаряжаемые гальванические элементы, которые с помощью внешнего источника тока ( зарядного устройства
) можно перезарядить; - топливные элементы
(электрохимические генераторы) — устройства, подобные гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне, а продукты реакций удаляются из него, что позволяет ему функционировать непрерывно, пока обеспечивается подача реагентов.
Следует заметить, что деление элементов на гальванические и аккумуляторы до некоторой степени условное, так как некоторые гальванические элементы, например щелочные батарейки, поддаются подзарядке, но эффективность этого процесса крайне низка.
По типу используемого электролита химические источники тока делятся на кислотные
(например свинцово-кислотный аккумулятор
, свинцово-плавиковый элемент
), щелочные
(например ртутно-цинковый элемент
, ртутно-кадмиевый элемент
, никель-цинковый аккумулятор
, никель-кадмиевый аккумулятор
) и солевые
(например, марганцево-магниевый элемент
, цинк-хлорный аккумулятор
).
Топливные элементы — это электрохимические устройства, которые теоретически могут иметь высокий коэффициент преобразования химической энергии
в электрическую
.
Обычно в низкотемпературных топливных элементах используются:
водород
подаваемый со стороны анода
и кислород
или воздух подаваемый на катод
(водородный элемент) или метанол
и кислород
воздуха.
- Принцип разделения потоков горючего и окислителя
В топливном элементе реагенты втекают, продукты реакции вытекают, и реакция может протекать так долго, как поступают в неё реагенты и сохраняется реакционная способность компонентов самого топливного элемента, чаще всего определяемая «отравлением» их катализатора побочными продуктами недостаточно чистых исходных веществ.
Одноразовые же гальванические элементы
и аккумуляторы
, в отличие от топливных элементов, содержат расходуемые твёрдые или жидкие реагенты содержание которых ограничена объёмом гальванического элемента, и, после исчерпания реагентов электрохимическая реакция прекращается, они должны быть заменены на новые либо электрически перезаряжены, чтобы произвести обратную электрохимическую реакцию, или, по крайней мере, в них нужно поменять израсходованные электроды и отработанный электролит.
Топливные элементы не предназначены для хранения электрической энергии, как гальванические элементы или электрохимические аккумуляторы, но для некоторых применений, таких как работающие изолированно от электрической системы электростанции
, использующие непостоянные источники энергии
(солнце, ветер), они совместно с электролизёрами
, компрессорами и ёмкостями для хранения топлива (например, баллоны для водорода) образуют устройство для хранения энергии.
Пример водородно-кислородного топливного элемента
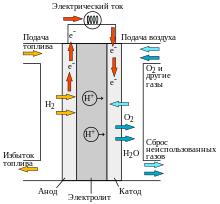
Водородно-кислородный топливный элемент с протонообменным электролитом
» (например, «с полимерной мембраной) содержит протонопроводящую полимерную мембрану, которая разделяет два электрода — анод
и катод
; каждый электрод
обычно представляет собой угольную пластину (матрицу) с нанесённым катализатором
— платиной
или сплавом платиноидов
и другие композиции.
На катализаторе анода молекулярный водород
диссоциируется
и теряет электроны
превращаясь в протоны
. Катионы водорода (протоны) проникают через мембрану к катоду, но электроны отдаются во внешнюю цепь, так как мембрана непроницаема для электронов, то есть не имеет электронной проводимости.
На катализаторе катода атомы кислорода соединюется с электронами (который подводятся по проводу внешней электрической цепи) и проникшими через электролит протонами и образует воду, являющуюся единственным продуктом реакции, вода отводится от катода в виде пара
и/или жидкости
.
Анодные и катодные материалы и катализаторы
Анод и катод, как правило, — это просто проводящий катализатор — платина
, нанесённая на высокоразвитую углеродную поверхность.
Аналогии в живой природе
Природным топливным элементом является митохондрия
живой клетки. Митохондрии перерабатывают органическое «горючее» — пируваты
и жирные кислоты
и синтезируют АТФ
— универсальный источник энергии для всех биохимических процессов в живых организмах, при этом возникает разность электрических потенциалов на своей внутренней мембране. Однако реализация этого процесса для получения электроэнергии в промышленных масштабах затруднительно, так как протонные помпы
митохондрий имеют белковую природу.
Основу химических источников тока составляют два электрода
(положительно заряженный катод
, содержащий окислитель
, и отрицательно заряженный анод
, содержащий восстановитель
) контактирующие с электролитом
. Между электродами устанавливается разность потенциалов — электродвижущая сила
, соответствующая свободной энергии окислительно-восстановительной реакции
. Действие химических источников тока основано на протекании при замкнутой внешней цепи пространственно-разделённых процессов: на отрицательном аноде восстановитель окисляется, образующиеся свободные электроны переходят по внешней цепи к положительному катоду, создавая разрядный ток, где они участвуют в реакции восстановления окислителя. Таким образом, поток отрицательно заряженных электронов по внешней цепи идет от анода к катоду, то есть от отрицательного электрода (отрицательного полюса химического источника тока) к положительному. Это соответствует протеканию электрического тока в направлении от положительного полюса к отрицательному, так как направление тока совпадает с направлением движения положительных зарядов в проводнике.
В современных химических источниках тока используются:
- в качестве восстановителя (материал анода) — свинец
Pb, кадмий
Cd, цинк
Zn и другие металлы; - в качестве окислителя (материал катода) — оксид свинца(IV)
PbO 2
, гидроксооксид никеля
NiOOH, оксид марганца(IV)
MnO 2
и другие; - в качестве электролита — растворы щелочей
, кислот
или солей
[2]
.
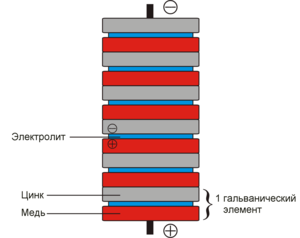
Первый химический источник тока был изобретён итальянским учёным Алессандро Вольта
в 1800 году. Это был «элемент Вольта» — сосуд с серной кислотой с опущенными в него цинковой
и медной
пластинками, с проволочными токовыводами. Затем учёный собрал батарею
из этих элементов, которая впоследствии была названа «вольтовым столбом»
. Это изобретение впоследствии использовали другие учёные в своих исследованиях. Так, например, в 1802 году русский академик В. В. Петров
сконструировал вольтов столб из 2100 элементов для получения электрической дуги
. В 1836 году английский химик Джон Даниель
усовершенствовал элемент Вольта, поместив цинковый и медный электроды в раствор серной кислоты
. Эта конструкция стала называться «элементом Даниеля»
.
В 1859 году французский физик Гастон Плантэ
изобрёл свинцово-кислотный аккумулятор
, поместив скрученную в рулон тонкую свинцовую пластину в серную кислоту. Этот тип элемента и по сей день используется в автомобильных аккумуляторах
.
В 1865 году французский химик Ж. Лекланше
предложил свой гальванический элемент ( элемент Лекланше
), состоявший из цинкового стаканчика, заполненного водным раствором хлористого аммония
или другой хлористой соли, в который был помещён агломерат
из оксида марганца(IV)
MnO 2
в качестве деполяризатора с угольным токоотводом. Модификация этой конструкции используется до сих пор в солевых батарейках для различных бытовых устройств.
В 1890 году в Нью-Йорке
Конрад Хьюберт
, иммигрант из России, создаёт первый карманный электрический фонарик
. А уже в 1896 году компания National Carbon
приступает к массовому производству первых в мире сухих элементов Лекланше «Columbia».
Преимущества и недостатки
Преимущества водородных топливных элементов
Водородные топливные элементы обладают рядом ценных качеств, среди которых:
- Высокий КПД
- У топливных элементов нет принципиального теоретического ограничения на КПД, как у тепловых машин (КПД цикла Карно
является максимально возможным КПД среди всех тепловых машин с такими же минимальной и максимальной температурами). - Высокий КПД достигается благодаря прямому превращению энергии топлива в электроэнергию. В обычных генераторных установках топливо сначала сжигается, нагретый водяной пар или газ вращает турбину или вал двигателя внутреннего сгорания, которые, в свою очередь, вращают электрический генератор. Результативный максимум КПД составляет чаще же он находится на уровне порядка Более того, из-за множества звеньев, а также из-за термодинамических ограничений по максимальному КПД тепловых машин, существующий КПД вряд ли удастся поднять выше. У существующих топливных элементов КПД составляет [17]
. - КПД почти не зависит от коэффициента загрузки.
- Экологичность
- Компактные размеры
Топливные элементы легче и имеют меньшие размеры, чем традиционные источники питания. Топливные элементы производят меньше шума, меньше нагреваются, более эффективны с точки зрения потребления топлива. Это становится особенно актуальным в военных приложениях. Применение топливных элементов позволит сократить затраты на логистику, снизить вес, продлить время действия приборов и оборудования.
Совокупная стоимость
владения водородно-воздушных систем значительно ниже обычных электрохимических батарей. Кроме того, они обладают высочайшей отказоустойчивостью
за счет отсутствия движущихся частей механизмов, не нуждаются в техническом обслуживании, а срок их эксплуатации достигает 15 лет, превосходя классические электрохимические батареи вплоть до пяти раз.
Проблемы топливных элементов
Внедрению топливных элементов на транспорте мешает отсутствие водородной инфраструктуры
. Возникает проблема «курицы и яйца» — зачем производить водородные автомобили, если нет инфраструктуры? Зачем строить водородную инфраструктуру, если нет водородного транспорта?
Большинство элементов при работе выделяют то или иное количество тепла. Это требует создания сложных технических устройств для утилизации тепла (паровые турбины и пр.), а также организации потоков топлива и окислителя, систем управления отбираемой мощностью
, долговечности мембран, отравления катализаторов
некоторыми побочными продуктами окисления топлива и других задач. Но при этом же высокая температура процесса позволяет производить тепловую энергию, что существенно увеличивает КПД энергетической установки.
Топливные элементы, в силу низкой скорости химических реакций, обладают инертностью и для работы в условиях пиковых или импульсных нагрузок требуют определённого запаса мощности или применения других технических решений ( суперконденсаторы
, аккумуляторные батареи).
Также существует проблема получения и хранения водорода
. Во-первых, он должен быть достаточно чистый, чтобы не произошло быстрого отравления катализатора
, во-вторых, достаточно дешёвый, чтобы его стоимость была рентабельна для конечного потребителя.
Из простых химических элементов водород и углерод
являются крайностями. У водорода самая большая удельная теплота сгорания среди всех химических элементов и высокая химическая активность, но очень низкая плотность. У углерода самая высокая удельная теплота сгорания среди твёрдых элементов, достаточно высокая плотность, но низкая химическая активность из-за энергии активации. Золотая середина — углевод (сахар) или его производные (этанол) или углеводороды (жидкие, твёрдые и газообразные). Выделяемый углекислый газ
должен участвовать в общем цикле дыхания планеты, не превышая предельно допустимых концентраций.
К сожалению, в водороде, произведённом из природного газа, будет присутствовать угарный газ (СО)
и сероводород
, отравляющие катализатор. Поэтому для уменьшения отравления катализатора необходимо повысить температуру топливного элемента. Уже при температуре в топливе может присутствовать СО.
Кроме того, водород ещё и крайне пожароопасен и взрывоопасен. Даже при сильных морозах он может самопроизвольно вспыхнуть при смешивании с воздухом.
История исследований в СССР и России
Русский электротехник П. Н. Яблочков получил патент (N. 187139) на электрический элемент с механической поляризацией (топливный элемент) в 1887 году, проживая в то время во Франции.
Первые систематические исследования в СССР начались в 60-х
годах. РКК «Энергия»
(с 1966 года) разрабатывала фосфорнокислотные (PAFC) топливные элементы для советской лунной программы
. С 1987 по 2005 годы «Энергия» произвела около 100 топливных элементов, которые наработали суммарно около
Во время работ над программой « Буран
» (1980-е годы), разрабатывались щелочные (AFC) элементы, отвечающие условиям и требованиям полёта. На «Буране» были установлены 10-киловаттные топливные элементы.
В 70-е — 80-е годы НПО «Квант»
совместно с Рижским автобусным заводом « РАФ
» разрабатывали щелочные ТЭ для автобусов. Прототип такого автобуса на топливных элементах ( Квант-РАФ
) был изготовлен в 1982 году
.
В 1999 году АвтоВАЗ
начал работы с топливными элементами. К 2003 году на базе автомобиля ВАЗ-2131
было создано несколько опытных экземпляров. В моторном отсеке автомобиля располагались батареи топливных элементов, а баки со сжатым водородом располагались в багажном отделении, то есть была применена классическая схема расположения силового агрегата и топливных баков-баллонов. Разработками водородного автомобиля руководил кандидат технических наук Г. К. Мирзоев.
В 2008 году была основана компания « ИнЭнерджи
», которая занимается научно-исследовательскими и опытно-конструкторскими работами в области электрохимических технологий и систем электропитания. По результатам проведённых исследований, при кооперации с ведущими институтами РАН (ИПХФ, ИФТТ и ИХТТМ), был реализован ряд пилотных проектов, показавших высокую эффективность. Для компании « МТС
» была создана и введена в эксплуатацию модульная система резервного питания
на базе водородно-воздушных топливных элементов, состоящая из ТЭ, системы управления, накопителя электроэнергии и преобразователя; с мощностью системы до
- fuelcells.org
- fuelcelltoday.com
- Раменский А. Ю., Григорьев С. А.
Технологии топливных элементов: вопросы технического регулирования, ISJAEE № 19-20 (207—208), 2016 год - hydrogenandfuelcells
// Департамент энергетики США - — сравнение ЭХГ с двигателями Стирлинга
- [1]
Как работает топливный элемент, на русском языке
Некоторые виды химических источников тока
Гальванический элемент — химический источник электрического тока, названный в честь Луиджи Гальвани
. Принцип действия гальванического элемента основан на взаимодействии двух металлов через электролит, приводящем к возникновению в замкнутой цепи электрического тока.
- См. также Категория: Гальванические элементы
.
Электрический аккумулятор — химический источник тока многоразового действия (то есть в отличие от гальванического элемента химические реакции, непосредственно превращаемые в электрическую энергию, многократно обратимы). Электрические аккумуляторы используются для накопления энергии и автономного питания различных устройств.
- См. также Категория: Аккумуляторы
.
Топливный элемент — электрохимическое устройство, подобное гальваническому элементу, но отличающееся от него тем, что вещества для электрохимической реакции подаются в него извне — в отличие от ограниченного количества энергии, запасенного в гальваническом элементе или аккумуляторе.
- См. также Категория: Топливные элементы
.Топливный элемент вырабатывает энергию посредством окислительно-восстановительной реакции между водородом и кислородом. На аноде водород окисляется в соответствии с реакцией:
с образованием воды и высвобождения электронов. При этом электроны текут через внешнюю цепь и возвращаются к катоду. Кислород расходуется в реакции:
и производит гидроксид ионы. Полный цикл реакции потребляет одну молекулу кислорода и две молекулы водорода, производя две молекулы воды. Тепловая энергия образуется как побочный продукт этой реакции.
Exhibit 1 — The Clarendon Dry Pile». Oxford Physics Teaching, History Archive. Retrieved 18 January 2008
В демонстрационных экспериментах зачастую используют мякоть плодов апельсина, яблоки и пр.
Элементарный учебник физики / Под ред. Г. С. Ландсберга
. — 13-е изд. — М.
: ФИЗМАТЛИТ
, 2003. — Т. 2. Электричество и магнетизм. — С. 151,152,465.Лекция по теме «Химические источники тока»
Виды
химических источников токаВиды
химических источников тока- Роль
анода выполняет электрод, находящийся
в более разбавленном растворе, так как
его электродный потенциал имеет более
низкое значение по сравнению со вторым
электродом. Э ДС такого гальванического
элемента зависит только от соотношения
концентраций потенциалопределяющих
ионов (в данном случае от концентрации
CuSO 4
).Практического
значения как источники электрической
энергии концентрационные гальванические
элементы не имеют.Аккумуляторы
–
гальванические элементы,
которые на основе обратимых электрохимических
реакций могут многократно накапливать
химическую энергию и отдавать ее для
потребления в виде электрической энергии
постоянного тока.
Аккумуляторы
— устройства многоразового действия,
сочетающие в себе гальванический элемент
и электролизер. Под воздействием
внешнего постоянного тока в них
аккумулируется (накапливается) химическая
энергия, которая затем превращается в
электрическую в результате
окислительно-восстановительной реакции.
Процесс накопления химической энергии
называют зарядом
аккумулятора
,
процесс ее превращения в электрическую
— разрядом
аккумулятора
.
В первом случае аккумулятор работает
как электролизер, во втором – как
гальванический элемент.Устройство
и принцип действия всех аккумуляторов
одинаков. Основное отличие состоит в
материале электродов и типе электролита.
На аноде как при разряде, так и при заряде
протекает процесс окисления, на катоде
– процесс восстановления.Наиболее
распространенными являются кислотные
и щелочные аккумуляторы.Кислотный
аккумулятор
( свинцовый
аккумулятор
)
представляет собой пластины в виде
отливок из хартблея (твердого свинца с
примесью сурьмы) ячеистой структуры,
собранные в батареи и помещенные в баки
из эбонита или полипропилена с
электролитом. В ячейки пластин
предварительно запрессовывается смесь
оксида свинца (PbO)
с глицерином, обладающая способностью
затвердевать в виде глицерата свинца.
Электролитом служит раствор серной
кислоты (35 — 40 % раствор H 2
SO 4
).
При взаимодействии оксида свинца с
H 2
SO 4
образуется
PbSO 4
.При
первичной и последующих зарядах
аккумулятора, когда он работает как
электрохимическая ячейка, PbSO 4на катоде превращается в свинец (Pb),
а аноде — в диоксид свинца (PbO 2
),
которые и являются электродами:(-) К : PbSO 4(тв)
+ 2


Pb
(
тв)+ SO

(р-р)(+) А : PbSO 4(тв)
+2 Н 2
О

PbО
2(тв)+ 2

+ 4 Н ++ SO

(р-р)
2PbSO 4(тв)
+ 2H 2
O
Pb (тв)+ PbO 2(тв)
+ 2 H 2
SO 4(р-р)ЭДС
заряженного аккумулятора приблизительно
равна 2 В (если 6 таких аккумуляторов
последовательно соединить, получается
обычный автомобильный аккумулятор с
ЭДС = 12В).При
работе аккумулятора – его разрядке,
когда он работает как химический источник
тока, на электродах протекают электродные
процессы в обратном направлении.По
мере его разрядки расходуются материалы
катода (PbО 2
)
, анода (Pb) и электролит — серная кислота.
Напряжение на зажимах аккумулятора
падает и его необходимо заряжать. Для
зарядки аккумулятор подключают к
внешнему источнику тока, направление
тока противоположно разрядному.Токообразующие
и электродные реакции в свинцовом
аккумуляторе можно представить в виде:Pb (
тв
)+ SO

(р-р)
PbSO4(тв)
+ 2
Химическими источниками тока
(ХИТ) называются электрохимические
устройства, в результате работы которых
химическая энергия окислительно-восстановительных
процессов превращается в электрическую
энергию постоянного тока. К ним относятся
гальванические элементы, аккумуляторы,
топливные элементы. Во всех видах
химических источниках тока используются
электролиты – водные, неводные, твердые.
К достоинствам современных ХИТ относятся
относительно высокие КПД (до 0,8) и высокая
удельная мощность (количество энергии,
отдаваемое в единицу времени единицей
массы ХИТ), что позволяет им конкурировать
с другими источниками тока. Основным
их недостатком является ограниченный
срок службы.
Среди
большого разнообразия гальванических
элементов можно выделить три основных
типа.Первый
тип.
Пластины из двух различных металлов
находятся в растворах солей, содержащих
собственные ионы. К этому типу относится
медно-цинковый гальванический элемент
(элемент Даниэля – Якоби ).Второй
тип.Пластины из двух различных металлов
находятся в растворе одного электролита.
Примером может служить элемент Вольта,
состоящий из двух пластин (Zn и Cu),
погруженных в раствор серной кислоты.
При его работе происходят следующие
процессы:(-)
А: Zn
Zn 2++ 2

— окисление (анодный процесс)(+)
К: 2Н ++ 2

Н 2

—
восстановление (катодный процесс)Выделяющийся
водород насыщает поверхность катода
(меди), в результате чего получается
электрод другого состава (не медный, а
водородный).Схема
гальванического элемента Вольта:
(-)
Zn /
Zn 2+
H 2
SO 4
2H +
/
H 2
(Cu)
(+)В
скобках справа указывается (Сu) — место
выделения водорода.Третий
тип
.
Гальванические элементы составлены из
двух совершенно одинаковых по природе
электродов (например, медных), погруженных
в растворы одного и того же электролита,
но различной концентрации. Такие элементы
называются концентрационными
.Схема
медного концентрационного гальванического
элемента:
(-)
Cu /
CuSO 4
CuSO 4
/
Cu
(+) ,C 1
< С 2
где
C 1и С
- 2
— концентрация раствора электролита,
моль/л.
PbО 2(тв)+ 2
+
4 Н+
(р-р)
+
SO(р-р)
PbSO4(тв)
+ 2 Н 2
- О
Pb (тв)+ PbO 2(тв)
+ 2 H 2
SO 4
(р-р)
2 PbSO4(тв)
+ 2H
2
- O
(
— ) Pb
/ Pb2+
│H
2
SO4
│Pb
2+
/ PbO 2
( + )
Стандартные
величины потенциалов для электродов
свинцового аккумулятора имеют следующие
значения:,
.
ЭДС
аккумулятора, как химического источника
тока, рассчитывается по уравнению:Из
данного уравнения видно, что ЭДС
аккумулятора зависит от концентрации
(активности) серной кислоты, которая
возрастает при заряде аккумулятора и
уменьшается при его разояде. О степени
разряда аккумулятора судят по концентрации
электролита, т.е. концентрации H 2
SO 4
.
Используя концентрированные растворы
H 2
SO 4
,
можно было бы увеличить ЭДС аккумулятора,
однако при концентрации H 2
SO 4больше 39% резко уменьшается электропроводность
растворов и увеличивается растворимость
свинца, поэтому оптимальными являются
32 — 39 % — ные растворы H 2
SO 4
.Во
время заряда аккумулятора растет
напряжение на его полюсах. В конце оно
достигает такого значения, что начинается
электролиз воды, сопровождающийся
выделением водорода на катоде и кислорода
– на аноде:(
-)
К : 2 Н 2
О
+ 2

Н 2

+2
ОН —(+)
А : 4 ОН —
О 2

+ 2 Н 2
О
+ 4


2
Н 2
О
2 Н 2

+
О 2

Так
называемое «кипение» электролита
является признаком окончания заряда
свинцового аккумулятора. Заряженный
аккумулятор может быть сразу использован
по назначению. При хранении же из него
выливают электролит и промывают водой.
В таком виде он может находиться до 2
лет и для его использования достаточно
лишь залить электролит. При хранении
незаряженного аккумулятора с раствором
серной кислоты происходит его
«сульфатирование» – образование на
пластинках большого количества PSO 4
.
Когда кислотный аккумулятор работает,
давая ток, PSO 4осаждается в очень мелкозернистой форме
на поверхности электродов. Когда же
аккумулятор выключен, мелкозернистый
слой рекристаллизуется и образуются
более крупные кристаллы, которые могут
закупорить поры электрода, уменьшая
его поверхность или отрываться от
электрода и оседать на дно аккумулятора.
Процесс сульфатации является основной
причиной выхода аккумулятора из строя,
поэтому нужно следить, чтобы аккумулятор
не простаивал частично в разряженном
состоянии.Преимущества
свинцового аккумулятора – высокий КПД
(около 80 %), высокая ЭДС и относительно
малое ее изменение при разряде, большая
электрическая емкость, устойчивость в
работе. Недостатки – большая масса и,
следовательно, малая удельная емкость,
саморазряд аккумулятора при хранении,
малый срок службы (2 – 5 лет), а также
токсичность свинца и сильные окислительные
свойства H 2
SO 4
.Щелочные
аккумуляторы
различаются
по материалу пластин отрицательно
заряженного электрода. Наиболее
распространенные из них кадмий —
никелевые (Cd
— Ni)
и железо — никелевые ( Fe
– Ni
) аккумуляторы. Активная масса положительных
пластин состоит, в основном, из
гидратированного оксида никеля (III),
кроме того в ней содержится графит,
добавляемый для увеличения
электропроводности. Электролитом служит
раствор КОН (20 %), содержащий небольшое
количество LiOH.
ЭДС заряженного аккумулятора (Cd
— Ni)
приблизительно равна 1,3
В.- Дасоян М. А.
Химические источники тока. — 2-е изд. — Л.
, 1969. - Романов В. В., Хашев Ю. М.
Химические источники тока. — М.
, 1968. - Орлов В. А.
Малогабаритные источники тока. — 2-е изд. — М.
, 1970. - Вайнел Д. В.
Аккумуляторные батареи. — пер. с англ., 4-е изд. — М. — Л., 1960. - The Primary Battery / ed. G. W. Heise, N. C. Cahoon. — N. Y. — L., 1971. — Т. v. 1.
- Химические источники тока
— статья из Большой советской энциклопедии
. - О химических источниках тока
- Аккумуляторные батареи различных электрохимических систем
- ГОСТ Р МЭК 60050-482-2011
. Источники тока химические. Термины и определения.
 4 Al(OH)3,}}}»>
4 Al(OH)3,}}}»>
 2 Al(OH)3 + 3 H2}}}»>
2 Al(OH)3 + 3 H2}}}»>

