Для алкинов характерна структурная и пространственная изомерия
.
Для алкинов характерна структурная и пространственная изомерия
.
Для алкенов характерна структурная и пространственная изомерия
.
Алкины
– углеводороды, в молекуле которых
присутствует тройная связь. Общая
формула алкинов С n
Н 2
n
-2
.
НС

СН – ацетилен
- Общая характеристика алкинов.
- Карбидный метод (промышленный способ)
- Пиролиз углеводородов (промышленный способ)
- Крекинг природного газа (промышленный способ)
- Метод прямого синтеза
- Электролиз солей непредельных карбоновых кислот
- Дегидрогалогенирование галогеналканов и галогеналкенов (лабораторный способ)
- Алкилирование алкинов (лабораторный способ)
- Прочие лабораторные способы получения алкинов
- Гомологический ряд алкенов
- Гидролиз карбида кальция
- «алкины ( ацетиленовые углеводороды).
- Гомологический ряд алкинов
- Дегидратация спиртов
- Дегидрогалогенирование галогеналканов
- Номенклатура алкинов.
- Пиролиз метана
- Изомерия
- 3 – С = СН С1 2 СН 3 – С – СН Сl Сl Сl Сl 1,2-дихлорпропен-1 1,1,2,2-тетрахлорпропан 1.3 Реакция гидрогалогенирования Сl С Н 3 – С СН НС1 СН 3 – С = СН 2 НС1 СН 3 – С – СН 3 Сl Сl 2-хлорпропен 2,2-дихлорпропан В результате реакции все алкины, кроме ацетилена образуют кетоны, ацетилен – альдегид. Реакция протекает через стадию образования енола. Н
Общая характеристика алкинов.
Алкины
—
это
непредельные углеводороды, имеющие в
своем составе одну тройную связь.
Атомы
углерода находятся в состоянии sp
– гибридизации. Валентный угол равен
180˚, длина связи 0,12 нм, Е=820 кДж/моль.
Суффикс,
характерный для алкинов, ин.
В названиях алкинов для обозначения тройной связи используется суффикс -ИН.
Например,
алкин на рисунке называется бутин-2

Для простейших алкинов применяются также исторически сложившиеся (тривиальные) названия:
Радикалы, содержащие тройную связь, также носят тривиальные названия:
В названиях алкинов для обозначения тройной связи используется суффикс -ИН.
Например,
алкин на рисунке называется бутин-2

Для простейших алкинов применяются также исторически сложившиеся (тривиальные) названия:
Радикалы, содержащие тройную связь, также носят тривиальные названия:
– это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна тройная связь между атомами углерода С≡С.
Остановимся на свойствах, способах получения и особенностях строения алкинов.
Строение, изомерия и гомологический ряд алкинов
Химические свойства алкинов
– это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна тройная связь между атомами углерода С≡С.
Остановимся на свойствах, способах получения и особенностях строения алкинов.
Строение, изомерия и гомологический ряд алкинов
Химические свойства алкинов
Дигалогеналканы, в молекулах которых два атома галогена расположены у одного, либо у соседних атомов углерода, реагируют с избытком спиртового раствора щелочей с образованием алкинов.
Например,
1,2-дихлорпропан реагирует со спиртовым раствором гидроксида натрия

1,1-дихлорпропан реагирует со спиртовым раствором щелочи с образованием пропина.
Для алкенов также характерна оптическая изомерия
.
Алкины, которые обладают достаточно большим углеродным скелетом, могут существовать в виде оптических изомеров
. В молекуле алкина должен присутствовать асимметрический
атом углерода
(атом углерода, связанный с четырьмя различными заместителями).
Цис-транс
-изомерия
для алкинов не характерна, так как по тройной связи вращение возможно.
Для некоторых алкинов также характерна оптическая изомерия
.
Алкины, которые обладают достаточно большим углеродным скелетом, могут существовать в виде оптических изомеров
. В молекуле алкина должен присутствовать асимметрический
атом углерода
(атом углерода, связанный с четырьмя различными заместителями).
Цис-транс
-изомерия
для алкинов не характерна, так как по тройной связи вращение возможно.
– это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна двойная связь между атомами углерода С=С.
Наличие двойной связи между атомами углерода очень сильно меняет свойства углеводородов. В этой статье мы подробно остановимся на свойствах, способах получения и особенностях строения алкенов.
Строение, изомерия и гомологический ряд алкенов
Химические свойства алкенов
У этого термина существуют и другие значения, см. Алкин (значения)
.
Алки́ны
( ацетиле́новые углеводоро́ды
) — ациклические
непредельные
углеводороды
, содержащие одну тройную связь
между атомами
углерода
, образующие гомологический ряд с общей формулой C n
H 2n-2
.
Атомы углерода при тройной связи находятся в состоянии sp-гибридизации
и имеют валентный угол
180°. Простейшим алкином является ацетилен
(C 2
H 2
).
По номенклатуре « IUPAC
», названия алкинов образуются от названий соответствующих алканов заменой суффикса « -ан
» на « -ин
»; положение тройной связи указывается арабской цифрой.


В названиях алкенов для обозначения двойной связи используется суффикс -ЕН.
Например,
алкен имеет название 2-метилпропен.

При этом правила составления названий (номенклатура) для алкенов в целом такие же, как и для алканов, но дополняются некоторыми пунктами:
Углеродная цепь, в составе которой есть двойная связь, считается главной.
Нумеруют атомы углерода в главной цепи так, чтобы атомы углерода при двойной связи получили наименьший номер. Нумерацию следует начинать с более близкого к двойной связи
конца цепи.
В конце молекулы вместо суффикса АН добавляют суффикс ЕН и указывают наименьший номер атома углерода при двойной связи в углеродной цепи.
Для простейших алкенов применяются также исторически сложившиеся (тривиальные) названия:
Радикалы, содержащие двойную связь, также носят тривиальные названия:
Основным промышленным
способом получения ацетилена является электро- или термокрекинг метана
, пиролиз
природного газа и карбидный метод.
Карбидный метод (промышленный способ)
Прокаливание смеси оксида кальция
с коксом
в электрических печах при 1800—2000°С приводит к образованию карбида кальция
:
При действии на полученный карбид воды образуется гидроксид кальция
и ацетилен
:
Пиролиз углеводородов (промышленный способ)
Крекинг природного газа (промышленный способ)
Метод прямого синтеза
Взаимодействие углерода
напрямую с водородом
при очень высоких температурах приводит к образованию ацетилена:
Этот метод имеет чисто историческое значение (получение ацетилена в 1863 году
французским химиком М. Бертло
).
Электролиз солей непредельных карбоновых кислот
Аналогично ацетилен образуется из акрилата
натрия.
Этот метод носит чисто историческое значение.
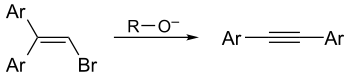
Дегидрогалогенирование галогеналканов и галогеналкенов (лабораторный способ)
Реакция дегидрогалогенирования проводят действием сильного основания на дигалогеналканы:
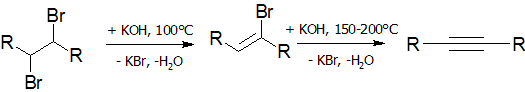

Алкилирование алкинов (лабораторный способ)
См. также: Алкины § Реакции нуклеофильного замещения алкинидов
Алкилирование алкинов с концевой тройной связью производится по следующей схеме:

Прочие лабораторные способы получения алкинов
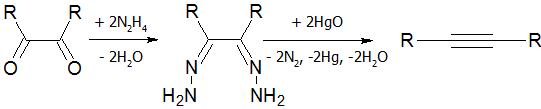
- Реакция Кори-Фукса
— синтез алкинов из альдегидов
[17]
:
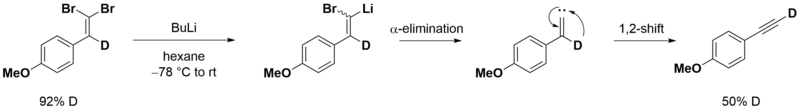
На первой стадии идёт образование дибромалкена:
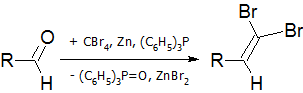
На второй стадии происходит обмен брома
на литий и альфа-элиминирование с последующим превращением винилидена в алкин в результате перегруппировки Фрича-Буттенбергера-Вихеля:
Гомологический ряд алкенов
Все алкены имеют некоторые общие или похожие физические и химические свойства. Схожие по строению алкены, которые отличаются на одну или несколько групп –СН 2
–, называют гомологами
. Такие алкены образуют гомологический ряд.
Самый первый представитель гомологического ряда алкенов – этен (этилен) C 2
H 4
, или СH 2
=СH 2
.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН 2
– в углеводородную цепь.
Общая формула гомологического ряда алкенов C n
H 2n
.
Первые четыре члена гомологического ряда алкенов – газы, начиная с C 5
– жидкости.
Алкены легче воды, не растворимы в воде и не смешиваются с ней.
Гидролиз карбида кальция
Лабораторный способ получения ацетилена – водный или кислотный гидролиз карбида кальция CaC 2
.
СаС 2
+ 2Н 2
О = Са(ОН) 2
+ С 2
Н 2
В кислой среде образуется ацетилен и соответствующая соль:
CaC 2
+ 2HCl = CaCl 2
+ C 2
H 2
Карбид кальция можно получить, нагревая оксид кальция с углеродом:
«алкины ( ацетиленовые углеводороды).
называть алкины по формуле и писать
структурную формулу по названию;выражать
уравнениями реакций способы получения
и химические свойства алкинов;выполнять качественные реакции.
- Миллер С.
Ацетилен, его свойства, получение и применение / Пер. с английского. — М.
: «Наука», 1969. — 680 с. - Общая органическая химия. Стереохимия, углеводороды, галогенсодержащие соединения = Comprehensive Organic Chemistry / Под ред. Д.Бартона и В. Д. Оллиса. — М.
: «Химия», 1981. — Т. 1. — С. 257—270. - Темкин О. Н., Шестаков Г. К., Трегер Ю. А.
Ацетилен: Химия. Механизмы реакций. Технология. — М.
: «Химия», 1991. — 416 с. — ISBN 5724505746
. - Темкин О. Н., Флид Р. М.
Каталитические превращения ацетиленовых соединений в растворах комплексов металлов. — М.
: «Наука», 1968. — 212 с. - Трофимов Б. А.
Гетероатомные производные ацетилена. — М.
: «Наука», 1981. — 319 с. - Henning Hopf.
Polyynes, Arynes, Enynes, and Alkynes / Houben-Weyl Methods of Organic Chemistry. Series Science of synthesis (V. 43). — 5. — Thieme Medical Pub, 2008. — 850 p. — ISBN 9783131189615
.
Гомологический ряд алкинов
Все алкины имеют общие или похожие физические и химические свойства. Схожие по строению алкины, которые отличаются на одну или несколько групп –СН 2
–, называют гомологами
. Такие алкины образуют гомологический ряд.
Первый представитель гомологического ряда алкенов – этин (ацетилен) C 2
H 2
, или СH≡СH.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН 2
– в углеводородную цепь.
Общая формула гомологического ряда алкинов C n
H 2n-2
.
Первые три члена гомологического ряда алкинов – газы, начиная с C 5
Н 8
по С 16
Н 30
– жидкости, начиная с С 17
Н 32
— твердые вещества.
Алкины плохо растворимы в воде и хорошо растворимы в органических растворителях.
В 1862 году
немецкий
химик и врач
Ф. Вёлер
вновь открыл ацетилен
, взаимодействую водой на карбид кальция
.
Большую роль в изучении химии ацетилена и его производных в конце XIX века сыграл русский химик-органик А. Е. Фаворский
.
Дегидратация спиртов
При нагревании спиртов (выше 140 о
С) в присутствии водоотнимающих веществ (концентрированная серная кислота, фосфорная кислота) или катализаторов (оксид алюминия) протекает дегидратация. Дегидратация — это отщепление молекул воды.
При дегидратации спиртов образуются алкены.
Например,
при дегидратации этанола при высокой температуре образуется этилен .

Дегидратация более сложных молекул также протекает по правилу Зайцева.
Например,
при дегидратации бутанола-2 преимущественно образуется бутен-2 .

Дегидрогалогенирование галогеналканов
Галогеналканы взаимодействуют с щелочами
в спиртовом растворе. При этом происходит дегидрогалогенирование – отщепление (элиминирование) атомов водорода и галогена от галогеналкана.
Например
, при взаимодействии хлорэтана с спиртовым раствором гидроксида натрия образуется этилен.
Номенклатура алкинов.
Названия алкинам по
международной систематической
номенклатуре дают следующим образом:
Выбирают наиболее
длинную углеродную цепь (в нее обязательно
должна входить тройная связь).Нумеруют с того
конца, к которому ближе тройная связь
(старшинство тройной связи).
Цифры
впереди показывают местоположение
боковых цепей. Затем называют сами
боковые цепи, затем основную цепь с
суффиксом инна конце.
Цифры в конце показывавют положение
тройной связи.
1 2 3
4 5 6
СН ≡ С ― С ― СН 2
― СН ― СН 3
│ │
СН 3
СН 3
3,5 – диметилгексин – 1
Пиролиз метана
Пиролиз метана –
это промышленный способ получения ацетилена.

Реакцию проводят, очень быстро пропуская метан между электродами (электродуговой способ) — примерно 0,1-0,01 секунды при температуре 1500 о
С.
Если процесс проводить дольше, то метан разлагается на углерод и водород:

Изомерия
Для
алкинов характерна структурная изомерия
углеводородного скелета и изомерия
положения тройной связи.
Пример:
СН 3
СН 3
СН 3
– СН – СН 2
– С

СН и СН 3
– СН 2
– СН – С

СН
4-метилпентин-1
3-метилпентин-1
СН 3
– СН 2
– С

СН и СН 3
– С

С – СН 3
бутин-1
бутин-2
Реакция
протекает по правилу Зайцева.
1.1
Использованы вицинальные
дигалогенопроизводные
(атомы галогена расположены у соседних
атомов углерода).
Пример:
Сl
Сl
С 
2
Н 5
– СН – СН – СН 3
-2NaC1;-2H 2
O
С 2
Н 5
– С

С – СН 3
2,3-дихлорпентан
пентин-2
1.2
Использованы геминальные
дигалогенопроизводные (атомы галогена
расположены у одного атома углерода).
Пример:
СI

СН 3
– С – СН 2
– СН 3
+ 2NaOH (
c
)
СН 3
– С

С – СН 3
метилацетиленид
натрия этилбромид пентин-2
ацетиленидмагнийбромид
метилбромид пропин
3. Получение
ацетилена
из карбида кальция
СаС 2
+ 2Н 2
О
= НС

СН
Химические
свойства в молекуле алкина определяются
строением тройной связи. Тройная связь
состоит из двух

и одной 
— связей. В молекуле алкина атомы углерода,
соединенные тройной связью, расположены
ближе друг к другу, чем в молекуле алкена. 
— электроны тройной связи втянуты внутрь
молекулы, поэтому положительно заряженные
атомы углерода менее экранированы с
внешней стороны. Следовательно, алкины труднее
чем алкены вступают в реакции
электрофильного присоединения (А E
)
и легче
в реакции нуклеофильного присоединения
(А N
).
Данный
тип реакций протекает по правилу
Марковникова в две стадии с последовательным
разрывом

— связей.


СН 3
– С

СН +Н 2
;Pt
CH 3
– CH
= CH 2
+ H2;Pt
CH 3
– CH 2
– CH 3
пропин
пропен
пропан
1.2
Реакция галогенирования
Сl
Сl
 СН
СН
– С
СН С1
2
СН
3
– С = СН С1
2 
СН  3
3
– С – СН
Сl
Сl
Сl
Сl
1,2-дихлорпропен-1
1,1,2,2-тетрахлорпропан
1.3
Реакция
гидрогалогенирования
Сl
С
Н
3
– С
СН НС1 СН 3
– С = СН
2
НС1 СН
3
– С – СН
- 3
Сl
Сl
2-хлорпропен
2,2-дихлорпропан
В
результате реакции все алкины, кроме
ацетилена образуют кетоны, ацетилен –
альдегид. Реакция протекает через стадию
образования енола.
Н
СН НОН СН
2
= СН – ОН СН 3
– СН = О
Hg
2+
,
H
+
енол этаналь
СН 3
– С
СН +НОН СН
3
– С = СН 2
СН 3
– С – СН
3
OH
O
енол
пропанон-2

Данный
тип реакций протекает по правилу
Марковникова в одну стадию.
2.1
Реакция с синильной
кислотой
H
С
СН +HCN
CH
2
= CH
— CN
 2.2
2.2
Реакция со
спиртами
В
результате данной реакции образуются
простые
эфиры.
Н
С
СН + С 2
Н 5
ОН
СН  2
2
= СН – ОС 2
Н 5 
этанол
этилвиниловый эфир
2.3
Реакция с карбоновыми
кислотами
В
результате данной реакции образуются
сложные
эфиры. 
Н
С
СН + СН
3
СООН
СН
2
= СН – ОСОСН
3
этановая
кислота уксусновиниловый эфир
3.
Реакции электрофильного
замещения
(S
E
)
Данный
тип реакций связан с отщеплением протона
водорода от атома углерода тройной
связи. В связи С-Н электроны сильнее
притягиваются к атому углерода, т.е.
связь поляризуется и водород способен
отщепляться в виде протона, что указывает
на проявление алкинами кислотных
свойств.
3.1
Образование ацетиленидов
и их производных,
реакция
металлирования
.
В
качестве реагентов могут использоваться:
амид натрия
; магнийорганические
соединения (реактив Гриньяра)
; аммиачные
растворы гидроксида меди или серебра
.

1.
СН 3
– С

СН +NaNH 2
CH 3
– C

C
– Na
+ NH 3
амид
натрия метилацетиленид натрия

2.
СН 3
– С

СН +CH 3
Mg
J
CH 3
– C

C
−MgJ
+ CH 4
3.
СН 3
– С

СН +Ag(NH 3
) 2
OH
CH 3
– C

C−Ag
+ 2NH 3
+ H 2
O
аммиачный
раствор метилацетиленид серебра
3.2
Конденсация
с альдегидами и кетонами
В
результате данной реакции образуются
спирты с тройной связью (алкинолы).
П 

ример:
ОН
С 


Н 3
– С

СН + СН 3
– СН = О СН 3
– С

С – СН – СН 3
этаналь
пентин-2-ол-4

О
ОН



СН 3
– С

СН + СН 3
– С – СН 3
СН 3
– С

С – С – СН 3
Процесс
окисления алкинов протекает в две стадии
через образование оксосоединений до
карбоновых кислот.
ример:
O
O
С 

Н 3
– С

СНCH 3
– C
– C−H
CH 3
COOH
+ HCOOH
альдегидокетон
Н 2
О
этановая метановая
Контрольные
вопросы по теме «Алкины»
1.
В чем особенности изомерии алкинов?
2.
Почему для алкинов реакции А N
протекают легче, чем А E
?
3. Почему
реакции А E
в алкинах протекают ступенчато через
стадию образования производных алкенов?
4.
Почему алкины проявляют слабые кислотные
свойства?
5.
Какие классы соединений образуются при
окислении алкинов?
- Этин
(ацетилен): C 2
H 2
; - Пропин
: C 3
H 4
; - Бутин
-1: C 4
H 6
; - Пентин
-1: C 5
H 8
; - Гексин
-1: C 6
H 10
; - Гептин
-1: C 7
7
H12
;
#
#
#
#
#

 Реакции присоединения
Реакции присоединения
Тройная связь состоит из σ-связи и двух π-связей. Сравним характеристики одинарной связи С–С, тройной связи СС и связи С–Н:
Таким образом, тройная связь короче, чем одинарная связь , поэтому π-электроны тройной связи прочнее удерживаются ядрами атомов углерода и обладают меньшей поляризуемостью и подвижностью. Реакции присоединения
по тройной связи к алкинам протекают сложнее, чем реакции присоединения по двойной связи к алкенам.
Для алкинов характерны реакции присоединения по тройной связи СС с разрывом π-связей.

Гидрирование алкинов протекает в присутствии катализаторов (Ni, Pt) с образованием алкенов, а затем сразу алканов. 
Например,
при гидрировании бутина-2 в присутствии никеля образуется сначала бутен-2, а затем бутан.

 При использовании менее активного катализатора (Pd, СaCO
При использовании менее активного катализатора (Pd, СaCO
3
, Pb(CH
3
COO)
2
) гидрирование останавливается на этапе образования алкенов.
Например,
при гидрировании бутина-1 в присутствии палладия преимущественно образуется бутен-1.
1.2. Галогенирование алкинов
Присоединение галогенов к алкинам происходит даже при комнатной температуре в растворе (растворители — вода, CCl 4
).
При взаимодействии с алкинами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это
качественная реакция на тройную связь.
Например,
при бромировании пропина сначала образуется 1,2-дибромпропен, а затем — 1,1,2,2-тетрабромпропан.


Аналогично алкины реагируют с хлором, но обесцвечивания хлорной воды при этом не происходит, потому что хлорная вода и так бесцветная)
Реакции протекают в присутствии полярных растворителей по ионному (электрофильному) механизму.
1.3. Гидрогалогенирование алкинов
Алкины присоединяют галогеноводороды. Реакция протекает по механизму электрофильного присоединения с образованием галогенопроизводного алкена или дигалогеналкана.
Например,
при взаимодействии ацетилена с хлороводородом образуется хлорэтен, а затем 1,1-дихлорэтан.


При присоединении галогеноводородов и других полярных молекул к симметричным алкинам образуется, как правило, один продукт реакции, где оба галогена находятся у одного атома С.
При присоединении полярных молекул к несимметричным алкинам образуется смесь изомеров. При этом выполняется правило Марковникова.
Правило Марковникова:
при присоединении полярных молекул типа НХ к несимметричным алкинам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода
при двойной связи.
Например,
при присоединении хлороводорода HCl к пропину преимущественно образуется 2-хлорпропен.


1.4. Гидратация алкинов
Гидратация (присоединение воды) алкинов протекает в присутствии кислоты и катализатора (соли ртути II).
Сначала образуется неустойчивый алкеновый спирт, который затем изомеризуется в альдегид или кетон.
Например,
при взаимодействии ацетилена с водой в присутствии сульфата ртути образуется уксусный альдегид.

Гидратация алкинов протекает по ионному (электрофильному) механизму.
Для несимметричных алкенов присоединение воды преимущественно по правилу Марковникова.
Например,
при гидратации пропина образуется пропанон (ацентон).

1.5. Димеризация, тримеризация и полимеризация
Присоединение одной молекулы ацетилена к другой ( димеризация
) протекает под действием аммиачного раствора хлорида меди (I). При этом образуется винилацетилен:

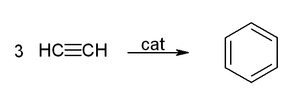
Тримеризация
ацетилена (присоединение трех молекул друг к другу) протекает под действием температуры, давления и в присутствии активированного угля с образованием бензола (реакция Зелинского):

Алкины также вступают в реакции полимеризации
— процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
Например,
при полимеризации ацетилена образуется полимер линейного или циклического строения.
Химические свойства алкинов
– непредельные углеводороды, в молекулах которых есть одна тройная связь. Строение и свойства тройной связи определяют характерные химические свойства алкинов. Химические свойства алкинов схожи с химическими свойствами алкенов из-за наличия кратной связи в молекуле.
 Для алкинов характерны реакции окисления. Окисление алкинов протекает преимущественно по тройной связи, хотя возможно и жесткое окисление (горение).
Для алкинов характерны реакции окисления. Окисление алкинов протекает преимущественно по тройной связи, хотя возможно и жесткое окисление (горение). 
Окисление алкинов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
2.1. Горение алкинов
Алкины, как и прочие углеводороды, горят с образованием углекислого газа и воды.
Уравнение сгорания алкинов в общем виде:
Например
, уравнение сгорания пропина:
2.2. Окисление алкинов сильными окислителями
Алкины реагируют с сильными окислителями (перманганаты или соединения хрома (VI)). При этом происходит окисление тройной связи С≡С и связей С-Н у атомов углерода при тройной связи
. При этом образуются связи с кислородом.
При окислении трех связей у атома углерода в кислой среде образуется карбоксильная группа СООН, четырех — углекислый газ СО 2
. В нейтральной среде — соль карбоновой кислоты и карбонат (гидрокарбонат) соответственно.
Таблица соответствия окисляемого фрагмента молекулы и продукта:
При окислении бутина-2 перманганатом калия в среде серной кислоты окислению подвергаются два фрагмента СН 3
–C, поэтому образуется уксусная кислота:

При окислении 3-метилпентина-1 перманганатом калия в серной кислоте окислению подвергаются фрагменты R–C и H–C , поэтому образуются карбоновая кислота и углекислый газ:

При окислении алкинов сильными окислителями в нейтральной среде углеродсодержащие продукты реакции жесткого окисления (кислота, углекислый газ) могут реагировать с образующейся в растворе щелочью в соотношении, которое определяется электронным балансом с образованием соответствующих солей.
Например
, при окислении бутина-2 перманганатом калия в воде при нагревании окислению подвергаются два фрагмента R–C, поэтому образуется соль уксусной кислоты – ацетат калия

Аналогичные органические продукты образуются при взаимодействии алкинов с хроматами или дихроматами.
Окисление ацетилена
протекает немного иначе, σ-связь С–С не разрывается, поэтому в кислой среде образуется щавелевая кислота:

В нейтральной среде образуется соль щавелевой кислоты – оксалат калия:

Обесцвечивание раствора перманганата калия — качественная реакция на тройную связь.
Простейшим алкином является этин (ацетилен C 2
H 2
)
. По номенклатуре « IUPAC
» названия алкинов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ин»; положение тройной связи указывается арабскими цифрами.
Углеводородные радикалы, образованные от алкинов имеют суффикс «-ини́л», так CH≡C-
называется « «этини́л»
».
Ниже представлены некоторые представители алкинов и их названия:

Различают внутреннюю
тройную связь (пример: бут-2-ин) и концевую
(пример: бут-1-ин).
Гомологический ряд
алкинов
:
Октин
-1: C 8
H 14
;

Нонин
-1: C
9
H 16
;
 Децин
Децин 
-1: C 10
H
18
.
В противном случае, разница в положении тройной связи в двух разных молекулах алкинов (например, бутин-1 и пентин-2) будет сигнализировать о том, что эти вещества будут являтся структурными изомерами по положению связи.
Из всех ацетиленовых углеводородов серьёзное промышленное значение имеет только ацетилен
, который является важнейшим химическим сырьём.
Ацетилен используют для синтеза следующих продуктов:
- тетрахлорэтан
, трихлорэтилен
, дихлорэтилен
(хлорирование ацетилена)
— растворители; - акрилонитрил
( конденсация
ацетилена с циановодородом)
— для получения полиакрилонитрила
; - акриламид
( конденсация
ацетилена с CO и аммиаком)
— для получения полиакриламида
; - тетрагидрофуран
( конденсация
ацетилена с формальдегидом с последующим гидрированием и дегидратацией)
— важный растворитель, сырьё для уретановых полимеров; - винилхлорид
(гидрохлорирование ацетилена)
— для получения поливинилхлорида
; - винилацетат
( конденсация
с уксусной кислотой)
— для получения поливинилацетата
; - ацетальдегид
(гидратация ацетилена)
— для дальнейшего получения уксусной кислоты
, ацетона
и др. продуктов; - бутиленгликоль
( конденсация
ацетилена с формальдегидом с последующим гидрированием)
— для получения полиуретанов
, полиэфиров
, пластификаторов. - винилацетилен
(димеризация ацетилена)
— полупродукт для синтеза полимеров; - хлоропрен
(гидрохлорирование винилацетилена)
— для получения хлоропреновых каучуков
; - бутадиен
(дегидратация бутиленгликоля)
— для получения бутадиеновых каучуков
;
Кислотные свойства алкинов
Связь атома углерода при тройной связи (атома углерода в sp-гибридизованном состоянии) с водородом значительно более полярная. чем связь С–Н атома углерода при двойной или одинарной связи (в sp 2
и sp 3
-гибридном состоянии соответственно). Это обусловлено большим вкладом s-орбитали в гибридизованное состояние.
Повышенная полярность связи С–Н у атомов углерода при тройной связи в алкинах приводит к возможности отщепления протона Н +
, т.е. приводит к появлению у алкинов с тройной связью на конце молекулы (алкинов-1) кислотных свойств
.
Ацетилен и его гомологи с тройной связью на конце молекулы R–CC–H проявляют слабые кислотные свойства
, атомы водорода на конце молекулы могут легко замещаться на атомы металлов.
Алкины с тройной связью на конце молекулы взаимодействуют с активными металлами, гидридами, амидами металлов и т.д.
Например
, ацетилен взаимодействует с натрием с образованием ацетиленида натрия.

Например
, пропин взаимодействует с амидом натрия с образованием пропинида натрия.

Алкины с тройной связью на конце молекулы взаимодействуют с аммиачным раствором оксида серебра (I) или аммиачным раствором хлорида меди (I).
При этом образуются нерастворимые в воде ацетилениды серебра или меди (I):

Алкины с тройной связью на конце молекулы взаимодействуют с аммиачным раствором оксида серебра
или аммиачным раствором хлорида меди (I)
с образованием белого или красно-коричневого осадка
соответственно. Это качественная реакция
на алкины с тройной связью на конце молекулы.
Соответственно, алкины, в которых тройная связь расположена не на конце молекулы, не реагируют с аммиачными растворами оксида серебра или хлорида меди (I).

Структурная изомерия
Для алкенов характерна структурная изомерия – изомерия углеродного скелета, изомерия положения кратной связи и межклассовая изомерия
.
Структурные изомеры
— это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета
отличаются строением углеродного скелета.
Изомеры с различным углеродным скелетом и с формулой С 4
Н 8
— бутен-1 и метилпропен
Межклассовые изомеры —
это вещества разных классов с различным строением, но одинаковым составом. Алкены являются межклассовыми изомерами с циклоалканами. Общая формула и алкенов, и циклоалканов — C n
H 2n
.
Межклассовые изомеры с общей формулой С 3
Н 6
— пропилен и циклопропан
Изомеры с различным положением двойной связи
отличаются положением двойной связи в углеродном скелете.
Изомеры положения двойной связи, которые соответствуют формуле С 4
Н 8
— бутен-1 и бутен-2
Реакции присоединения
Для алкенов характерны реакции присоединения по двойной связи С=С, при которых протекает разрыв пи-связи в молекуле алкена.
Алкены реагируют с водородом при нагревании и под давлением в присутствии металлических катализаторов (Ni, Pt, Pd и др.).
Например,
при гидрировании бутена-2 образуется бутан.

Реакция протекает обратимо. Для смещения равновесия в сторону образования бутана используют повышенное давление.
1.2. Галогенирование алкенов
Присоединение галогенов к алкенам происходит даже при комнатной температуре в растворе (растворители — вода, CCl 4
).
При взаимодействии с алкенами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на двойную связь.
Например,
при бромировании пропилена образуется 1,2-дибромпропан, а при хлорировании — 1,2-дихлорпропан.


Реакции протекают в присутствии полярных растворителей по ионному (электрофильному) механизму.
1.3. Гидрогалогенирование алкенов
Алкены присоединяют галогеноводороды. Реакция идет по механизму электрофильного присоединения с образованием галогенопроизводного алкана.
Например,
при взаимодействии этилена с бромоводородом образуется бромэтан.

При присоединении полярных молекул к несимметричным алкенам образуется смесь изомеров. При этом выполняется правило Марковникова.
Правило Марковникова:
при присоединении полярных молекул типа НХ к несимметричным алкенам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода
при двойной связи.
Например,
при присоединении хлороводорода HCl к пропилену атом водорода преимущественно присоединяется к атому углерода группы СН 2
=, поэтому преимущественно образуется 2-хлорпропан.

Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
Например,
при взаимодействии этилена с водой образуется этиловый спирт.

Гидратация алкенов также протекает по ионному (электрофильному) механизму.
Для несимметричных алкенов реакция идёт преимущественно по правилу Марковникова.
Например,
при взаимодействии пропилена с водой образуется преимущественно пропанол-2.

Полимеризация
— это процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
Например,
при полимеризации этилена образуется полиэтилен, а при полимеризации пропилена — полипропилен.


Гидрирование алкинов
Гидрирование алкинов протекает в присутствии катализаторов (Ni, Pt) с образованием алкенов, а затем сразу алканов.
При использовании менее активного катализатора (Pd, СaCO 3
, Pb(CH 3
COO) 2
) гидрирование останавливается на этапе образования алкенов.
Например,
при гидрировании бутина-1 в присутствии палладия преимущественно образуется бутен-1.

Алкины по своим физическим свойствам напоминают соответствующие алкены
. Низшие (до С 4
) — газы без цвета и запаха, имеющие более высокие температуры кипения, чем аналоги в алкенах. Алкины плохо растворимы в воде, лучше — в органических растворителях.
* Значения измерены при температуре кипения.
Гомологический ряд алкинов
Все алкины имеют общие или похожие физические и химические свойства. Схожие по строению алкины, которые отличаются на одну или несколько групп –СН 2
–, называют гомологами
. Такие алкины образуют гомологический ряд.
Первый представитель гомологического ряда алкенов – этин (ацетилен) C 2
H 2
, или СH≡СH.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН 2
– в углеводородную цепь.
Общая формула гомологического ряда алкинов C n
H 2n-2
.
Первые три члена гомологического ряда алкинов – газы, начиная с C 5
Н 8
по С 16
Н 30
– жидкости, начиная с С 17
Н 32
— твердые вещества.
Алкины плохо растворимы в воде и хорошо растворимы в органических растворителях.
Качественной реакцией на алкины с концевой тройной связью является взаимодействие алкина с аммиакатом серебра
или меди
( подробнее см. подраздел
: « Образование алкинидов
»).
Дегидрирование алканов
При дегидрировании алканов, содержащих от двух до трех атомов углерода в молекуле, образуются двойные и тройные связи.
Например
, при дегидрировании этана может образоваться этилен или ацетилен:

Химические свойства алкенов
– непредельные углеводороды, в молекулах которых есть одна двойная связь. Строение и свойства двойной связи определяют характерные химические свойства алкенов.
Двойная связь состоит из σ-связи и π-связи. Рассмотрим характеристики одинарной связи С-С и двойной связи С=С:
Можно примерно оценить энергию π-связи в составе двойной связи С=С:
Е π
= Е (С=С)
— Е (С-С)
= 620 — 348 = 272 кДж/моль
Таким образом, π-связь — менее прочная, чем σ-связь. Поэтому алкены вступают в реакции присоединения, сопровождающиеся разрывом π-связи. Присоединение к алкенам может протекать по ионному и радикальному механизмам.
Для алкенов также характерны реакции окисления и изомеризации. Окисление алкенов протекает преимущественно по двойной связи, хотя возможно и жесткое окисление (горение).
Систематическая номенклатура (июпак)
Порядок
названия соединений по данной номенклатуре
идентичен алкенам с заменой суффикса
–ен
на
–ин
.
Пример:
4 3 2 1
С 



Н 3
– СН – СН 2
– С

СН



5,6,7
С 3
Н 7
4-метилгептин-1
Рациональная номенклатура
По
аналогии с алкенами называются соединения
по рациональной номенклатуре с заменой
этилена
на
ацетилен
и
отсутствием симметричности.
С 




Н 3
– С

С – СН – СН 3
Алкилирование соединений алкинов с металлами
Ацетилениды, пропиниды и прочие соединения алкинов с металлами реагируют с галогеналканами с образованием гомологов алкинов. При этом происходит удлиннение исходной молекулы алкина.
Например,
пропинид натрия реагирует с бромэтаном с образованием пентина-2

Физические свойства.
с
С2
по С4
― газы
с
С5
по С15
― жидкости
с
С17
― твердые вещества
в
воде не растворимы, хорошо растворимы
в органических растворителях.
Окисление алкенов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
2.1. Каталитическое окисление
Каталитическое окисление протекает под действием катализатора.
Взаимодействие этилена с кислородом в присутствии солей палладия протекает с образованием этаналя (уксусного альдегида)

Взаимодействие этилена с кислородом в присутствии серебра протекает с образованием эпоксида

2.2. Мягкое окисление
Мягкое окисление протекает при низкой температуре в присутствии перманганата калия. При этом раствор перманганата обесцвечивается.
В молекуле алкена разрывается только π-связь
и окисляется каждый атом углерода при двойной связи.
При этом образуются двухатомные спирты (диолы).

Например
, этилен реагирует с водным раствором перманганата калия при низкой температуре с образованием этиленгликоля (этандиол-1,2)

2.2. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) происходит полный разрыв двойной связи С=С и связей С-Н у атомов углерода при двойной связи
. При этом вместо разрывающихся связей образуются связи с кислородом.
Так, если у атома углерода окисляется одна связь, то образуется группа С-О-Н (спирт). При окислении двух связей образуется двойная связь с атомом углерода: С=О, при окислении трех связей — карбоксильная группа СООН, четырех — углекислый газ СО 2
.
Поэтому можно составить таблицу соответствия окисляемого фрагмента молекулы и продукта:
При окислении бутена-2 перманганатом калия в среде серной кислоты окислению подвергаются два фрагмента –CH=, поэтому образуется уксусная кислота:

При окислении метилпропена перманганатом калия в присутствии серной кислоты окислению подвергаются фрагменты >C= и CH 2
=, поэтому образуются углекислый газ и кетон:

При жестком окислении алкенов в нейтральной среде образующаяся щелочь реагирует с продуктами реакции окисления алкена, поэтому образуются соли
(кроме реакций, где получается кетон
— кетон со щелочью не реагирует).
ри окислении бутена-2 перманганатом калия в воде при нагревании окислению подвергаются два фрагмента –CH=, поэтому образуется соль уксусной кислоты – ацетат калия:

Например
, при окислении метилпропена перманганатом калия в воде при нагревании окислению подвергаются фрагменты >C= и CH 2
=, поэтому образуются карбонат калия и кетон:

Взаимодействие алкенов с хроматами или дихроматами протекает с образованием аналогичных продуктов окисления.
2.3. Горение алкенов
Алкены, как и прочие углеводороды, горят в присутствии кислорода с образованием углекислого газа и воды.
В общем виде уравнение сгорания алкенов выглядит так:
Например
, уравнение сгорания пропилена:
3. Замещение в боковой цепи
Алкены с углеродной цепью, содержащей более двух атомов углерода, могут вступать в реакции замещения в боковой цепи, как алканы.

При взаимодействии алкенов с хлором или бромом при нагревании до 500 о
С или на свету происходит не присоединение, а радикальное замещение атомов водорода в боковой цепи. При этом хлорируется атом углерода, ближайший к двойной связи.
Например
, при хлорировании пропилена на свету образуется 3-хлорпропен-1

4. Изомеризация алкенов
При нагревании в присутствии катализаторов (Al 2
O 3
) алкены вступают в реакцию изомеризации. При этом происходит либо перемещение двойной связи, либо изменение углеродного скелета. При изомеризации из менее устойчивых алкенов образуются более устойчивые. Как правило, двойная связь перемещается в центр молекулы.
Например
, при изомеризации бутена-1 может образоваться бутен-2 или 2-метилпропен

Алкины (ацетиленовые углеводороды)
Алкины
– это углеводороды, в молекулах которых два атома углерода находятся в состоянии sp-гибридизации и связаны друг с другом тройной связью.
Алкины
( ацетиленовые углеводороды
) – непредельные алифатические (ациклические) углеводороды, молекулы которых содержат одну тройную связь.
Ацетиленовыми углеводородами
( алкинами
) называются непредельные (ненасыщенные) углеводороды, содержащие в молекуле одну тройную связь и имеющие общую формулу C n
H 2
n
-2
.
Первый представитель этого класса – ацетилен НС≡СН, в связи с этим алкины называют ацетиленовыми углеводородами.
Общая формула
гомологического ряда совпадает с общей формулой алкадиенов, поэтому алкины и алкадиены являются межклассовыми изомерами.
Ацетилен
– первый член гомологического ряда ацетиленовых углеводородов, или алкинов.
Молекулярная формула ацетилена
C 2
H 2
Структурная формула ацетилена
H–C≡C–H
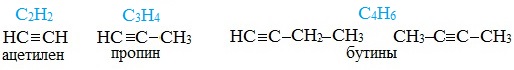
Модели молекул
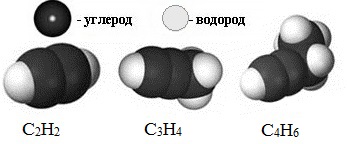
Крекинг алканов
Крекинг –
это реакция разложения алкана с длинной углеродной цепью на алканы и алкены с более короткой углеродной цепью.
Крекинг бывает термический и каталитический
.
Термический крекинг
протекает при сильном нагревании без доступа воздуха.
При этом получается смесь алканов и алкенов с различной длиной углеродной цепи и различной молекулярной массой.
Например,
при крекинге н-пентана образуется смесь, в состав которой входят этилен, пропан, метан, бутилен, пропилен, этан и другие углеводороды.

Каталитический крекинг
проводят при более низкой температуре в присутствии катализаторов. Процесс сопровождается реакциями изомеризации и дегидрирования.
Катализаторы каталитического крекинга – цеолиты (алюмосиликаты кальция, натрия).
Дегалогенирование дигалогеналканов
Дигалогеналканы, в молекулах которых два атома галогена расположены у соседних атомов углерода, реагируют с активными металлами с образованием алкенов.
Как правило, для отщепления используют двухвалентные активные металлы — цинк или магний.
Например,
1,2-дихлорпропан реагирует с цинком с образованием пропилена

Для алкинов характерны реакции
присоединения
. В отличие от алкенов
, которым свойственны реакции электрофильного присоединения
, алкины могут вступать также и в реакции нуклеофильного присоединения
. Это обусловлено значительным s-характером связи и, как следствие, повышенной электроотрицательностью атома углерода. Кроме того, большая подвижность атома водорода при тройной связи обусловливает кислотные свойства алкинов в реакциях замещения
.
Кислотные свойства алкинов и реакции нуклеофильного замещения
Пропинид серебра представляет собой осадок белого цвета, пропинид меди
— осадок жёлтого цвета, наконец, диацетиленид меди
— осадок красного цвета.
Реакции нуклеофильного замещения алкинидов
Алкиниды являются сильными нуклеофилами и легко вступают в реакции нуклеофильного замещения
:
Это, в частности, широко используется для синтеза гомологов ацетилена:
Реакция нуклеофильного замещения алкинидов
В случае реакции с вторичными или третичными галогеналканами реакция во многом идёт по альтернативному пути (элиминирование):

Аналогично протекает и реакция Куртца
(катализатор — ацетиленид меди):
Реакция идёт в присутствии солей меди (I).
Реакции электрофильного присоединения
Электрофильное присоединение
к алкинам инициируется под воздействием положительно заряженной частицы — электрофила
. В общем случае, катализатором таких реакций являются кислоты
.
Общая схема первой стадии реакции электрофильного присоединения:

Алкины способны присоединять одну или две молекулы галогена с образованием соответствующих галогенпроизводных:
Галогенирование алкинов идёт как транс
-присоединение (как правило) и протекает по аналогии с галогенированием алкенов
.
Вместе с тем, присоединение по тройной связи идёт труднее, чем по двойной, в связи с чем при наличии в соединении как двойной, так и тройной связи, возможно провести избирательное присоединение:

Присоединение хлороводорода
и бромоводорода
к алкинам происходит по аналогии с алкенами.
Реакция идёт в две стадии: сперва образуется галогеналкен, который далее переходит в дигалогеналкан:
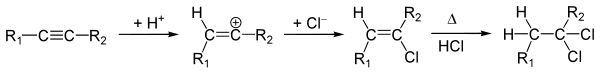
Несмотря на бо́льшую электроотрицательность галогенов, обе стадии реакции идут по правилу Марковникова
.
В присутствии солей ртути
алкины присоединяют воду с образованием ацетальдегида
(для ацетилена
) или кетона
(для прочих алкинов). Эта реакция известна как « реакция Кучерова
».
Считается, что процесс гидратации идёт через стадию образования енола
:

где Х: ОН, OR, OCOR, NH 2
и пр.
Отдельно стоит упомянуть реакцию оксилительного карбохлорирования:
Прочие реакции электрофильного присоединения
- Присоединение карбоновых кислот
с образованием диэфиров
:
Взаимодействие уксусной кислоты
с ацетиленом
образует винилацетат
:
Ацетиленовые углеводороды присоединяют CO 2
и вторичные амины
с образованием амидов
:
- Взаимодействие ацетилена
с цианистым водородом
в присутствии солей одновалентной меди приводит к образованию акрилонитрила
:
- Ацетилен
способен в присутствии катализаторов присоединять углеводороды
с образованием новых С-С связей [20]
:
Реакции нуклеофильного присоединения
Нуклеофильное присоединение к алкинам инициируется под воздействием отрицательно заряженной частицы — нуклеофила
. В общем случае, катализатором таких реакций являются основания
.
Общая схема первой стадии реакции нуклеофильного присоединения:

Типовые реакции нуклеофильного присоединения
- Характерным примером реакции нуклеофильного присоединения является « реакция Фаворского
» — присоединение спиртов
в присутствии щелочей
с образованием алкенильных эфиров:
- Первичные амины
под действием оснований присоединяются к алкинам с образованием иминов [23]
:
При высокой температуре в присутствии катализатора имин дегидрируется и превращается в ацетонитрил
:
- В среде очень сильных оснований (например: КОН
+ ДМСО
) ацетилен реагирует с сероводородом
, образуя дивинилсульфид [20]
:
Реакции радикального присоединения
В присутствии перекисей или других условиях, способствующих образованию свободных радикалов, присоединение к алкинам идёт по радикальному механизму — против правила Марковникова
(« эффект Караша
»):
По свободнорадикальному механизму
* может протекать реакция алкинов с тиолами:
* — В присутствии оснований реакция идёт по нуклеофильному механизму.
Аналогично происходит присоединение карбенов:

Реакциями этинилирования называют реакции увеличения углеродного скелета алкинов с сохранением тройной связи. Они могут протекать как по электрофильному, так и нуклеофильному механизму в зависимости от среды и условий реакции, характера субстрата, а также типа используемого катализатора.
Получение ацетиленовых спиртов
Важнейшей реакцией из этой группы является присоединения формальдегида
к ацетилену
с образованием пропаргилового спирта
и далее бутин-2-диола-1,4 *
:
* Бутин-2-диол-1,4 является важным промежуточным полупродуктом для получения бутиленгликоля, γ-Бутиролактона , изопрена и тетрагидрофурана .
Эту реакцию разработал в 1925 году
В. Реппе
(« реакция Фаворского-Реппе
»). Она протекает при высоком давлении в присутствии ацетиленида меди.
Получение ацетиленовых эфиров и кислот
Катализаторы: PdCl 2
, CuCl
.
На первой стадии образуется алкен
, который практически сразу же гидрируется до алкана
:
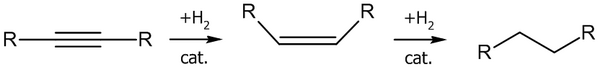
Для остановки реакции на стадии получения алкена используют катализаторы Линдлара
(Pd/PbO/CaCO 3
) или борид никеля.
При гидрировании ацетилена
на никель-кобальтовом катализаторе можно получить изобутилен
:
Гомогенное гидрирование проводят с амидом натрия
в жидком аммиаке
или алюмогидридом лития
в тетрагидрофуране
. В ходе реакции образуются транс
-алкены.

Алкины легко присоединяют диборан
против правила Марковникова
, образуя цис
-алкенилбораны:
По аналогии с реакциями алкенов, алкины вступают в реакцию восстановительного карбоксилирования.
В зависимости от условий реакции и типов катализаторов, конечными продуктами могут стать спирты
, альдегиды
или алканы
:
Реакции окислительного присоединения
Ацетилен
, в зависимости от окислителя может давать три продукта:
( щавелевая кислота
) — окисление KMnO 4
в кислой среде или HNO 3
в присутствии PdCl 2
.
Отдельный тип реакций — реакции окислительного карбоксилирования.
В растворах комплексов палладия
образуются эфиры малеиновой кислоты:
Реакции окислительного расщепления
При действии сильных окислителей в жёстких условиях алкины окисляются с разрывом тройной связи. В ходе реакции образуются карбоновые кислоты и CO 2
:
Реакции окислительного сочетания
В присутствии солей одновалентной меди
в спиртовом растворе аммиака
алкины окисляются кислородом воздуха до диацетиленов (« реакция Глазера
»):
Реакция для ацетилена может идти c образованием полиинов:
Реакции олигомеризации, полимеризации и циклообразования
В присутствии солей меди(I) и хлорида аммония
в водной среде ацетилен вступает в реакцию олигомеризации с образованием винилацетилена
:
Реакция может идти дальше с образованием дивинилацетилена:
Реакция была впервые открыта Ю. Ньюлендом и служит первой промышленной стадией для синтеза хлоропрена
.
В ходе реакции был получен полукристаллический полиацетилен
.
Ацетилен под действием катализаторов — раскалённого активированного угля при 500 °С ( реакция Зелинского
) или органоникелевого катализатора (например, тетракарбонила никеля
) при 60 °С и повышенном давлении ( реакция Реппе
) — достаточно легко циклотримеризуется, образуя бензол
, а в других условиях (катализатор — цианид никеля(II) в ТГФ) — циклооктатетраен
:
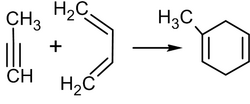
Важной способностью алкинов является их возможность вступать в реакцию Дильса-Альдера
:
Реакции образования гетероциклов
Образование производных пиррола
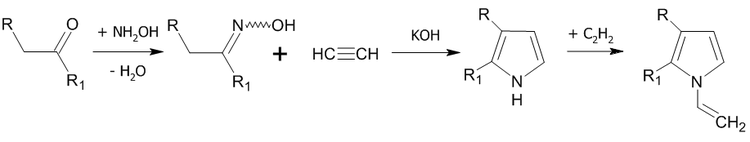
Гетероциклизация протекает при температуре 70—120 °С в среде диметилсульфоксида
.

Образование производных фурана

Образование прочих гетероциклов

Гидрирование алкадиенов
Гидрирование алкадиенов протекает в присутствии металлических катализаторов, при нагревании и под давлением.
При присоединении одной молекулы водорода к дивинилу образуется смесь продуктов (бутен-1 и бутен-2):

Соотношение продуктов 1,2- и 1,4- присоединения зависит от условий реакции.
При комнатной и повышенной температуре основным продуктом реакции является 1,4-продукт (бутен-2).
При полном гидрировании дивинила образуется бутан:

Дегидрирование алканов
При дегидрировании алканов, содержащих от 2 до 4 атомов углерода в молекуле, образуются двойные и тройные связи.
Например
, при дегидрировании этана может образоваться этилен или ацетилен:

При дегидрировании бутана под действием металлических катализаторов образуется смесь продуктов. Преимущественно образуется бутен-2:

Если бутан нагревать в присутствии оксида хрома (III), преимущественно образуется бутадиен-1,3:

III. Изомерия алкинов.
Для алкинов характерна изомерия:
а) СН ≡ С ― СН2
― СН2
― СН3
б) СН ≡С ― СН ― СН3
пентин
– 1 │
3 – метилбутин – 1
Изомерия
положения тройной связи:
а) СН ≡ С ― СН2
― СН2
― СН3
б) СН3
― С ≡ С
―СН 2
—СН3
пентин – 1
пентин – 2
Межклассовая
изомерия с алкадиенами и циклоалканами
Гомологический ряд
C2H2
этинС3Н4
пропинС4Н6
бутинС5Н8
пентинС6Н10
гексинС7Н12
гептинС8Н14
октинС9Н16
нонинС10Н18
декин
Структура тройной связи


На представленной выше диаграмме приведены молекулярные орбитали этилена
и ацетилена
.
//chemege. ru/wp-content/uploads/2019/11/%D1%85%D0%BB%D0%BE%D1%80%D1%8D%D1%82%D0%B0%D0%BD-%D1%81%D0%BE-%D1%81%D0%BF%D0%B8%D1%80%D1%82%D0%BE%D0%B2%D1%8B%D0%BC-%D1%80%D0%B0%D1%81%D1%82%D0%B2%D0%BE%D1%80%D0%BE%D0%BC-%D1%89%D0%B5%D0%BB%D0%BE%D1%87%D0%B8-300×25. jpg 300w» sizes=»(max-width
При отщеплении галогена и водорода от некоторых галогеналканов могут образоваться различные органические продукты. В таком случае выполняется правило Зайцева
.
Правило Зайцева:
отщепление атома водорода при дегидрогалогенировании и дегидратации происходит преимущественно от наименее гидрогенизированного
атома углерода.
Например,
при взаимодействии 2-хлорбутана со спиртовым раствором гидроксида натрия преимущественно образуется бутен-2. Бутен-1 образуется в небольшом количестве (примерно 20%). В реакции мы указываем основной продукт.











![\mbox{CH}_3\!\!-\!\!\mbox{C}\!\!\equiv\!\!\mbox{C}\!\!-\!\!\mbox{Ag}+2\mbox{NaCN}+\mbox{H}_2\mbox{O}\rightarrow\mbox{CH}_3\!\!-\!\!\mbox{C}\!\!\equiv\!\!\mbox{CH}\!\uparrow+\mbox{Na}[\mbox{Ag(CN)}_2]+\mbox{NaOH}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7dc9eb0c6df7c85aa7c6d143aab6dd331a1d4d23)





































![\mbox{RC}\!\!\equiv\!\!\mbox{CR}+2[\mbox{O}]\rightarrow\mbox{R}\!\!-\!\!\mbox{C}(\mbox{O})\!\!-\!\!\mbox{C}(\mbox{O})\!\!-\!\!\mbox{R}](https://wikimedia.org/api/rest_v1/media/math/render/svg/82da449b588c8a5950072f3694cce95d96e34dfd)
![\mbox{HC}\!\!\equiv\!\!\mbox{CH}+4[\mbox{O}]\rightarrow\mbox{HOOC}\!\!-\!\!\mbox{COOH}](https://wikimedia.org/api/rest_v1/media/math/render/svg/70f9a7fe621232ec7d4e63368486bbc4fbeb315e)

![\mbox{RC}\!\!\equiv\!\!\mbox{CR}'+3[\mbox{O}]+\mbox{H}_2\mbox{O}\rightarrow\mbox{RCOOH}+\mbox{R}'\mbox{COOH}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c75b60c32a3fa656ea69e23c377b7d2576a60870)
![\mbox{RC}\!\!\equiv\!\!\mbox{CH}+4[\mbox{O}]\rightarrow\mbox{RCOOH}+\mbox{CO}_2](https://wikimedia.org/api/rest_v1/media/math/render/svg/2f966501384b13d56ca9ba897061144c944bc5c5)


![\mbox{CH}_3\!\!-\!\!\mbox{CH}_2\!\!-\!\!\mbox{C}\!\!\equiv\!\!\mbox{CH}\rightleftarrows[\mbox{CH}_3\!\!-\!\!\mbox{CH}\!\!=\!\!\mbox{C}\!\!=\!\!\mbox{CH}_2]\rightleftarrows\mbox{CH}_3\!\!-\!\!\mbox{C}\!\!\equiv\!\!\mbox{C}\!\!-\!\!\mbox{CH}_3](https://wikimedia.org/api/rest_v1/media/math/render/svg/d57c99f9b1ee32791acd3ed13a85fc0c5e43c8ec)