Природная сера состоит из четырёх стабильных изотопов: 32S (сера-32), 33S (сера-32), 34S (сера-34) и 36 (сера-36).
Получены также искусственные радиоактивные изотопы с массовыми числами от 26 до 49.
Основные сферы использования: научные исследования, медицина, лазерная техника, метрология.
К таблице выпускаемых изотопов
У этого термина существуют и другие значения, см. Сера (значения).
Простое вещество сера — это светло-жёлтый порошкообразный неметалл. В водородных и кислородных соединениях находится в составе различных ионов, образуя многие кислоты и соли. Практически нерастворима в воде. Многие серосодержащие соли малорастворимы в воде.
► К таблице выпускаемых изотопов
По вопросам приобретения обращаться к специалистам отдела продаж:
Тел.: +7 (39169) 9–49–11, 9–49–03, 9–31–73
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 23 декабря 2020 года; проверки требуют 4 правки.
Изотопы серы — разновидности атомов (и ядер) химического элемента серы, имеющие разное содержание нейтронов в ядре.
Природная сера состоит из четырёх стабильных изотопов: 32S (95,02 %), 33S (0,75 %), 34S (4,21 %), 36S (0,02 %). Самым долгоживущим радиоизотопом является 35S с периодом полураспада 87,4 суток.
1. Элемент сера имеет химический знак S, атомный номер Z = 16. Сера расположена в третьем периоде, малом, в VI A-группе, главной. Относительная атомная масса Ar(S) = 32.
2. Строение атома:
а) заряд ядра атома серы +16. В состав ядра атома серы входят 16 протонов. Самый распространённый в природе изотоп — это нуклид 32S. Число нейтронов в ядре этого нуклида равно 32 – 16 = 16;
б) электронная оболочка атомов серы содержит 16 электронов, которые распределены по трем энергетическим уровням; электронная схема: 16S 2e, 8e, 6e; формула электронной конфигурации: 16S 1s22s22p63s23p4; электронно-графическая схема:
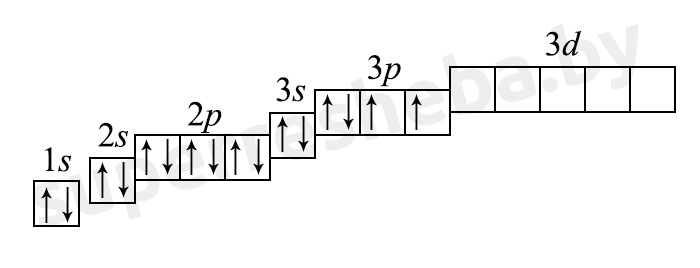
в) конфигурация внешнего электронного слоя: 3s23p4, значит, сера — р-элемент.
3. Степени окисления атомов элемента: высшая +6, так как на внешнем энергетическом уровне атома находится 6 электронов, низшая –2. Электроотрицательность: x(S) = 2.5. megaresheba.ru megareslieba.ru
4. Простое вещество азот является неметаллом, агрегатное состояние при н. у. — твердое, химическая формула S.
5. Формула высшего оксида S+6O3, оксид серы (VI), кислотный; формула гидроксида, соответствующего высшему оксиду, H2S+6O4, гидроксид кислотный, серная кислота; водородное соединение H2S-2, летучее, так как сера является неметаллом.
1. Элемент хлор имеет химический знак Cl, атомный номер Z = 17. Хлор расположен в третьем периоде, малом, в VII A-группе, главной. Относительная атомная масса Ar(Сl) = 35.5.
а) заряд ядра атома хлора +17. В состав ядра атома хлора входят 17 протонов. Самый распространённый в природе изотоп — это нуклид 35Cl. Число нейтронов в ядре этого нуклида равно 35 – 17 = 18.
б) электронная оболочка атомов содержит 17 электронов, которые распределены по трем энергетическим уровням; электронная схема: 17Cl 2e, 8e, 7e; формула электронной конфигурации: 17Cl 1s22s22p63s23p5; электронно-графическая схема:
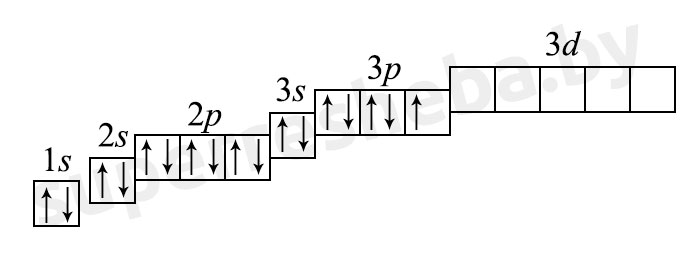
в) конфигурация внешнего электронного слоя: 3s23p5, значит, хлор — р-элемент.
3. Степени окисления атомов элемента: высшая +7, так как на внешнем энергетическом уровне атома находится 7 электронов, низшая –1. Электроотрицательность: х(Сl) = 3.0.
4. Простое вещество хлор является неметаллом, агрегатное состояние при н. у. — газ, химическая формула Cl2.
5. Формула высшего оксида Cl+72O7, оксид серы (VII), кислотный; формула гидроксида, соответствующего высшему оксиду, HCl+7O4, гидроксид кислотный, хлорная кислота; водородное соединение HCl-1, летучее, так как хлор является неметаллом.
1. Элемент алюминий имеет химический знак Al, атомный номер Z = 13. Алюминий расположен в третьем периоде, малом, в III A-группе, главной. Относительная атомная масса Ar(Al) = 27.
а) заряд ядра атома алюминия +13. В состав ядра атома входят 13 протонов. Единственный в природе изотоп — это нуклид 27Al. Число нейтронов в ядре этого нуклида равно 27 – 13 = 14.
б) электронная оболочка атомов содержит 13 электронов, которые распределены по трем энергетическим уровням; электронная схема: 13Al 2e, 8e, 3e; формула электронной конфигурации: 13Al 1s22s22p63s23p1; электронно-графическая схема:
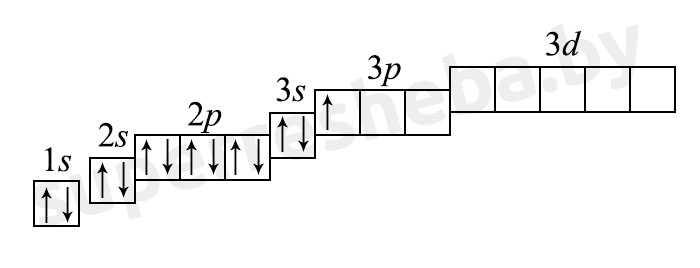
в) конфигурация внешнего электронного слоя: 3s23p1, значит, алюминий — р-элемент.
3. Степени окисления атомов элемента: высшая +3, так как на внешнем энергетическом уровне атома находится 3 электронов, низшая 0. Электроотрицательность: х(Al) = 1.5.
4. Простое вещество алюминий является металлом, агрегатное состояние при н. у. —твердое, химическая формула Al.
5. Формула высшего оксида Al+32O3, оксид алюминия, амфотерный; формула гидроксида, соответствующего высшему оксиду, Al(OH)3, гидроксид алюминия, амфотерный; водородное соединение Al-3H3, нелетучее, так как алюминий является метал.
1. Элемент натрий имеет химический знак Na, атомный номер Z = 11. Натрий расположен в третьем периоде, малом, в I A-группе, главной. Относительная атомная масса Ar(Na) = 23.
а) заряд ядра атома натрия +11. В состав ядра атома входят 11 протонов. Самый распространённый в природе изотоп — это нуклид 23Na. Число нейтронов в ядре этого нуклида равно 23 – 11 = 12.
б) электронная оболочка атомов содержит 11 электронов, которые распределены по трем энергетическим уровням; электронная схема: 11Na 2e, 8e, 1e; формула электронной конфигурации: 11Na 1s22s22p63s1; электронно-графическая схема:
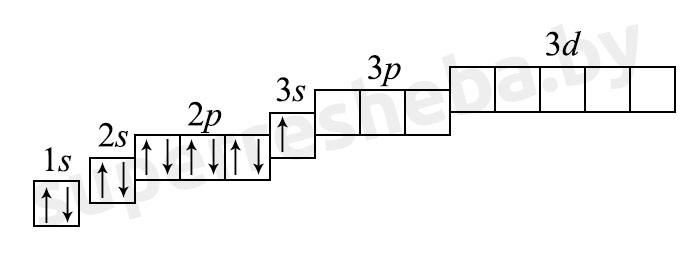
в) конфигурация внешнего электронного слоя: 3s1, значит, натрий — s-элемент.
3. Степени окисления атомов элемента: высшая +1, так как на внешнем энергетическом уровне атома находится 1 электронов, низшая 0. Электроотрицательность: x(Na) = 0.9.
4. Простое вещество натрий является металлом, агрегатное состояние при н. у. — твердое, химическая формула Na.
5. Формула высшего оксида Na+12O, оксид натрия, основный; формула гидроксида, соответствующего высшему оксиду, NaOH, гидроксид натрия, основный (щелочь), водородное соединение Al-3H3 нелетучее, гак как алюминий является металлом.
Распространенность серы и ее изотопов
Кафедра минералогии, кристаллографии и петрографии
Выполнила: студентка гр. М ГП-09 _________________ / Коваленко К. Д./
Проверил: доцент _________________ /Морозов М. В./
Общая информация об изотопах серы
Сера (S) — элемент VI группы периодической системы Менделеева, атомный номер 16, атомная масса 32,06.
Сера — второй по геохимической значимости после О анион, определяющий поведение халько- и сидерофильных металлов. Характерной особенностью геохимии серы является ее способность выступать в нескольких валентных состояниях. В зависимости от условий сера выступает то в качестве окислителя, то восстановителя. Для нее характерны следующие валентные формы: -2; 0; +2; +4; +6. Наиболее распространенными в природе являются первая S2- — в сульфидах, сульфосолях и сероводороде и S6+ — в сульфатах. Элементная (самородная) сера по сравнению с вышеупомянутыми валентными формами имеет значительно меньшее распространение. Весьма малую роль играет ион в соединении SО2 в вулканических эманациях.
Сера является широко распространенным элементом в литосфере, гидросфере и атмосфере Земли. В окисленной форме она встречается в виде сульфатов в океанах и в эвапоритовых породах. Сера обнаруживается в самородном состоянии в кепроке соляных куполов и в породах из некоторых вулканических регионов. Встречаются также восстановленные формы серы в сульфидах полиметаллических месторождений, ассоциирующихся с магматическими, осадочными и метаморфическими породами. Поэтому данные об изотопном составе серы особенно полезны для изучения сульфидных рудных месторождений.
Природная сера состоит из четырех стабильных изотопов: 32S, 33S, 34S и 36S (табл. 1).
Получены также искусственные радиоактивные изотопы 31S (T½ = 2,4 сек), 35S (T½ = 87,1 сут), 37S (Т½= 5,04 мин) и другие.
Распространенность серы и ее изотопов
Приблизительная распространенность изотопов серы: 32S = 95,02%, 33S = 0,75%, 34S = 4,21% и 36S = 0,02% (рис. 1).
Рис. 1. Распространенность стабильных изотопов серы.
Масс-спектрометрические определения обнаружили естественные колебания изотопного состава серы различных природных объектов.
Наиболее часто употребляется отношение 32S/34S в связи с повышенной распространенностью этих изотопов. Изотопный состав серы характеризуется уплотнением:
В качестве стандарта используется сера троилита (FeS) из железного метеорита Canyon Diablo, в котором отношение 32S/34S = 22,2. Этот стандарт удобен, поскольку изотопный состав серы в мафических магматических породах очень близок изотопному составу метеоритов. Следовательно, величина δ34S данного образца земной серы может служить в качестве меры изменений ее изотопного состава, происшедших со времени первоначального поступления серы в земную кору.
Поиск по сайту:
Примерно половина производимой серы используется в производстве серной кислоты.
Серу применяют для вулканизации каучука, как фунгицид в сельском хозяйстве и серу коллоидную как лекарственный препарат. Также сера в составе серобитумных композиций применяется для получения сероасфальта, а в качестве заместителя портландцемента — для получения серобетона. Сера находит применение для производства пиротехнических составов, ранее использовалась в производстве пороха, применяется для производства спичек. Серная лампа — источник белого света, очень близкого к солнечному, с высоким КПД.
Природный сросток кристаллов самородной серы
Сера существенно отличается от кислорода способностью образовывать устойчивые цепочки и циклы из атомов. Наиболее стабильны циклические молекулы S8, имеющие форму короны, образующие ромбическую и моноклинную серу. Это кристаллическая сера — хрупкое вещество жёлтого цвета. Кроме того, возможны молекулы с замкнутыми (S4, S6) цепями и открытыми цепями. Такой состав имеет пластическая сера, вещество коричневого цвета, которая получается при резком охлаждении расплава серы (пластическая сера уже через несколько часов становится хрупкой, приобретает жёлтый цвет и постепенно превращается в ромбическую). Формулу серы чаще всего записывают просто S, так как она, хотя и имеет молекулярную структуру, является смесью простых веществ с разными молекулами. В воде сера нерастворима, но хорошо растворяется в органических растворителях, например, в сероуглероде, скипидаре.
Плавление серы сопровождается заметным увеличением объёма (примерно 15 %). Расплавленная сера представляет собой жёлтую легкоподвижную жидкость, которая выше 160 °C превращается в очень вязкую тёмно-коричневую массу. Наибольшую вязкость расплав серы приобретает при температуре 190 °C; дальнейшее повышение температуры сопровождается уменьшением вязкости и выше 300 °C расплавленная сера снова становится подвижной. Это связано с тем, что при нагревании серы она постепенно полимеризуется, увеличивая длину цепочки с повышением температуры. При нагревании серы свыше 190 °C полимерные звенья начинают рушиться.
Фазовая диаграмма серы
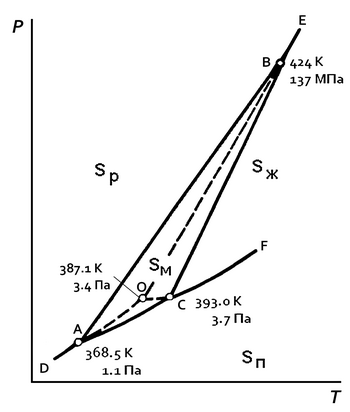
Фазовая диаграмма элементарной серы. Sp — ромбическая сера; Sм — моноклинная сера; Sж — жидкая сера; Sп — пары серы.
Пунктирные линии отражают возможность существования метастабильных фаз, которые наблюдаются при резком изменении температуры:
Сера — хороший окислитель, как и O2, Но более сильные окислители, такие как кислород и галогены, окисляют её.
История и этимология
Точное время открытия серы не установлено, но этот элемент использовался до нашей эры.
Сера использовалась жрецами в составе священных курений при религиозных обрядах. Она считалась произведением сверхчеловеческих существ из мира духов или подземных богов.
Очень давно сера стала применяться в составе различных горючих смесей для военных целей. Уже у Гомера описаны «сернистые испарения», смертельное действие выделений горящей серы. Сера, вероятно, входила в состав «греческого огня», наводившего ужас на противников.
Около VIII века китайцы стали использовать её в пиротехнических смесях, в частности, в смеси типа пороха. Горючесть серы, лёгкость, с которой она соединяется с металлами с образованием сульфидов (например, на поверхности кусков металла), объясняют то, что её считали «принципом горючести» и обязательной составной частью металлических руд.
Пресвитер Теофил (XII век) описывает способ окислительного обжига сульфидной медной руды, известный, вероятно, ещё в древнем Египте.
В период арабской алхимии возникла ртутно-серная теория состава металлов, согласно которой сера почиталась обязательной составной частью (отцом) всех металлов.
В дальнейшем она стала одним из трёх принципов алхимиков, а позднее «принцип горючести» явился основой теории флогистона. Элементарную природу серы установил Лавуазье в своих опытах по сжиганию.
С введением пороха в Европе началось развитие добычи природной серы, а также разработка способа получения её из пиритов; последний был распространён в древней Руси. Впервые в литературе он описан у Агриколы.
Кристаллы серы среди щёток арагонита
Пожароопасные свойства серы
Тонкоизмельчённая сера склонна к химическому самовозгоранию в присутствии влаги, при контакте с окислителями, а также в смеси с углём, жирами, маслами. Сера образует взрывчатые смеси с нитратами, хлоратами и перхлоратами.
Самовозгорается при контакте с хлорной известью.
Обнаружение горения серы пожарной автоматикой является трудной проблемой. Пламя сложно обнаружить человеческим глазом или видеокамерой, спектр голубого пламени лежит в основном в ультрафиолетовом диапазоне. Тепловыделение при пожаре приводит к температуре ниже, чем при пожарах других распространённых пожароопасных веществ. Для обнаружения горения тепловым извещателем необходимо размещать его непосредственно близко к сере. Пламя серы не излучает в инфракрасном диапазоне. Таким образом оно не будет обнаружено распространёнными инфракрасными извещателями. Ими будут обнаруживаться лишь вторичные возгорания. Пламя серы не выделяет паров воды. Таким образом детекторы ультрафиолетовых извещателей пламени, использующие соединения никеля, не будут работать.
Пожары на складах серы
31S (T½ = 2,4 с), 35S (T½ = 87,1 сут), 37S (Т½= 5,04 мин) и другие.
Сера в природе
Самородная сера на вулкане Килауэа
Природные минералы серы
Сера является шестнадцатым по химической распространённости элементом в земной коре. Встречается в свободном (самородном) состоянии и в связанном виде.
Важнейшие природные минералы серы: FeS2 — железный колчедан, или пирит, ZnS — цинковая обманка, или сфалерит (вюрцит), PbS — свинцовый блеск, или галенит, HgS — киноварь, Sb2S3 — антимонит, Cu2S — халькозин, CuS — ковеллин, CuFeS2 — халькопирит. Кроме того, сера присутствует в нефти, природном угле, природных газах и сланцах. Сера — шестой элемент по содержанию в природных водах, встречается в основном в виде сульфат-иона и обусловливает «постоянную» жёсткость пресной воды. Жизненно важный элемент для высших организмов, составная часть многих белков, концентрируется в волосах.
Таблица изотопов серы
В Юникоде есть алхимический символ серы.
В человеке содержится примерно 2 г серы на 1 кг массы тела.
Самородная сера на почтовой марке, 2009
Чистая сера не ядовита, но многие летучие серосодержащие соединения ядовиты (сернистый газ, серный ангидрид, сероводород и др.).
В древности и в средние века серу добывали, вкапывая в землю большой глиняный горшок, на который ставили другой, с отверстием в дне. Последний заполняли породой, содержащей серу, и затем нагревали. Сера плавилась и стекала в нижний горшок.
В настоящее время серу получают главным образом путём выплавки самородной серы непосредственно в местах её залегания под землёй. Серные руды добывают разными способами — в зависимости от условий залегания. Залежам серы почти всегда сопутствуют скопления ядовитых газов — соединений серы. К тому же нельзя забывать о возможности её самовозгорания.
При добыче руды открытым способом экскаваторами снимают пласты пород, под которыми залегает руда. Взрывами рудный пласт дробят, после чего глыбы руды отправляют на сероплавильный завод, где из концентрата извлекают серу.
В 1890 г. Герман Фраш предложил плавить серу под землёй и через скважины, подобные нефтяным, выкачивать её на поверхность. Сравнительно невысокая (113 °C) температура плавления серы подтверждала реальность идеи Фраша. В 1890 г. начались испытания, приведшие к успеху.
Известно несколько методов получения серы из серных руд: пароводяные, фильтрационные, термические, центрифугальные и экстракционные.
Также сера в больших количествах содержится в природном газе в газообразном состоянии (в виде сероводорода, сернистого ангидрида). При добыче она откладывается на стенках труб и оборудования, выводя их из строя. Поэтому её улавливают из газа как можно быстрее после добычи. Полученная химически чистая мелкодисперсная сера является идеальным сырьём для химической и резиновой промышленности.
Серу из природного сернистого газа получают методом Клауса. Для этого используются так называемые серные ямы, где происходит дегазация серы, на выходе получают модифицированную серу — продукт, широко использующийся в производстве асфальта. Технологические установки для получения серы обычно включают в себя ямы недегазированной серы, ямы дегазации, ямы хранения дегазированной серы, а также налив жидкой серы и склад комовой серы. Стены ямы обычно делают из кирпича, дно заливают бетоном, а сверху закрывают яму алюминиевой крышей. Так как сера — это весьма агрессивная среда, ямы периодически приходится полностью реконструировать.
Крупнейшее месторождение самородной серы вулканического происхождения находится на острове Итуруп с запасами категории A+B+C1 — 4227 тыс. тонн и категории C2 — 895 тыс. тонн, что достаточно для строительства предприятия мощностью 200 тыс. тонн гранулированной серы в год.
Склад серы у химического цеха ММСК (1960-е гг.)
— До пятидесятого года стране приходилось импортировать много серы из-за границы. Теперь нужда в импорте серы отпала, — говорил директор завода Александр Адольфович Бурба. — Но завод продолжает расширяться. Начали строить цех производства серной кислоты.
С высокой эстакады застывшим потоком повис ярко-жёлтый массив серы. То, что мы видим в небольших количествах в стеклянных баночках в лабораториях, здесь, на заводском дворе, лежало огромными глыбами.
Комовая сера до начала 1970-х годов была основным видом серы, выпускаемым промышленностью СССР. Её получение технологически просто и осуществляется подачей жидкой серы по обогреваемому трубопроводу на склад, где производится заливка серных блоков. Застывшие блоки высотой 1—3 метра разрушают на более мелкие куски и транспортируют заказчику. Метод, однако, имеет недостатки: невысокое качество серы, потери на пыль и крошку при рыхлении и погрузке, сложность автоматизации.
Жидкую серу хранят в обогреваемых резервуарах и транспортируют в цистернах. Транспорт жидкой серы более выгоден, чем её плавление на месте. Достоинства получения жидкой серы — отсутствие потерь и высокая чистота. Недостатки — опасность возгорания, траты на обогрев цистерн.
Формованная сера бывает чешуйчатая и пластинчатая. Чешуйчатую серу начали производить на НПЗ в 1950-х годах. Для получения используют вращающийся барабан, внутри он охлаждается водой, а снаружи кристаллизуется сера в виде чешуек толщиной 0,5—0,7 мм. В начале 1980-х годов вместо чешуйчатой стали выпускать пластинчатую серу. На движущуюся ленту подаётся расплав серы, который охлаждается по мере движения ленты. На выходе образуется застывший лист серы, который ломают с образованием пластинок. Сегодня эта технология считается устаревшей, хотя около 40 % канадской серы экспортируется именно в таком виде ввиду больших капиталовложений в установки для её получения.
Гранулированную серу получают различными методами.
Крупнейшими производителями молотой серы в России являются предприятия ООО «Каспийгаз» и АО «Сера».
Коллоидная сера — разновидность молотой серы с размером частиц менее 20 мкм. Её применяют в сельском хозяйстве для борьбы с вредителями и в медицине как противовоспалительные и дезинфицирующие средства. Коллоидную серу получают различными способами.
Высокочистую серу получают используя химические, дистилляционные и кристаллизационные методы. Её применяют в электронной технике, при изготовлении оптических приборов, люминофоров (серная лампа), в производстве фармацевтических и косметических препаратов — лосьонов, мазей, средств против кожных болезней.


