3.1. Алканы. Принадлежность к классу определяется наличием углеродных и водородных атомов, отсутствием функциональных групп. В зависимости от соотношения атомов углерода и водорода различают насыщенные и ненасыщенные углеводороды.
Насыщенные углеводороды (Сn H2n+2) отличаются соотношением углерода и водорода и степенью разветвления углеродной цепи. Известно более 70 углеводородов с неразветвленной цепью (гомологов) от СН4 до С70Н142 и множество изомеров. Число изомеров прогрессивно возрастает с увеличением числа углеродных атомов.
Неразветвленные углеводороды, начиная с пятого члена гомологического ряда, называют по названию греческих или латинских (с С8 и далее) числительных с добавлением суффикса «-ан». Первые четыре представителя алканов имеют тривиальные названия, например:
метан этан пропан
бутан пентан Построение названия включает этапы:
1. Выбор самой длинной неразветвленной цепи углеродных атомов (главной цепи).
Если в насыщенном разветвленном углеводороде имеются цепи разной длины, то в качестве основной выбирают цепь:
— имеется наибольшее число боковых ответвлений;
— в которой атомы, несущие боковые цепи, имеют меньшие номера;
— имеется наибольшее число атомов углерода в меньших боковых цепях,
— имеются наименее разветвленные боковые цепи.
Алканы, по радикально-функциональной номенклатуре, считают производными метана, которым является наиболее разветвленный атом углерода (четвертичный; затем третичный; затем вторичный). Радикалы в названии располагают в алфавитном порядке.
Номенклатура алкильных заместителей. Заместители в углеродной цепи разветвленных алканов являются радикалами углеводородов состава C n H 2n+1.
Название одновалентных радикалов (1-8) происходит от названия соответствующего алкана с замещением суффикса «-ан» на «-ил», другие радикалы имеют, как правило, тривиальные названия. Заместители 3 – 4 и 5 — 8 являются изомерами между собой, они отличаются положением cвободной валентности у атома углерода. Так, в соединениях 3, 5, 7 свободная валентность находится у первичного атома углерода, 4,6 – вторичного, 8 – третичного.
*метилтрет. бутилдиэтилметан *изопропилдиэтилметан
*Вт.бутилтрет. бутилметан 2,2,5-триметилгептан
Родовое название углеводородов с одной двойной связью – алкены, одной тройной связью
— алкины; с несколькими двойными или тройными связями – полиены и полиины,
В основе систематического названия алкена лежит название алкана с тем же числом
атомов углерода, родовое окончание алкала «-ан» замещается на родовое окончание
Чтобы назвать алкин, в названии соответствующего алкана «-ан» замещается на
“-ин» (в следствие правил чтения в английском языке идет изменение согласных
декан — децен — децин.
Углеродные атомы в цепи нумеруют таким образом, чтобы положение кратной связи
соответствовало наименьшим возможным номерам. Цифры, указывающие положение
кратной связи, ставят перед названием. Однако, в русской литературе принято
отклонение от этого правила, цифру ставят после названия. Цифра от названия
отделяется дефисом. Примеры;
Если имеется две или большее число кратных связей в молекуле, названия углерода
две двойные связи «адиен» (родовое название «алкадиены»)
три двойные связи «атриен»- (родовое название «алкатриены»)
две тройные связи «адиины» (родовое название «алкадиинны»),
три тройные связи «атриины» и т.д.
Сохраняются следующие несистематические названия: этилен, аллен, дивинил, изопрен,
Если в молекуле ненасыщенного неразветвленного углеводорода имеются как двойные,
так и тройные связи, то атомы углерода нумеруют так, чтобы сумма локантов была
наименьшей. Если возможны несколько вариантов нумерации, то двойная связь
считается «ставшей», то есть ей присваиваются наименьшие номера.
(а не 2-пентен-4-ин, т.к. З+1 < 2+4)
Для названий ненасыщенных разветвленных углеводородов следуют правилам:
— двойные и тройные связи обязательно должны входить в главную цепь, даже если
она не самая длинная.
Пример: в молекуле
главная цепь состоит из 5-ти атомов
углерода, а не из 6-ти;
если в нескольких цепях число атомов углерода одинаково, то выбирают цепь с
максимальным числом кратных связей;
нумерация главной цепи определяется положением не заместителя, а кратной связи.
если нет возможности включить все кратные связи в главную цепь, то
использует названия непредельных радикалов.
Название одновалентных радикалов — производных ненасыщенных ациклических
углеводородов оканчиваются на «энил», «инил», «диенил», и т.д. В случав
необходимости указывают положения двойных и тройных связей. Атом углерода
со свободной валентностью получает номер I.
НС = С – этинил
Н3С – СН = НС – 1- пропил
Н3С – СН = НС – СН2 — 2 – бутенил
Н2С = СН – СН = НС – 1,3 – бутадиенил
НС = С – СН2 — 1 – пропинил
Н3С – С = С – 2- пропил
НС = С – СН = НС – СН2 – 2 – пентил – 4 инил
Сохраняются тривиальные названия одновалентных насыщенных радикалов:
Для двух и трехвалентных ненасыщенных радикалов сохраняются названия:
3.1. Алканы. Принадлежность
к классу определяется наличием углеродных
и водородных атомов, отсутствием
функциональных групп. В зависимости от
соотношения атомов углерода и водорода
различают насыщенные и ненасыщенные
углеводороды.
Насыщенные углеводороды (Сn
H2n+2)
отличаются соотношением углерода и
водорода и степенью разветвления
углеродной цепи. Известно более 70
углеводородов с неразветвленной цепью
(гомологов) от СН4до С70Н142и множество изомеров. Число изомеров
прогрессивно возрастает с увеличением
числа углеродных атомов.
Неразветвленные углеводороды, начиная
с пятого члена гомологического ряда,
называют по названию греческих или
латинских (с С8 и далее) числительных
с добавлением суффикса «-ан». Первые
четыре представителя алканов имеют
тривиальные названия, например:
метан
этан пропан
бутан
пентан
Построение
названия включает этапы:
Если в насыщенном разветвленном
углеводороде имеются цепи разной длины,
то в качестве основной выбирают цепь:
Алканы, по радикально-функциональной
номенклатуре, считают производными
метана, которым является наиболее
разветвленный атом углерода (четвертичный;
затем третичный; затем вторичный).
Радикалы в названии располагают в
алфавитном порядке.
Номенклатура алкильных заместителей.
Заместители в углеродной цепи
разветвленных алканов являются радикалами
углеводородов составаCn H2n+1.
Название одновалентных радикалов ( 1-8
) происходит от названия соответствующего
алкана с замещением суффикса «-ан» на
«-ил», другие радикалы имеют, как правило,
тривиальные названия. Заместители 3 –
4 и 5 — 8 являются изомерами между собой,
они отличаются положением cвободной
валентности у атома углерода. Так, в
соединениях 3, 5, 7 свободная валентность
находится у первичного атома углерода,
4,6 – вторичного, 8 – третичного.
3. Пропил
6. Вт. бутил
8 . Трет. бутил
9. Метилен
10. Винил
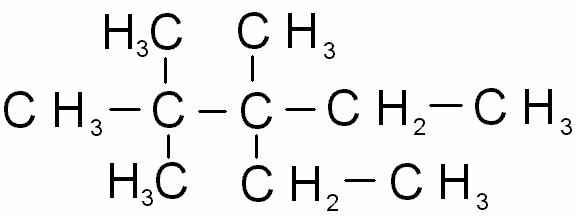
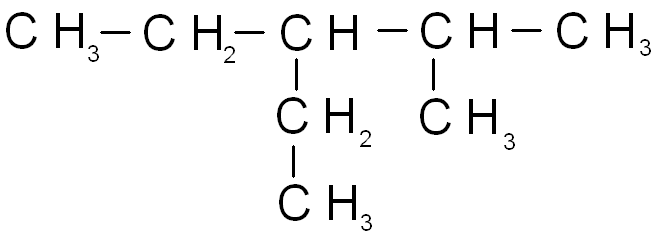
)
2)
2,2,3-триметил-3-этилпентан,
2-метил-3-этилпентан,
*метилтрет. бутилдиэтилметан
*изопропилдиэтилметан
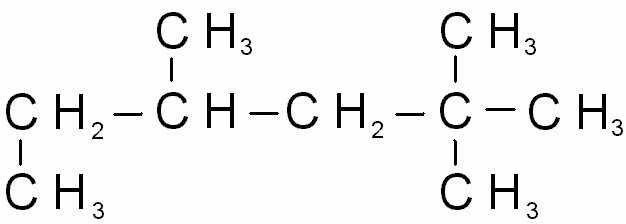
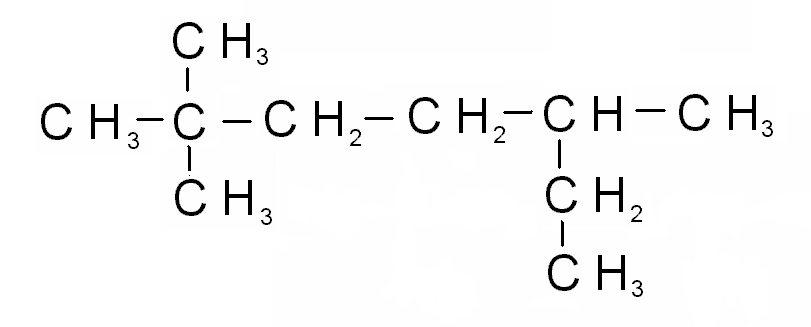
3)
4)
*Вт.бутилтрет. бутилметан
2,2,5-триметилгептан
1. Назовите следующие соединения:

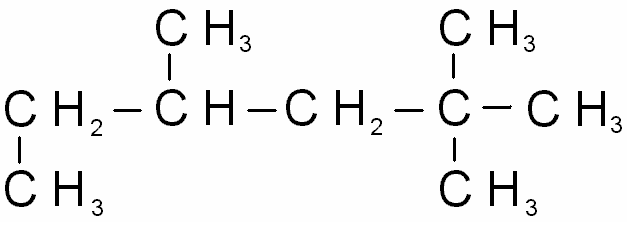
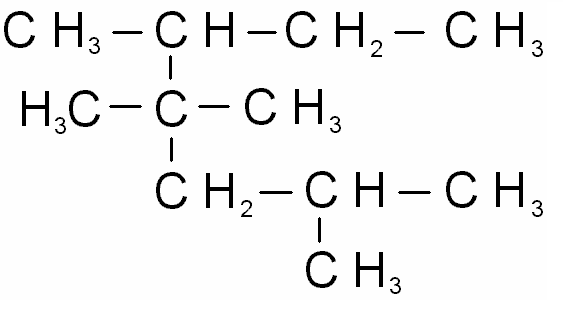
2. Напишите структурные формулы соединений,
назовите по другой номенклатуре:
3.2. Алкены. Ненасыщенные ациклические
углеводороды (Сn
H2n),
имеющие одну двойную связь, получают
название путем замены суффикса «-ан»
в наименовании соответствующего
насыщенного углеводорода на «-ен». Если
имеется две или большее число двойных
связей, название будет оканчиваться
суффиксами «-адиен », «-атриен » и т.д.
Названия таких углеводородов соответственно
будут «алкены», «алкадиены», «алкатриены»
и т.д. Углеродные атомы в цепи нумеруются
так, чтобы положение двойной связи
соответствовало наименьшему номеру.
Сохраняется несистематическое название
«этилен» для этена, «аллен» для
пропадиена-1,2.
Название ненасыщенных ациклических
соединений включает этапы:
Алкены по радикально-функциональнлй
номенклатуре ( * ) считают производными
этилена. В соединениях 2 и 3 понятие
симметрии ( сокращенный вариант «сим-»
«несим-» ) относится к положению
заместителей по отношению к-связи.
В соединениях 6 и 7 приведены тривиальные
названия(** ).
)
2)
3)
бутен-1, *этилэтилен
бутен-2 ,
2-метилпропен-1,
*сим.- диметилэтилен*несим.- диметилэтилен
4)
5)
6)
пропадиен -1,2, *аллен
бутадиен-1,2,*метилаллен
бутадиен-1,3,**дивинил
7) 8)
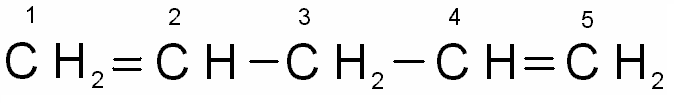
2-метилбутадиен-1,3, **изопрен
пентадиен-1,4
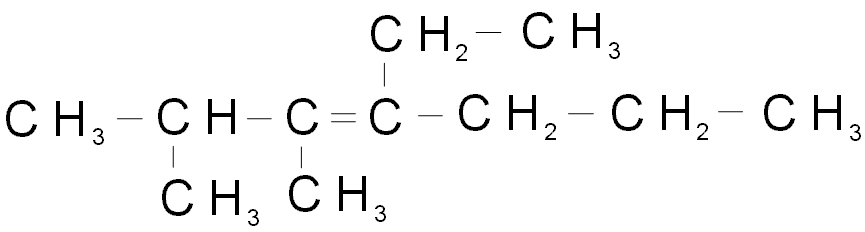

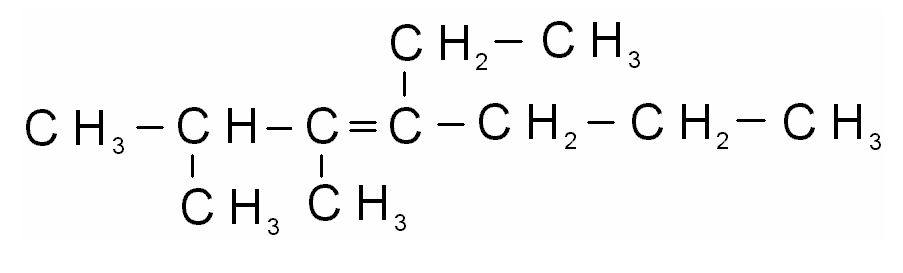
)
2)
3) 4)
5)
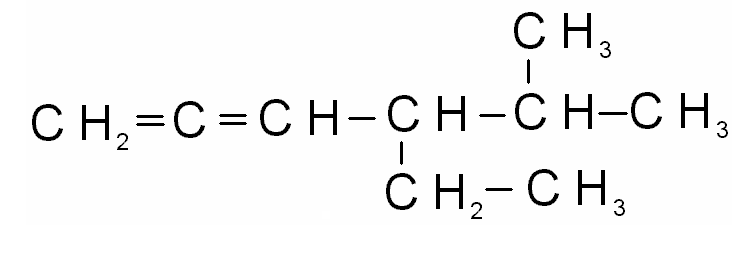
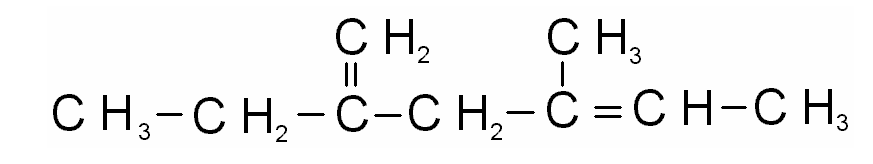
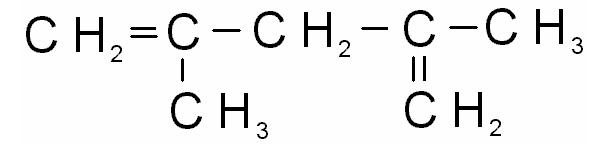
3.3. Алкины. Ациклические углеводороды,
имеющие одну тройную связь, получают
название путем замены суффикса «-ан»
на «-ин» (Сn H2n-2).
Если имеется две или большее число
тройных связей, название будет оканчиваться
суффиксами «-адиин», «-атриин» и т.д.
Названия таких углеводородов соответственно
будут «алкины», «алкадиины», «алкатриины»
и т.д. Углеродные атомы в цепи нумеруются
так, чтобы положение тройной связи
соответствовало наименьшему номеру.
Сохраняется несистематическое название
«ацетилен» для этина.
Название алкинов включает те же этапы,
что название алкенов, нумерацию цепи
определяет тройная связь. В углеводородах,
имеющих как двойные, так и тройные связи
старшей при определении нумерации цепи
считают двойную связь, она должна иметь
наименьший локант. В названии первым
указывается суффикс двойной связи, а
затем — тройной.
По радикально-функциональной
номенклатуре, алкины считают производными
ацетилена.
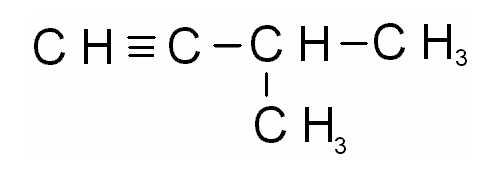
)
2)
3)
этин, *ацетилен пропин,*метилацетилен 3-метилбутин-1,*изопропилацетилен
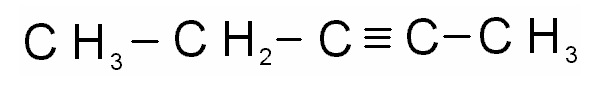
пентин-2 , *метилэтилацетилен
бутен-1-ин-3,*винилацетилен
1) 2) 3)
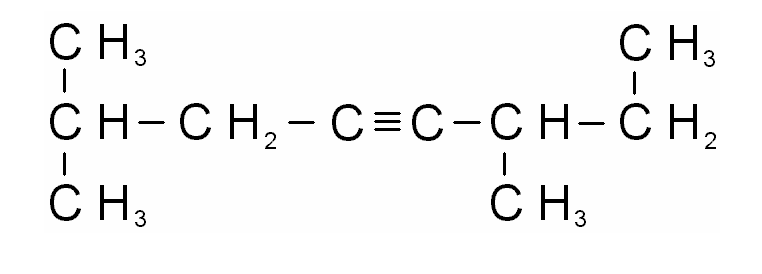
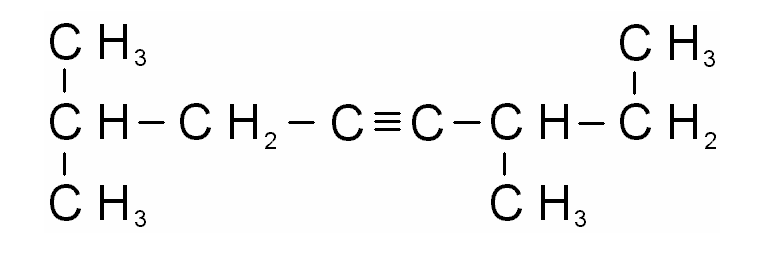
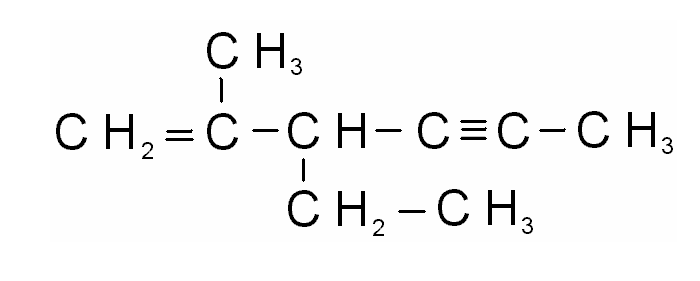
Воснову научной классификации и номенклатуры органических соединений положены принципы теории химического строения А. М. Бутлерова.
Все органические соединения подразделяют на следующие основные ряды:
I. Ациклические соединения — с открытой цепью углеродных атомов (их называют также алифатическими соединениями, или соединениями жирного ряда):
1. Предельные (насыщенные).
2. Непредельные (ненасыщенные).
II. Циклические соединения — с замкнутой в кольцо цепью атомов.
1. Карбоциклические (изоциклические), — в кольцевую систему которых входят только углеродные атомы:
а) алициклические (предельные и непредельные), б) ароматические.
2. Гетероциклические соединения — в их кольцевую систему, кроме углеродных атомов, входят атомы других элементов — гетероатомы (кислород, азот, сера и т. д.).
В рядах ациклических икарбоциклических соединений основными классами являются углеводороды.
В основе гетероциклических соединений лежат гетероциклы, в которых атомы, образующие кольцо, соединены только с атомами водорода.
В предельных (насыщенных) углеводородах атомы углерода соединены друг с другом простыми (ординарными) связями С—С. В непредельных (ненасыщенных) углеводородах имеются одна или несколько пар углеродных атомов, соединенных кратными — двойными С = С или тройными С ≡ С связями.
Углеводороды с двойными или тройными связями могут быть образованы путем отнятия 2, 4, 6 и более атомов водорода от пар смежных углеродных атомов в предельных углеводородах; при этом получаются непредельные углеводороды, содержащие соответственно двойную, тройную, две двойные ит. д. связи. При отнятии же двух и более атомов водорода от несмежных углеродных атомов из предельных ациклических углеводородов могут быть получены циклические углеводороды.
Таким образом, все другие углеводороды можно рассматривать как производные предельных ациклических углеводородов.
Несколько кратных связей могут иметь различное взаимное расположение в углеродной цепи. Например, различают кумулированные С = С = С, сопряженные (или конъюгированные) С = С—С = С и изолированные (или уединенные)С = С—(СН2) п —С = С двойные связи.
Углеводороды различных классов образуют так называемые гомологические ряды, в которых каждый последующий углеводород отличается от предыдущего члена ряда на гомологическую разность СН2. Состав любого члена гомологического ряда выражается общей для данного ряда эмпирической формулой. Например, состав ациклических предельных углеводородов может быть представлен формулой С n Н2 n +2, непредельных — с одной двойной связью C n H2 n , — с одной тройной или с двумя двойными связями С n Н2 n – 2 и т. д. Например:
Названия гомологических рядов углеводородов иногда производят от названий их простейших членов, например: углеводороды ряда метана, углеводороды ряда этилена (этиленовые углеводороды), углеводороды ряда ацетилена (ацетиленовые углеводороды).
При замещении в углеводородах того или иного гомологического ряда одного или нескольких атомов водорода отдельными атомами или группами (например, галогенами, группами —NO2, —ОН, —NH2 и т. д.) образуются гомологические ряды, соответственно, галогенпроизводных, нитросоединений, спиртов, аминов и т. д. Таким образом, все другие классы органических соединений того или иного ряда являются производными углеводородов.
Для наименования отдельных органических соединений широкое распространение получили тривиальные названия, рациональная, Женевская (1892 г.) и Льежская (1930 г.) номенклатуры. Среди них наиболее строгой с точки зрения единого принципа наименования органических соединений и однозначности их названий (особенно для ациклических соединений) является Женевская номенклатура. К сожалению, она в свое время не была разработана полностью и не может быть использована как единственная при наименовании очень многих сложных органических соединений.
В 1947 г. на совещании Международного союза чистой и прикладной химии (International Union of Pure and Applied Chemistry — сокращенно IUPAC), состоявшемся в Лондоне, было принято решение о пересмотре существовавших правил номенклатуры органических соединений и о выработке новых международных правил. Созданная комиссия выработала правила, которые в 1957 г. были опубликованы под названием Правила номенклатуры органических соединений IUPAC 1957.
В СССР А. П. Терентьевым с сотрудниками (1951 г.) была предложена систематическая номенклатура,основанная на строгом едином принципе и позволяющая однозначно называть любое органическое соединение. Однако эта номенклатура, вследствие довольно значительного отличия от обычных привычных химикам названий, не является общепринятой.
Ниже дана краткая характеристика различных номенклатурных систем.
Тривиальные названия не вытекают из каких-либо единых систематических принципов номенклатуры; они не выражают строения соединения и обычно отражают историю, происхождение веществ, выделение их из природных продуктов, путь синтеза и т. п. (например, рудничный газ, муравьиная кислота, винный спирт, бензол, ванилин, стрептоцид). Многие соединения названы по имени ученого, открывшего их (кетон Михлера, углеводород Чичибабина и т. п.). Однако и некоторые тривиальные названия приведены в известную систему. Так, в ряду метана все названия углеводородов, начиная от C5, являются систематическими — корни их производятся от греческих числительных, и все они имеют общее окончание -ан (пентан, гексан, гептан) и т. д.; названия же первых четырех представителей этого ряда (метан, этан, пропан, бутан) — тривиальные, так как корни их не образованы по какой-либо системе, однако и эти названия имеют общее для ряда метана окончание -ан. Такие названия по номенклатуре IUPAC обозначаются как полутривиальные или полусистематические (semi-trivial и semi-sistematic).
Рациональная и другие упомянутые номенклатуры построены на принципах научной систематики органических соединений: название соединения должно отражать его химическое строение.
По рациональной номенклатуре за основу наименования органического соединения обычно принимают название наиболее простого (чаще всего первого) члена данного гомологического ряда. Все остальные соединения рассматривают как производные этого простейшего гомолога, образованные замещением в нем атомов водорода углеводородными или иными радикалами, атомами или атомными группами.
По Женевской номенклатуре основой (корнем) названия органического соединения является название нормального углеводорода, содержащего то же число атомов углерода, что и наиболее длинная углеродная цепь в называемом соединении. Приставки (префиксы) и окончания (суффиксы) показывают наличие в этой главной цепи боковых цепей (углеводородных радикалов), функциональных групп, нефункциональных заместителей и кратных связей; при этом цифрами обозначают положение боковых цепей, групп или кратных связей в главной углеродной цепи, а греческими (иногда латинскими) числительными — число одинаковых замещающих групп или кратных связей.
Порядок перечисления в общем женевском названии соединения названий и обозначений всех этих групп и кратных связей определяется их условным старшинством по отношению друг к другу. Названия углеводородных радикалов помещают перед корнем слова (т. е. перед названием главной цепи), а обозначения кратных связей — после корня.
К нефункциональным заместителям относят галогены, нитрозо-(—NO), нитро-(—NO2), азидо-(—N3) группы; они не содержат атомов водорода; их обозначения в женевском названии помещают перед названиями азотсодержащих функциональных групп или перед названиями радикалов, а если эти последние отсутствуют — перед корнем слова.
В общем названии соединения вначале указываются младшие, затем старшие группы.
Нумерация углеродных атомов в главной цепи соединения определяется также условным старшинством замещающих групп или кратных связей и их расположением по отношению к одному или другому концу этой цепи. При этом углеводородные радикалы являются старшими по отношению к кратным связям и к другим заместителям (при одинаковом положении двух радикалов по отношению к концам главной цепи старшим является радикал с меньшим числом углеродных атомов). Таким образом, в продуктах замещения углеводородов сохраняется нумерация, принятая для углеводородов.
Ниже приведена схема построения женевского названия сложного органического соединения ациклического ряда, предложенная А. П. Терентьевым (1951 г.).
1. Цифры II—VI обозначают уменьшение старшинства групп при определении начала нумерации цепи. Например, если есть углеводородные радикалы (II) и кратные связи (III) — начало нумерации цепи определяется более старшими группами — радикалами; кислородсодержащие группы (IV) старше азотсодержащих групп (V) и т. д.
2. Внутри разделов, обозначенных цифрами II—VI, начало нумерации определяется любой группой данного раздела, стоящей ближе к концу цепи. Если же группы данного раздела расположены симметрично, т. е. на равных расстояниях от концов цепи, начало нумерации определяет старшая группа. Возрастание старшинства в каждом разделе указано стрелками. Например, при симметричном расположении спиртовой и кетонной групп начало нумерации определяет старшая — кетонная группа.
3. В разделе IV каждая серусодержащая группа старше соответствующей кислородсодержащей группы.
По Льежской номенклатуре за основу названия, так же как и по Женевской номенклатуре, принимается самая длинная углеродная цепь, но допускаются и отклонения от этого правила: если боковые радикалы в этой самой длинной цепи оказываются сложными, за основу названия может быть выбрана и более короткая цепь так, чтобы боковые радикалы оказались более простыми.
Главная углеродная цепь, согласно Льежской номенклатуре, должна включать функциональную группу, даже если эта цепь и не является самой длинной; если функциональных групп несколько, главную цепь выбирают так, чтобы вней оказалось наибольшее число функциональных групп. Аналогично в главную цепь включаются и кратные связи. В то же время карбоксильную группу по Льежской номенклатуре иногда рассматривают как замещающую функциональную группу, тогда как по Женевской номенклатуре углерод карбоксильной группы должен быть включен в счет атомов углерода цепи. Начало нумерации определяет прежде всего функциональная группа, затем двойные и тройные связи и в последнюю очередь атомы и радикалы, обозначаемые приставками (отличие от Женевской номенклатуры). При наличии нескольких функциональных групп начало нумерации определяет главная функция (например, в оксиальдегидах — альдегидная группа; в оксикислотах — карбоксильная группа).
Номенклатура IUPAC 1957. Новые правила, разработанные комиссией IUPAC по номенклатуре органических соединений в период с 1947 по 1957 гг., состоят из разделов: А. Номенклатура углеводородов (ациклических, циклических, терпенов); В. Номенклатура основных гетероциклических систем.
Правила IUPAC 1957 являются развитием и упорядочением в основном Льежской номенклатуры.
За основу ациклических соединений принимается обязательно самая длинная углеродная цепь, но при этом подробно разработана номенклатура боковых цепей — нормальных и разветвленных — и установлено старшинство радикалов при перечислении их в названии и при определении порядка нумерации атомов главной цепи или цикла. Официально введены наиболее употребительные тривиальные и полутривиальные названия многих соединений, принимаемых за основу, а также радикалов.
В 1963 г. опубликован предварительный текст продолжения правил IUPAC, раздел С, в который входит номенклатура соединений, содержащих функциональные группы, и номенклатура функциональных производных. Правила регламентируют выбор главной функции и предлагают ряд способов наименования для каждого типа соединений. См. International Union of Pure and Applied Chemistry. Tentative Rules for Nomenclature of Organic Chemistry, Section C. London Butterworths Scientific Publications, 1963.
Ниже приведены официальные тексты правил Женевской и Льежской номенклатур, а также правил IUPAC 1957.
Предварительно даны используемые в различных номенклатурных системах названия важнейших радикалов и атомных групп, сокращения, приставки и окончания, а также греческие (и некоторые латинские) числительные и буквы греческого алфавита.
Приведены некоторые дополнительные сведения о способах наименования органических соединений различных классов, которые используются впрактике наряду с правилами указанных выше номенклатур, а также сведения о названиях по старой рациональной номенклатуре.
Основы классификации и номенклатуры органических соединений
В основу научной классификации и номенклатуры органических соединений положены принципы теории химического строения А. М. Бутлерова.
Все органические соединения подразделяют на следующие основные ряды:
I. Ациклические соединения — с открытой цепью углеродных атомов (их называют также алифатическими соединениями, или соединениями жирного ряда):
1. Предельные (насыщенные).
2. Непредельные (ненасыщенные).
II. Циклические соединения — с замкнутой в кольцо цепью атомов.
1. Карбоциклические (изоциклические),— в кольцевую систему которых входят только углеродные атомы:
а) алициклические (предельные и непредельные), б) ароматические.
2. Гетероциклические соединения — в их кольцевую систему, кроме углеродных атомов, входят атомы других элементов — гетероатомы (кислород, азот, сера и т. д.).
В рядах ациклических и карбоциклических соединений основными классами являются углеводороды.
В предельных (насыщенных) углеводородах атомы углерода соединены друг с другом простыми (ординарными) связями С—С. В непредельных (ненасыщенных) углеводородах имеются одна или несколько пар углеродных атомов, соединенных кратными — двойными С = С или тройными С ≡ С связями.
Углеводороды с двойными или тройными связями могут быть образованы путем отнятия 2, 4, 6 и более атомов водорода от пар смежных углеродных атомов в предельных углеводородах; при этом получаются непредельные углеводороды, содержащие соответственно двойную, тройную, две двойные и т. д. связи. При отнятии же двух и более атомов водорода от несмежных углеродных атомов из предельных ациклических углеводородов могут быть получены циклические углеводороды.
Несколько кратных связей могут иметь различное взаимное расположение в углеродной цепи. Например, различают кумулированные С = С = С, сопряженные (или конъюгированные) С = С—С = С и изолированные (или уединенные) С = С—(СН2)п—С = С двойные связи.
Углеводороды различных классов образуют так называемые гомологические ряды, в которых каждый последующий углеводород отличается от предыдущего члена ряда на гомологическую разность СН2. Состав любого члена гомологического ряда выражается общей для данного ряда эмпирической формулой. Например, состав ациклических предельных углеводородов может быть представлен формулой СnН2n+2, непредельных — с одной двойной связью CnH2n, — с одной тройной или с двумя двойными связями СnН2n – 2 и т. д. Например:
В СССР А. П. Терентьевым с сотрудниками (1951 г.) была предложена систематическая номенклатура, основанная на строгом едином принципе и позволяющая однозначно называть любое органическое соединение. Однако эта номенклатура, вследствие довольно значительного отличия от обычных привычных химикам названий, не является общепринятой.
Ниже дана краткая характеристика различных номенклатурных систем.
Тривиальные названия не вытекают из каких-либо единых систематических принципов номенклатуры; они не выражают строения соединения и обычно отражают историю, происхождение веществ, выделение их из природных продуктов, путь синтеза и т. п. (например, рудничный газ, муравьиная кислота, винный спирт, бензол, ванилин, стрептоцид). Многие соединения названы по имени ученого, открывшего их (кетон Михлера, углеводород Чичибабина и т. п.). Однако и некоторые тривиальные названия приведены в известную систему. Так, в ряду метана все названия углеводородов, начиная от C5, являются систематическими — корни их производятся от греческих числительных, и все они имеют общее окончание -ан (пентан, гексан, гептан) и т. д.; названия же первых четырех представителей этого ряда (метан, этан, пропан, бутан) — тривиальные, так как корни их не образованы по какой-либо системе, однако и эти названия имеют общее для ряда метана окончание -ан. Такие названия по номенклатуре IUPAC обозначаются как полутривиальные или полусистематические (semi-trivial и semi-sistematic).
1. Цифры II—VI обозначают уменьшение старшинства групп при определении начала нумерации цепи. Например, если есть углеводородные радикалы (II) и кратные связи (III) — начало нумерации цепи определяется более старшими группами — радикалами; кислородсодержащие группы (IV) старше азотсодержащих групп (V) и т. д.
2. Внутри разделов, обозначенных цифрами II—VI, начало нумерации определяется любой группой данного раздела, стоящей ближе к концу цепи. Если же группы данного раздела расположены симметрично, т. е. на равных расстояниях от концов цепи, начало нумерации определяет старшая группа. Возрастание старшинства в каждом разделе указано стрелками. Например, при симметричном расположении спиртовой и кетонной групп начало нумерации определяет старшая — кетонная группа.
3. В разделе IV каждая серусодержащая группа старше соответствующей кислородсодержащей группы.
Главная углеродная цепь, согласно Льежской номенклатуре, должна включать функциональную группу, даже если эта цепь и не является самой длинной; если функциональных групп несколько, главную цепь выбирают так, чтобы в ней оказалось наибольшее число функциональных групп. Аналогично в главную цепь включаются и кратные связи. В то же время карбоксильную группу по Льежской номенклатуре иногда рассматривают как замещающую функциональную группу, тогда как по Женевской номенклатуре углерод карбоксильной группы должен быть включен в счет атомов углерода цепи. Начало нумерации определяет прежде всего функциональная группа, затем двойные и тройные связи и в последнюю очередь атомы и радикалы, обозначаемые приставками (отличие от Женевской номенклатуры). При наличии нескольких функциональных групп начало нумерации определяет главная функция (например, в оксиальдегидах — альдегидная группа; в оксикислотах — карбоксильная группа).
Номенклатура IUPAC 1957. Новые правила, разработанные комиссией IUPAC по номенклатуре органических соединений в период с 1947 по 1957 гг., состоят из разделов: А. Номенклатура углеводородов (ациклических, циклических, терпенов); В. Номенклатура основных гетероциклических систем.
За основу ациклических соединений принимается обязательно самая длинная углеродная цепь, но при этом подробно разработана номенклатура боковых цепей — нормальных и разветвленных — и установлено старшинство радикалов при перечислении их в названии и при определении порядка нумерации атомов главной цепи или цикла. Официально введены наиболее употребительные тривиальные и полутривиальные названия многих соединений, принимаемых за основу, а также радикалов.
В 1963 г. опубликован предварительный текст продолжения правил IUPAC, раздел С, в который входит номенклатура соединений, содержащих функциональные группы, и номенклатура функциональных производных. Правила регламентируют выбор главной функции и предлагают ряд способов наименования для каждого типа соединений. См. International Union of Pure and Applied Chemistry. Tentative Rules for Nomenclature of Organic Chemistry, Section C. London Butterworths Scientific Publications, 1963.
Ниже приведены официальные тексты правил Женевской и Льежской номенклатур, а также правил IUPAC 1957.
Приведены некоторые дополнительные сведения о способах наименования органических соединений различных классов, которые используются в практике наряду с правилами указанных выше номенклатур, а также сведения о названиях по старой рациональной номенклатуре.
Тривиальные и систематические названия некоторых радикалов и атомных групп по различным номенклатурным системам
Номенклатура
В настоящее время в органической химии
используется систематическая, рациональная
и тривиальная номенклатура.
Тривиальная (эмпирическая)
номенклатура – это исторически
появившиеся названия, не отражающие
строение вещества, – пропан, ацетон,
уксусная кислота и т.д.
Рациональная номенклатура
рассматривает все предельные углеводороды
как производные метана: СН3–СН(СН3)–СН2–СН3–диметилэтилметан.
По международной заместительной
номенклатуре за основу выбирают самую
длинную и наиболее разветвленную цепь
углеродных атомов. Нумерацию атомов
углерода в цепи начинают с того конца,
к которому ближе находится двойная
(тройная) связь или какой-либо заместитель.
Положение заместителя указывают цифрой
по номеру атома углерода, при котором
он находится, потом называют заместитель,
а затем основу. Основу называют
производными словами от числительных,
указывающих число атомов углерода в
цепи. Если в цепи есть кратная связь или
функциональные группы, то их наличие
указывают суффиксом, а положение в цепи
цифрой, которую ставят перед названием
основы. Начало нумерации цепи определяется
старшинством функциональных групп:

(В порядке падения старшинства)
Примечание: *— (***) —
обозначается корень в названии (основная
цепь углеродных атомов);**— в
отечественной литературе окончание «
-о » в случае галогенов обычно опускается.
При необходимости в название включают
умножающие префиксы и локанты. При
наличии 2-х или более заместителей
различной природы они перечисляются в
алфавитном порядке, который
устанавливается следующим образом:
Цифры – локанты ставят перед префиксомипосле суффиксов, отделяя их от
букв дефисами. В английском и других
иностранных языках используется иной
порядок расстановки локантов.
Правила радикально – функциональной
номенклатуры. В названии соединений
по радикально – функциональной
номенклатуре используются, в общем, те
же приемы, что и в заместительной
номенклатуре, с той лишь разницей, что
никогда не используются суффиксы. Вместо
этого одним словом обозначают название
функционального класса (таблица 2.2), а
остальную часть названия — соответствующими
радикалами, которые обозначают в названии
первыми валфавитномпорядке.
Например,триметилметан,метилэтилкетон,ацетилхлорид. Если соединение
включает более одного типа функциональных
групп, то за название функционального
класса принимают группу, которая
расположена выше других в табл.2.2, все
прочие группы обозначаются префиксами,
например, гидроксиметиленметилкетон,
2-гидроксиэтилметилкетон. В
некоторых случаях к названию радикала
присоединяется соответствующее окончание
«-овый», «-овая», например, метиловый
спирт.
Таблица 2.2. Названия функциональных
классов в радикально-функциональной
номенклатуре (в
порядке падения старшинства)
Примеры построения названий соединений
по некоторым другим номенклатурам:
— по аддитивнойноменклатуре
(номенклатура присоединения) к названию
основной части молекулы добавляют
названия присоединенных к ней атомов,
например, 1,2,3,4 -тетрагидронафталин
;
— субстрактивнаяноменклатура
указывает наудаление отдельных
атомов или групп, которые обозначаются
субстрактивными префиксами в имеющихся
систематических или тривиальных
названиях, например, 6,7 –дигидроциклопентанпергидрофенантрен
;
— конъюнктивная(объединительная)
номенклатура применяется в тех случаях,
когда старшая группа связана с ациклическим
компонентом, который в свою очередь
непосредственно соединен углерод-углеродной
связью с циклическим компонентом.
Углеродные атомы боковой цепи, которая
ограничена старшей группой, обозначают
греческими буквами, начиная от старшей
группы по направлению к циклическому
компоненту. Все другие звенья цепи
рассматриваются как заместители и
обозначаются префиксами перед названием
циклического компонента, например, α,
ß-диметил-2-нафталинэтанол  .
.
1) 2)
3)



Углеводороды
Угеводороды – простейшие
органические соединения, молекулы
которых построены только из атомов
углерода и водорода.
Ациклические углеводороды
Алканы (парафины, предельные
или насыщенные углеводороды)CnH2n+2– это углеводороды, у которых атомы
углерода связаны между собой простой
(одинарной) связью.
СН3–СН2–СН2–СН2–СН2–СН3
(С6Н14) гексан и т.д.
Каждый последующий член гомологического
ряда отличается от предыдущего на
гомологическую разность (СН2).
Молекула алкана, потеряв водород,
превращается в радикал: •СН3– метил,•С3Н7– пропил
и т. д.; отсюда даются соответствующие
названия соединениям: СН3–СН2–NH2– этиламин;CH3I–йодистый метил; СН3–О–СН3– диметиловый эфир и пр.
Физические свойства:метан, этан,
пропан и бутан – бесцветные газы без
запаха или со слабым запахом бензина.
Углеводороды от пентана до пентадекана
– жидкости; высшие углеводороды (C15H32)
при обычных температурах – твёрдые
вещества.
Химические свойстваалканов
определяются высокой прочностью
ковалентных связей (σ-связей), поэтому
химическая активность предельных
углеводородов мала. Алканы могут вступать
в реакции только в жёстких условиях:
при повышенной температуре, облучении,
действии активных реагентов, использовании
катализаторов. Для предельных углеводородов
характерны следующие типы реакций:
а) Реакции замещения, когда атомы
водорода замещаются на другие атомы
или группы атомов. Типичной реакцией,
протекающей по радикальному механизму
замещения, является реакция галогенирования,
идущая при облучении светом:


б) Реакция термического расщепления
С–С – связей (крекинг). Обычно идет с
образованием алканов и алкенов через
свободные радикалы:
в) Реакция окисления. Может происходить
в жестких условиях, т.е. при горении:
2СН3–СН3+ 7О2
4СО2+ 6Н2О, но при наличии
катализаторов могут образовываться
карбоновые кислоты:
октадекан стеариновая
кислота
Предельные углеводороды используются
для синтеза этилена, пропилена, ацетилена,
бензола, толуола, ксилолов, нафталина
и т.д. Путём крекинга нефти, а затем
ректификации полученных продуктов по
фракциям вырабатывают такие нефтепродукты,
как моторное топливо, растворители,
смазочные масла, вазелин, гудрон и др.
Алканы входят в состав природных газов,
обычно это смеси метана (основное
количество), этана (от 2–5%), пропана и
других более тяжёлых углеводородов.
Некоторые примеры использования метана:
СН4+ О2100
атм. СН3ОН метиловый спирт;
Н4+ О2 10 атм.
СС14+ НС1 и другие хлоруглеводороды.
Алкены (олефины, непредельные,
этиленовые углеводороды) –это
углеводороды, в структуре углеродного
скелета которых имеется двойная (σ и π)
связь. Их молекулярная формула СnН2n.
По физическим свойствам алкены мало
отличаются от алканов. Низшие гомологи
С2– С4– газы; С5–
С17– жидкости; высшие гомологи –
твёрдые вещества. В воде алкены
нерастворимы, хорошо растворимы в
органических растворителях.
СН2=СН2этен (этилен), его
радикал СН2=СН•– винил;
Для алкенов характерна изомерия:
а) структурная (изомерия углеродного
скелета, изомерия положения двойной
связи);
б) пространственная (цис-, трансизомерия).
Химические свойства определяются
наличием двойной связи в этиленовых
углеводородах – это реакции электрофильного
присоединения, окисления и полимеризации,
сопровождающиеся разрывом π-связи.
Примеры реакций присоединения:
а) Реакция гидробромирования:
пропен 2-бромпропан
Реакции с галогеноводородами идут по
правилу Марковникова, т.е. водород
присоединяется к более гидрированному
атому углерода в несимметричных алкенах.
б) Реакция гидрирования:
этилен этан
в) Реакция галогенирования:
г) Реакция гидратации:
присоединение по правилу Марковникова
д) Реакции окисления:
полное окисление (горение)
окисление в мягких условиях
Это качественная реакция на двойную
связь.
е) Реакции полимеризации:
пропилен полипропилен
Алкины (ацетиленовые
углеводороды) СnH2n-2– это ненасыщенные углеводороды, которые
имеют одну тройную связь.
Структурная изомерия алкинов, как и
алкенов, обусловлена строением углеродной
цепи и положением в ней тройной связи.
Физические свойства. Ацетилен,
метил- и этилацетилены – газы; следующие
гомологи ацетилена (от С5до С15)
– жидкости; высшие ацетиленовые
углеводороды (от С15Н28) –
твердые вещества.
Химические свойства алкинов
определяются наличием тройной связи.
1. Реакции присоединения:
а) Гидрирование (гидрогенизация):
пропин пропен
пропан
б) Присоединение галогеноводородных
кислот согласно правилу Марковникова:
пропин 2-хлорпропен
2,2-дихлорпропан
г) Гидратация (реакция Кучерова):


уксусный альдегид уксусная кислота
2. Реакции окисления:
а) СН≡СН + 5О2
4СО2+ 2Н2О (горение);
3. Образование ацетиленидов по реакции
замещения:
а) циклическая ЗНС≡СН

б) линейная 2СН≡СН
Ацетиленовые углеводороды используются
для получения поливинилацетата,
акрилацетата (для синтеза каучуков,
пластмасс), бензола и его производных.
Алкадиены СnН2n-2– это углеводороды, содержащие две
двойные связи. Для них характерна
структурная изомерия и цис-, трансизомерия.
По физическим свойствам диеновые
углеводороды могут быть газами и твердыми
веществами.
Промышленное значение имеют диены с
сопряжёнными двойными связями (дивинил,
изопрен).
Химические свойства алкадиенов
определяются особенностями строения
молекул этих углеводородов.
1. Реакция гидрирования:
2. Реакция гидробромирования:
3. Реакция полимеризации:
Для получения синтетических каучуков
с необходимыми свойствами используется
процесс совместной полимеризации
бутадиена-1,3 с другими непредельными
соединениями, например с винилхлоридом
СН2=СНСl, стиролом
СН2=СНС6Н5, акрилонитрилом
СН2=CHCN. Так, бутадиен
– стирольный каучук износостоек и идёт
на изготовление автошин и подошв к
обуви.
Соседние файлы в папке Всякое
