Рассмотрим твердые тела подробнее. По упорядоченности мельчайших частиц, из которых состоят твердые тела, их можно разделить на аморфные и кристаллические.
Рис. 3. Общественное достояние, дата обращения: 2021.08.01, https://commons.wikimedia.org/wiki/File:Allotropy_arabic.jpg.
Рис. 4. Указание автора не требуется, 2021.08.03, Pixabay License, https://pixabay.com/ru/photos/карандаш-графитный-карандаш-запись-1510731/. Указание авторства не требуется, 2021.08.03, Pixabay License, https://pixabay.com/ru/illustrations/алмаз-блестящий-gem-жемчужина-1186139/.
Рис. 1. http://www.astroguide.ru/files/article/55171/main-image/0706_16.jpg
В твёрдых телах молекулы расположены в определённом порядке. Это лёд, соль, металлы, минералы и т. д.
Такие тела называются .


(от греч. κρύσταλλος «лёд», «горный хрусталь; кристалл») — твёрдые тела, в которых частицы (атомы и молекулы) расположены закономерно, образуя кристаллическую решётку.
— условный пространственный каркас, соединяющий частицы твёрдого вещества, для лучшего понимания геометрического строения кристалла.
Кристаллическое строение есть у веществ: поваренная соль, кварц, сахар, алмаз, графит, лёд.
Строение кристалла соли имеет форму правильного гексаэдра
, в вершинах которого находятся атомы \(Na\) и \(Cl\) поочерёдно.
<img alt="ф4_т4
кристалл поваренной соли2.jpg» src=»https://8b08ab88-ee1b-4b04-9ae9-321e0da71ae2.selcdn.net/e61ebd26-678e-43e5-a492-2eff64e88103/%D1%844_%D1%824%284%29%D0%BA%D1%80%D0%B8%D1%81%D1%82%D0%B0%D0%BB%D0%BB%20%D0%BF%D0%BE%D0%B2%D0%B0%D1%80%D0%B5%D0%BD%D0%BD%D0%BE%D0%B9%20%D1%81%D0%BE%D0%BB%D0%B82.jpg»>
<img alt="ф4_т4
кристаллич решетка поваренной соли.jpg» src=»https://8b08ab88-ee1b-4b04-9ae9-321e0da71ae2.selcdn.net/f1587a3a-9bb1-4168-a9f2-894967973fdd/%D1%844_%D1%824%285%29%20%D0%BA%D1%80%D0%B8%D1%81%D1%82%D0%B0%D0%BB%D0%BB%D0%B8%D1%87%20%D1%80%D0%B5%D1%88%D0%B5%D1%82%D0%BA%D0%B0%20%D0%BF%D0%BE%D0%B2%D0%B0%D1%80%D0%B5%D0%BD%D0%BD%D0%BE%D0%B9%20%D1%81%D0%BE%D0%BB%D0%B8.jpg»>
Самая распространённая форм — гексагональная (шестиугольная). В \(1955\) году русский учёный А. Заморский разделил снежинки на \(9\) классов (пластинки, иглы, звёзды, ежи, столбики, пушинки, запонки, призмы, групповые) и \(48\) видов.

Международная комиссия по снегу и льду приняла в \(1951\) году довольно простую классификацию кристаллов льда: пластинки, звёздчатые кристаллы, столбцы или колонны, иглы, пространственные дендриты, столбцы с наконечниками и неправильные формы. И ещё три вида обледенелых осадков: мелкая снежная крупка, ледяная крупка и град.
Любое вещество может существовать в трёх агрегатных состояниях: твёрдом, жидком и газообразном. Всем известно, что жидкая при комнатной температуре вода становится твёрдой при охлаждении до \(0\) °С, а при нагревании до \(100\) °С превращается в пар.
вещества делят на
и
.
Отличие аморфных и кристаллических веществ заключается в степени упорядоченности их внутреннего строения.
В
веществах все частицы располагаются в
п
В
веществах этот порядок
.

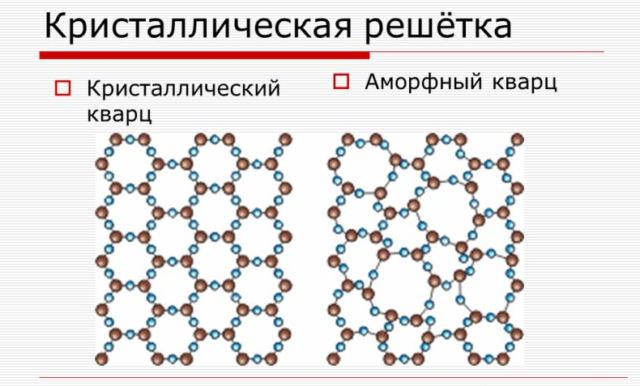
Рис. \(1\). Строение кристаллических и аморфных веществ
называют вещества, в которых частицы располагаются в строгом порядке.
Примеры кристаллических веществ: , , , , , и .

Рис. \(2\). Кристаллы льда

Рис. \(3\). Кристаллы аметиста
называют вещества, у которых нет строгого порядка в расположении частиц.
К аморфным веществам относятся: , , , , , , .

Рис. \(4\). Поделка из пластилина

Рис. \(5\). Янтарь
Кристаллические и аморфные вещества
.
При ударе кристаллические вещества распадаются на мелкие кристаллики формы.
Слово «аморфный» переводится с греческого языка как «бесформенный».

Рис. \(6\). Осколки стекла
вещества имеют определённую температуру плавления
, при которой они сразу становятся жидкими. Например, алюминий плавится при температуре \(660\) °С, а алмаз — при \(3827\) °С.
Если нагревать стекло, то оно сначала размягчается и превращается в пластичную массу.
вещества
точной
— при нагревании они постепенно размягчаются и переходят в вязкое состояние. Способность аморфных веществ становиться вязкими при нагревании позволяет придавать им
.
Рис. 2. Кристаллы льда https://cdn.pixabay.com/photo/2018/02/27/20/40/water-3186525_960_720.jpg
Рис. 3. Кристаллы аметиста https://cdn.pixabay.com/photo/2021/02/02/23/19/gem-5975835_960_720.jpg
Рис. 4. Поделка из пластилина https://cdn.pixabay.com/photo/2012/03/01/01/14/elephant-20071_960_720.jpg
Рис. 5. Янтарь https://upload.wikimedia.org/wikipedia/commons/2/22/Amber.insect.800pix.050203.jpg
Рис. 6. Осколки стекла https://cdn.pixabay.com/photo/2016/11/12/01/34/broken-glass-1818066_960_720.jpg
- Кристаллические и аморфные тела
- Твердые тела
- Аморфные тела
- Кристаллические тела
- Что мы узнали?
- Тест по теме
- Оценка доклада
- Как на графике выглядит процесс кристаллизации для кристаллического тела
- Как на графике выглядит процесс плавления кристаллического тела
- Плавление аморфных тел
- Примеры аморфных тел
- Плавление кристаллических тел
- Примеры кристаллических тел
- Чем отличаются кристаллические и аморфные тела
- Выводы
Кристаллические и аморфные тела


Всего получено оценок: 408.
Всего получено оценок: 408.
В зависимости от внутреннего строения твердые тела бывают либо кристаллическими, либо аморфными. Молекулы и атомы кристаллов расположены в определенной, повторяющейся последовательности на больших расстояниях, сохраняя так называемый дальний порядок. Атомы и молекулы в аморфных телах размещены неупорядоченно, для них характерен ближний порядок со строением аналогичным жидкому состоянию вещества. Рассмотрим основные отличия кристаллических тел от аморфных, которые проявляются в их физических свойствах.
Твердые тела
Все твердые тела обладают следующими общими свойствами:
- Способностью долгое время сохранять форму и объем (геометрические размеры);
- Наличием упругих сил, которые возникают при небольших изменениях объема от внешнего воздействия (сжатия, растяжения или сдвига).
Современные ученые исследуют пространственное расположение атомов и молекул в твердых телах с помощью электронных микроскопов, которые позволяют получить изображение объекта с сильным увеличением (до 10 6
раз). Первый электронный микроскоп был изобретен в 30-х годах прошлого века. В 2018 г. с помощью последних версий этого прибора было получено разрешение 0,39 ангстрем. Напомним, что 1 ангстрем равен 10 -8
см. В большинстве кристаллов это соответствует шагу атомной решетки.
Аморфные тела
Смола, воск, графит, изделия из стекла и янтаря, пластмассы — все это примеры аморфных тел (от греч.слова Amorphous — бесформенный, некристаллический).
Отсутствие дальнего порядка в расположении частиц вещества у аморфных тел приводит к тому, что их физические свойства одинаковы во всех направлениях. Такие тела называют изотропными (слово “изотропный” составлено из двух греческих слов: isos — ровный, tropos — направление). Изотропность физических свойств аморфных тел является следствием хаотичного расположения составляющих их молекул и атомов.
Характерной особенностью аморфных тел является отсутствие определенной температуры плавления, то есть отсутствует четкий переход от твердого состояния к жидкому: при нагревании аморфное тело становится только более текучим.
Кристаллические тела
Твердые тела, в которых молекулы и атомы расположены упорядоченно и образуют периодически повторяющуюся структуру, называются кристаллами. Физические свойства кристаллов (упругие, механические, тепловые, электрические, магнитные, оптические) в разных направлениях неодинаковы. Такое свойство называется анизотропностью. Анизотропия кристаллов объясняется тем, что при упорядоченном расположении частиц расстояния между ними и силы взаимодействия (притяжения и отталкивания) оказываются неодинаковыми в разных направлениях.
Различают кристаллические тела двух видов: монокристаллы и поликристаллы. Главным признаком монокристаллов является повторяющееся внутреннее строение (структура) во всем объеме тела.
Поликристалл — это совокупность (набор) сросшихся друг с другом, хаотически ориентированных, небольших кристаллов. Каждый маленький кристалл обладает свойствами анизотропии, но их совокупность — поликристалл — изотропен.

Часто встречаются кристаллические тела одинаковые по своему химическому составу, но обладающие очень разные физические свойства. Самый известный пример — это углерод, имеющий две модификации: графит и алмаз. Разное строение кристаллических решеток является причиной того, что алмаз имеет рекордные показатели твердости, а графит из-за его мягкости используется в качестве грифелей для карандашей.


Что мы узнали?
Итак, мы узнали, что кристаллические и аморфные тела кроме общих признаков, которые относят их к твердым телам, имеют совершенно разные физические свойства. Аморфные тела обладают изотропными свойствами, а для кристаллов характерна анизотропия физических параметров. Кристаллические тела делятся на монокристаллы и поликристаллы.
Тест по теме

Чтобы попасть сюда — пройдите тест.
Оценка доклада
Всего получено оценок: 408.
А какая ваша оценка?
Как на графике выглядит процесс кристаллизации для кристаллического тела
Давайте теперь прекратим нагревание воды, вынесем кастрюльку на мороз и, оставим ее там на какое-то время. Вода начнет охлаждаться, ее температура будет понижаться. На рисунке 4 это отражено убывающей до нуля прямой наклонной синей линией.

Рис. 4. Процесс кристаллизации – это горизонтальная линия на температурном графике
Когда вода охладится до нуля градусов, начнется процесс превращения жидкости в твердое тело – лед. Потому, что ноль градусов Цельсия – это температура не только плавления, но и кристаллизации льда. Вначале начнут появляться маленькие льдинки. Этому соответствует левая часть красной горизонтальной линии на графике 4.
Примечание:
Если в воде присутствуют пылинки, или другие мелкие примеси, то кристаллизация проходит быстрее. Такие мелкие примеси называют центрами кристаллизации.
Постепенно, количество льда увеличивается, а воды становится все меньше. При этом, температура воды и льда в кастрюльке продолжает оставаться равной нулю градусов по Цельсию.
Когда вся вода в кастрюльке превращается в лед – этому соответствует крайняя правая точка на красной линии на графике.
Только после этого температура льда начинает понижаться от нуля в отрицательную область температур. На рисунке это описано наклонной синей линией, примыкающей справа к горизонтальной красной линии.
Примечание:
Чтобы тело перешло из жидкого состояния в твердое (кристаллизовалось), оно должно избавиться от избытка тепловой энергии. Значит, при кристаллизации, тело отдает энергию окружающим телам. Физики скажут так: «Тело выделяет тепловую энергию во внешнюю среду».
Как на графике выглядит процесс плавления кристаллического тела
Рассмотрим переход из твердого состояния в жидкое — плавление и, обратно — кристаллизацию, на примере льда.
Возьмем лед при начальной температуре «-40» градусов по Цельсию (рис. 3) и поместим его в кастрюльку. Поставим эту кастрюльку на газовую плиту и начнем нагревать лед.
Процесс нагревания льда изображается наклонной линией синего цвета. Потому, что время идет, а температура льда повышается.
Во время нагревания льда от отрицательной температуры до нуля градусов, в емкости будет содержаться только твердый лед.

Рис.3. Процесс плавления – это горизонтальная линия на температурном графике
Как только будет достигнута температура плавления льда – «0» градусов по Цельсию, лед начнет превращаться в жидкость. В кастрюльке начнет понемногу появляться вода. То есть, будет присутствовать и лед, и вода одновременно. Постепенно воды становится все больше, а льда – все меньше.
Мы продолжаем подавать тепловую энергию. Но температура льда во время плавления не меняется до тех пор, пока весь лед не расплавится и не превратится в жидкость.
Поэтому на графике температуры плавление кристаллических тел изображается горизонтальной линией. На рисунке 3 эта линия выделена красным цветом.
- Чтобы тело расплавить, ему нужно передать тепловую энергию. Значит, при плавлении, тепловая энергия поглощается телом.
- При плавлении кристаллических тел, вся полученная тепловая энергия тратится на разрушение кристаллической решетки. Поэтому кристаллические тела имеют конкретную температуру плавления. Она не будет повышаться до тех пор, пока все кристаллическое тело полностью не расплавится.
Когда лед полностью расплавится, в кастрюльке будет присутствовать только жидкая вода. На рисунке 5 это — крайняя правая точка на горизонтальной красной линии.
Если продолжать подводить тепловую энергию, температура воды начнет повышаться. Идет процесс нагревания воды. На графике процесс нагревания – это еще одна наклонная прямая линия, она располагается справа от красной линии плавления.
Плавление аморфных тел
Аморфные тела конкретной температуры плавления не имеют. Строение аморфных тел больше похоже на очень вязкую жидкость, чем на твердое кристаллическое тело. Во время нагревания они будут становиться более текучими, все больше проявляя свойство жидкости. При этом, хрупкость, присущая твердому состоянию, будет исчезать. Одновременно с плавлением, температура аморфных тел будет повышаться.
Важно!
Одновременно с плавлением, температура
аморфных тел будет непрерывно повышаться. Потому, что такие тела не имеют конкретной температуры плавления.
Примеры аморфных тел
- канифоль (смола хвойных деревьев);
- стекло;
- эбонит;
- сургуч;
- различные пластмассы;
Примечание:
Эбонит («Эбенос» др.-греч. — чёрное дерево) – это вулканизированный каучук с добавлением большого количество серы, до 50 % от массы каучука. Цвет эбонита обычно тёмно-бурый или чёрный. Этот материал не проводит электрических ток – то есть, является хорошим изолятором.
Плавление кристаллических тел
Чтобы кристаллическое тело начало плавиться, его нужно нагреть до определенной температуры. Одни кристаллические тела будут плавиться при низкой температуре, а другие – при высокой. То есть, у каждого вещества своя температура плавления. Ее можно найти в справочнике физики. При этом, пока вещество не расплавится, его температура изменяться не будет.
Важно!
Кристаллические тела имеют конкретную температуру плавления. Пока кристаллическое вещество полностью не расплавится, его температура не изменится!
- Кристаллические вещества плавятся при той же температуре, при которой они будут превращаться в твердое тело (кристаллизоваться).
- Чтобы жидкое вещество начало кристаллизоваться, оно сначала должно остыть до определенной температуры.
- Температура плавления и температура кристаллизации – это одна и та же температура.
Примеры кристаллических тел
- лед;
- свинец;
- алюминий;
- ртуть;
- железо;
- золото;
- серебро;
Чем отличаются кристаллические и аморфные тела
У кристаллических тел есть строго упорядоченное положение мельчайших частиц. Эти частички образуют правильную кристаллическую решетку (рис. 1).
Примечание:
Атомы кристаллических тел располагаются в узлах кристаллической решетки. Связи между атомами обозначены линиями. Эти линии у различных кристаллических тел образуют разные пространственные фигуры.

Рис.1. Кристаллические тела имеют более упорядоченную структуру в твердом состоянии, чем аморфные тела
Аморфные тела не обладают строгой упорядоченностью мельчайших частиц — молекул
, из которых они состоят. У аморфных тел порядок есть, но он не так выражен, как у кристаллических тел. Аморфное тело по своему строению больше похоже на очень вязкую жидкость, чем на твердое тело. Поэтому, аморфные тела обладают текучестью.
Основные отличия кристаллических и аморфных тел приведены на рисунке 2.

Рис. 2. Сравниваем свойства кристаллических и аморфных тел
- Благодаря текучести, спустя много лет после изготовления, верхняя часть установленного в раму оконного стекла, становится немного тоньше, чем его нижняя часть.
- Канифоль со временем может принимать форму сосуда, в который ее поместили.
- из жидкого в твердое состояние – кристаллизация;
- из твердого в жидкое состояние – плавление;
Выводы
- Все тела в твердом состоянии по их строению можно разделить на аморфные и кристаллические.
- Переход из твердого в жидкое состояние – это плавление, а из жидкого в твердое состояние – кристаллизация;
- Аморфные тела конкретной температуры плавления не имеют. Их строение больше похоже на очень вязкую жидкость, чем на твердое кристаллическое тело. Одновременно с плавлением, температура аморфных тел будет повышаться.
- Кристаллическое тело плавится и кристаллизуются при одной и той же температуре. Эту температуру называют температурой плавления (кристаллизации). Т. е. пока происходят процессы плавления и кристаллизации, температура не меняется.
- Во время плавления тело получает тепловую энергию ( количество теплоты
), а во время кристаллизации тело отдает тепловую энергию в окружающее пространство. - Сколько теплоты тело получило во время плавления, столько же оно отдаст в окружающую среду во время кристаллизации. Потому, что выполняется закон сохранения энергии
(тепловой). - Чтобы твердое тело превратить в жидкость, ему нужно сообщить (передать) тепловую энергию.
- Чтобы жидкое тело превратить в твердое, нужно избавить его от излишка тепловой энергии.
- Перед тем, как расплавить твердое кристаллическое вещество, нужно нагреть его до температуры плавления. Температуру плавления различных веществ можно найти в справочнике физики.


