Встречающиеся в органических соединениях кратные связи (двойные или тройные):
образуются при обобществлении двумя атомами более чем одной пары электронов:
Н2С СН2; R2С О; HС CH; RС N и т.п.
Кратные связи являются сочетанием σ- и π-связей.
Двойная связь состоит из одной σ- и одной π-связей и осуществляется 4-мя общими электронами.
Тройная связь является комбинацией из одной σ- и двух π-связей и включает в себя шесть электронов.
Число электронных пар, участвующих в образовании ковалентной связи называется порядком связи.
Таким образом, порядок простой связи
равен 1,двойной – 2,тройной – 3.
В случае сопряжённых (делокализованных) связей порядок связи отличается от этих целочисленных значений
Ковалентная связь считается локализованной, если её электронная пара находится в поле двух ядер и связывает только два атома.
Делокализованная связь — связь, электронная пара которой рассредоточена между несколькими (более двух) ядрами атомов (подобие металлической связи).
Такая делокализация (рассредоточение) электронов характерна для сопряжённых π-связей, то есть кратных связей, чередующихся с одинарными.
Делокализация подвижных π-электронов приводит к тому, что в сопряжённой системе связи становятся нецелочисленными (дробными), то есть ни двойными или тройными, ни одинарными.
Например, делокализация π-связей в молекуле CH2=CH–CH=CH2 обусловлена возможностью перекрывания р-орбиталей атомов C2 и C3:

Непредельные углеводороды

Всего получено оценок: 542.
Органические соединения, содержащие кратные связи (двойные или тройные), называются ненасыщенными или непредельными углеводородами. О том, на какие классы ненасыщенные углеводороды, какими свойствами они обладают, говорим в этой статье.
Классы
К ненасыщенным углеводородам относятся ациклические классы веществ – алкены, алкины, алкадиены. Подробнее о классах ненасыщенных углеводородов рассказано в таблице.
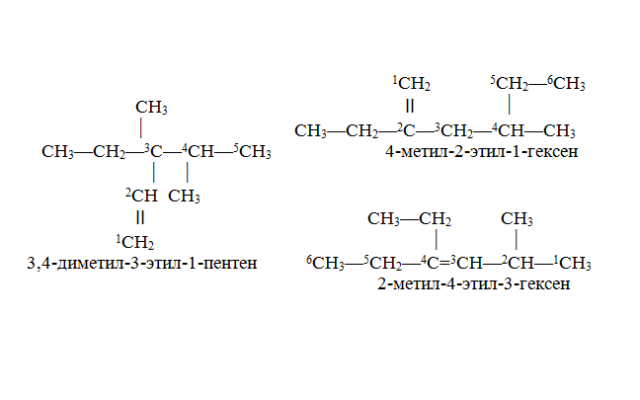
Рис. 1.Структурные формулы ненасыщенных углеводородов.
Для ненасыщенных углеводородов характерна изомерия углеродного скелета, положения кратной связи и межклассовая изомерия (алкины с алкадиенами, алкены с циклоалканами). Пример: бутадиену (СН2=СН-СН=СН2) соответствует бутин-1 (СН≡С-СН2-СН3) и бутин-2 (СН3-С≡С-СН3).
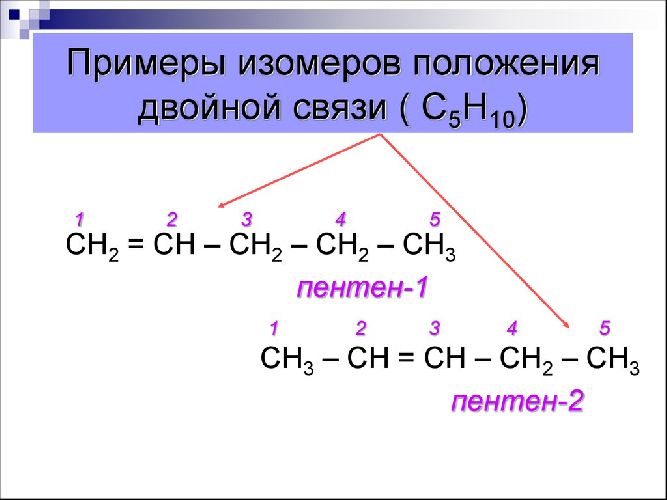
Рис. 2. Примеры изомеров.
Свойства
В зависимости от количества атомов углерода ненасыщенные углеводороды – это газы (C2-С4), жидкости (C5-С17), твёрдые вещества (C18 и выше). Плотность, температуры плавления и кипения веществ увеличиваются с возрастанием молекулярной массы.
Ненасыщенные углеводороды более активны, чем предельные углеводороды. За счёт разрыва кратных связей в молекулах непредельные углеводороды могут присоединять дополнительные атомы водорода, становясь насыщенными углеводородами. Также присоединяют галогены и галогеноводороды. В таблице описаны основные химические свойства непредельных углеводородов.
Ненасыщенные углеводороды используют в сварке, в качестве растворителей, для изготовления каучука.

Рис. 3. Искусственный каучук.
Что мы узнали?
Из урока 9 класса узнали, что такое непредельные или ненасыщенные углеводороды. К ним относятся алкены с одной двойной связью, алкины с одной тройной связью и алкадиены с двумя двойными связями. В зависимости от количества связей в молекуле соединения находятся в газообразном, жидком, твёрдом состоянии. Эти вещества более активны, чем предельные углеводороды, за счёт разрыва кратных связей. Вступают в реакции присоединения, способны полимеризоваться.
Тест по теме
Чтобы попасть сюда — пройдите тест.
Оценка доклада
А какая ваша оценка?
Классификация соединений по строению углеродной цепи
В зависимости от строения углеродной цепи (углеродного скелета) органические соединения делят на
Ациклические соединения — соединения с открытой (незамкнутой) углеродной цепью. Эти соединения называются также алифатическимиТермин «алифатические (жирные) соединения» происходит от греческого слова «aleiphar» — «жир», т.к. впервые структуры с длинными углеродными цепями были обнаружены в составе жиров.
Среди ациклических соединений различают предельные (насыщенные), содержащие в скелете только одинарные связи C–C и непредельные (ненасыщенные), включающие кратные связи C=C и C≡C.
Ациклические соединения подразделяют также на соединения с неразветвленной и разветвленной цепью. В этом случае учитывается
число связей атома углерода с другими углеродными атомами (тип атомов углерода)
Неразветвленные и разветвленные углеродные цепи
Атом углерода, связанный в цепи только с одним другим атомом углерода, называют первичным, с двумя – вторичным, с тремя – третичным, с четырьмя – четвертичным.
Цепь, содержащая только первичные и вторичные атомы углерода, является неразветвленной и называется нормальной (обозначается буквой «н-» перед названием соединения).
Цепь, в которую входят третичные и/или четвертичные атомы углерода, становится разветвленной (в названии часто обозначается приставкой «изо»).
Атомы углерода: —
Особое место среди веществ цепного строения занимают соединения с молекулярной массой, достигающей десятков тысяч и даже миллионов а.е.м.атомная единица массы Эту группу веществ называют высокомолекулярными соединениями или полимерами. Длинные цепные молекулы полимеров (макромолекулы) могут содержать кратные связи, разветвления, гетероатомыАтомы, кроме углерода и водорода, в органической химии называют гетероатомами (от греч. heteros — другой, иной)., функциональные группы и циклические фрагменты.
Циклические соединения — соединения с замкнутой цепью химически связанных атомов.
В зависимости от природы атомов, составляющих цикл, различают карбоциклические и гетероциклические соединения.
Карбоциклические соединения (карбоциклы) — соединения, которые содержат в цикле только атомы углерода.
Карбоциклы делятся на две существенно различающихся по химическим свойствам группы: алифатические циклические (сокращенно алициклические) и ароматическиеАроматические соединения – соединения, содержащие устойчивые циклические группы атомов с замкнутой системой сопряженных связей (простейший представитель — бензол). соединения.
Гетероциклические соединения (гетероциклы) — соединения, содержащие в цикле, кроме атомов углерода, один или несколько атомов других элементов (гетероатомовГетероатом (от греч. heteros – другой, иной) — любой атом, кроме углерода и водорода.) — кислород, азот, серу и др.
Гетероциклические соединения также подразделяются на алифатические (например, этиленоксид) и ароматические (тиофен, пиридин) гетероциклы.
Ковалентная химическая связь

Всего получено оценок: 1081.
Ковалентная связь – это связь, связывающая чаще всего атомы неметаллов молекулах и кристаллах. О том, какую химическую связь называют ковалентной говорим в этой статье.
Что такое ковалентная химическая связь?
Ковалентная химическая связь – это связь, осуществляемая за счет образования общих (связывающих) электронных пар.
Если между двумя атомами имеется одна общая электронная пара, то такая связь называется одинарной (ординарной), если две – двойной, если три – тройной.
Связь принято обозначать горизонтальной черточкой между атомами. Например, в молекуле водорода одинарная связь: H-H; в молекуле кислорода двойная связь: O=O; в молекуле азота тройная связь:
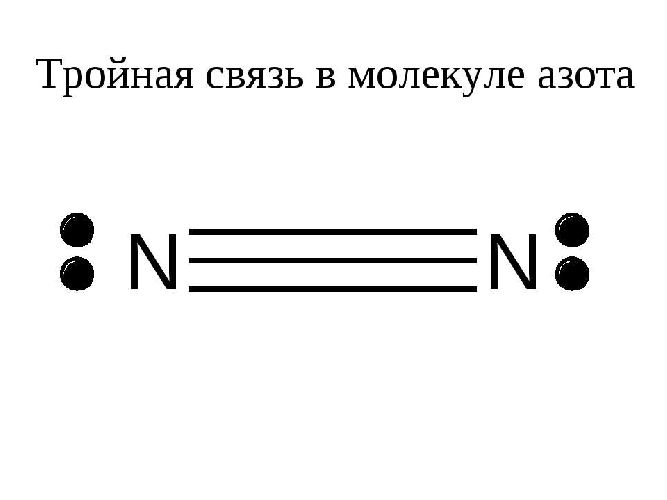
Рис. 1. Тройная связь в молекуле азота.
Чем выше кратность связи, тем прочнее молекула: наличие тройной связи объясняет высокую химическую устойчивость молекул азота.
Образование и виды ковалентной связи
Существуют два механизма образования ковалентной связи: обменный механизм и донорно-акцепторный механизм:
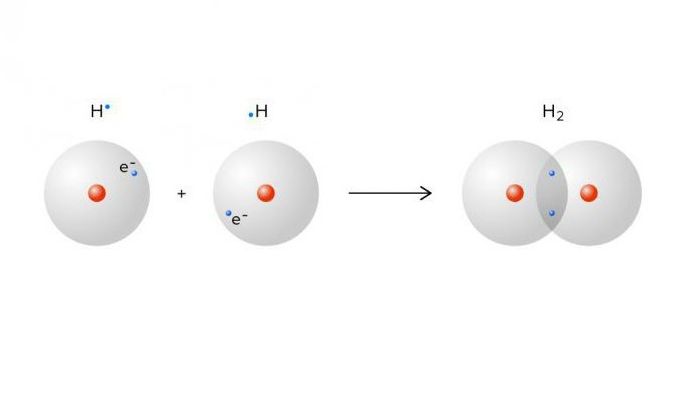
Рис. 2. Образование молекула водорода.
Общая электронная пара принадлежит каждому из связанных атомов, то есть электронная оболочка у них завершена.
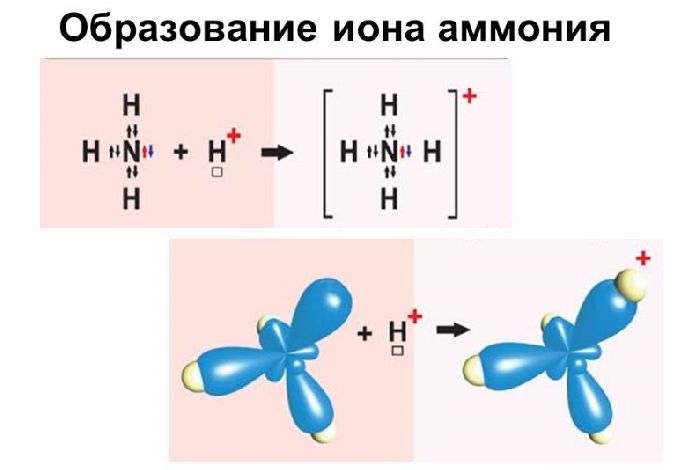
Рис. 3. Образование иона аммония.
Так образуется ион аммония NH4 +. Этот положительно заряженный ион (катион) образуется при взаимодействии газа аммиака с любой кислотой. В растворе кислоты существуют катионы водорода (протоны), в водородной среде образующие катион гидроксония H3O+. Формула аммиака NH3: молекула состоит из одного атома азота и трех атомов водорода, связанных одинарными ковалентными связями по обменному механизму. У атома азота остается при этом одна неподеленная электронная пара. Ее он предоставляет в качестве общей, как донор, иону водорода H+, имеющему свободную орбиталь.
Ковалентная химическая связь в химических веществах может быть полярной и неполярной. Связь не имеет дипольного момента, то есть полярности, если связаны два атома одного и того же элемента, имеющие одно и то же значение электроотрицательности. Так, в молекуле водорода связь неполярная.
В молекуле хлороводорода HCl ковалентной одинарной связью соединены атомы с разной электроотрицательностью. Общая электронная пара оказывается сдвинутой в сторону хлора, у которого выше сродство к электрону и электроотрицательность. Возникает дипольный момент, связь становится полярной. При этом происходит частичное разделение заряда: атом водорода становится положительным концом диполя, а атом хлора – отрицательным.
Любая ковалентная связь обладает следующими характеристиками: энергия, длина, кратность, полярность, поляризуемость, насыщаемость, направленность в пространстве
Ковалентная химическая связь образуется перекрытием пары валентных электронных облаков. Этот вид связи может образовываться по донорно-акцепторному механизму, а также по обменному механизму. Ковалентная связь бывает полярной и неполярной и характеризуется наличием длины, кратности, полярности, направленности в пространстве.
