Для
объяснения строения простых и комплексных
частиц с центральными атомами d-элементов,
имеющими незавершённый внутренний
(n-1)d–подуровень,
используют метод ВС, дополненный теорией
кристаллического поля.
Л8.
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ И ИХ
СВОЙСТВА.
Отдельные химические элементы,
взаимодействуя между собой, образуют
соединения первого порядка: оксиды,
кислоты, основания, соли; которые,
реагируя друг с другом, образуют
соединения высшего порядка – комплексные
соединения.
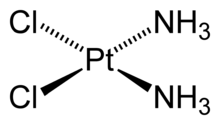
-платин
— одно из многих координационных соединений
Ко́мплексные соедине́ния
( лат.
— сочетание, обхват) или координацио́нные соедине́ния
( лат.
— «вместе» и ordinatio
— «упорядочение») — это соединения
(нейтральные молекулы или ионы
), которые образуются в результате присоединения к данному иону
(или атому
), называемому комплексообразователем
, нейтральных молекул
или других ионов, называемых лигандами
. Теория комплексных соединений ( координационная теория
) была предложена в 1893
г. А. Вернером
.
Комплексные соединения, имеющие внешнюю сферу
, в водном растворе полностью диссоциируют
на комплексный малодиссоциирующий катион
или анион
. Комплексные соединения без внешней сферы
в воде нерастворимы (например, карбонилы металлов
).
Комплексные соединения разнообразны и многочисленны.
- Содержание
- Вид химической связи в комплексных соединениях
- Координационная теория Вернера.
- Химическая связь в комплексных соединениях и их строение
- Метод валентных связей
- Номенклатура.
- Теория кристаллического поля
- < глицин < пиридин < этилендиамин< NC
- Пространственная (геометрическая) изомерия
- Природа химических связей в комплексных соединениях.
- Структура и стереохимия
- Устойчивость комплексных соединений.
- Метод валентных связей
- Типы комплексных соединений
- По заряду комплекса
- По числу мест, занимаемых лигандами в координационной сфере
- По природе лиганда
Вид химической связи в комплексных соединениях
Однако простая
электростатическая теория не в состоянии
объяснить избирательность (специфичность)
комплексообразования, поскольку она
не принимает во внимание природу
центрального атома и лигандов, особенности
строения их электронных оболочек. Для
учета этих факторов электростатическая
теория была дополнена поляризационными
представлениями, согласно которым
комплексообразованию благоприятствует
участие в качестве центральных атомов
небольших многозарядных катионов
d-элементов,
обладающих сильным поляризующим
действием, а в качестве лигандов –
больших, легко поляризующихся ионов
или молекул. В этом случае происходит
деформация электронных оболочек
центрального атома и лигандов, приводящая
к их взаимопроникновению, что и вызывает
упрочнение связей.
б) Метод валентных
связей.
В методе валентных
связей предполагается, что центральный
атом комплексообразователя должен
иметь для образования ковалентных
связей с лигандами свободные орбитали,
число которых определяет максимальное
значение к.ч. комплексообразователя.
При этом ковалентная σ-связь возникает
при перекрывании свободной орбитали
атома комплексообразователя с заполненными
орбиталями доноров, т.е. содержащими
неподеленные пары электронов. Эта связь
называется координационной
связью.
Решение
.
Тетраэдрическое строение молекул
характерно при образовании sp 3
-гибридных
орбиталей.
Решение
.
Линейное строение этого иона является
следствием образования двух гибридных
sp-орбиталей
ионом Cu +
,
на которые поступают электронные пары
NH 3
.
в) Теория
кристаллического поля.
Решение
.
Ион парамагнитен в соответствии с тем,
что имеется один неспаренный электрон,
локализованный на ионе Ti 3+
.
Этот электрон занимает одну из трех
вырожденных d ε
-орбиталей.
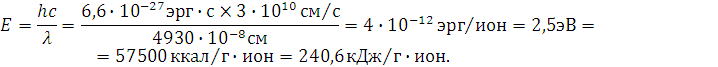
Длина волны 4930Å
относится к зеленой части видимого
спектра. Видимый спектр имеет следующие
длины волн (Å):
Фиолетовый
4000-4240 Желтый 5750-5850
Голубой
4240-4900 Оранжевый 5850-6470
Зеленый
4900-5750 Красный 6470-7100
При поглощении
определенной части спектра само вещество
является окрашенным в дополнительный
цвет.
Поглощение:
фиолетовый, синий, голубой, сине-зеленый,
зеленый
.
Окраска вещества: зелено-желтый, желтый,
оранжевый, красный, пурпурный
,
соответственно.
Таким образом,
если соединения поглощают лучи в синей
части спектра, они окрашены в дополнительный
желтый цвет, например, оксид свинца PbO.
Однако часто бывает, что окраска связана
с поглощением в различных частях видимого
спектра.
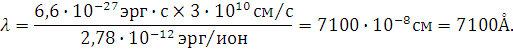
Следовательно,
гексагидрат Cr 3+
поглощает лучи в красной части спектра,
а соединения трехвалентного хрома в
водных растворах должны быть окрашены
в зеленый цвет, что согласуется с окраской
растворов.
- #
- #
- #
- #
- #
- #
Во внутренней сфере между комплексообразователем и лигандами существуют ковалентные связи, образованные, в том числе, и по донорно-акцепторному механизму. Для образования таких связей необходимо наличие свободных орбиталей у одних частиц (имеются у комплексообразователя) и неподеленных электронных пар у других частиц (лиганды). Роль донора (поставщика электронов) играет лиганд, а акцептором, принимающим электроны, является комплексообразователь. Донорно-акцепторная связь возникает как результат перекрывания свободных валентных орбиталей комплексообразователя с заполненными орбиталями донора.
Между внешней и внутренней сферой существует ионная связь. Приведем пример.
Электронное строение атома бериллия:
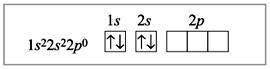
Электронное строение атома бериллия в возбужденном состоянии:
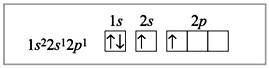
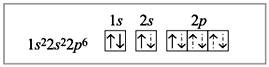
Пунктирными стрелками показаны электроны фтора; две связи из четырех образованы по донорно-акцепторному механизму. В данном случае атом Be является акцептором, а ионы фтора – донорами, их свободные электронные пары заполняют гибридизованные орбитали (sp3-гибридизация).
Номенклатура комплексных соединений.
В соединении сначала называют анион, а затем катион. При указании состава внутренней сферы прежде всего называют анионы, прибавляя к латинскому названию суффикс -о-, например: Cl– – хлоро, CN– – циано, OH– – гидроксо и т.д. Далее называют нейтральные лиганды и, в первую очередь, аммиак и его производные. При этом пользуются терминами: для координированного аммиака – аммин, для воды – аква. Число лигандов
указывают греческими словами: 1 – моно, 2 – ди, 3 – три, 4 – тетра, 5 – пента, 6 – гекса. Затем переходят к названию центрального атома. Если центральный атом входит в состав катионов, то используют русское название соответствующего элемента и в скобках указывают его степень окисления (римскими цифрами). Если центральный атом содержится в анионе, то употребляют латинское название элемента, а в конце прибавляют окончание — ат
. В случае неэлектролитов степень окисления центрального атома не приводят, т.к. она однозначно определяется из условия электронейтральности комплекса.
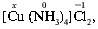
1•x + 2•(–1) = 0, x = +2, C. O.(Cu) = +2.
Аналогично находят степень окисления иона кобальта:
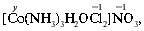
y + 2•(–1) + (–1) = 0, y = +3, С. О.(Со) = +3.
Чему равно координационное число кобальта в этом соединении? Сколько молекул и ионов окружает центральный ион? Координационное число кобальта равно шести.
Название комплексного иона пишут в одно слово. Степень окисления центрального атома обозначают римской цифрой, помещенной в круглые скобки. Например:
На примере нескольких комплексных соединений определим структуру молекул (ион-комплексообразователь, его С. О., координационное число, лиганды, внутреннюю и внешнюю сферы), дадим название комплексу, запишем уравнения электролитической диссоциации.
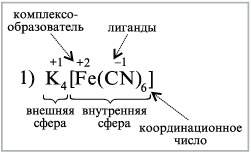
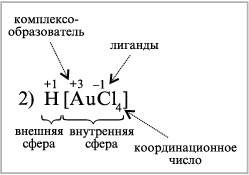
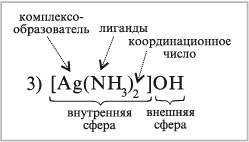
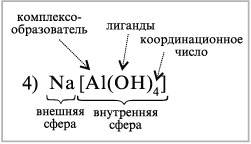
К комплексным соединениям относятся и многие органические вещества, в частности, известные вам продукты взаимодействия аминов с водой и кислотами. Например, соли хлорид метиламмония и хлорид фениламмония являются комплексными соединениями. Согласно координационной теории они имеют следующее строение:
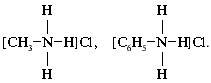
Здесь атом азота – комплексообразователь, атомы водорода при азоте, радикалы метил и фенил – лиганды. Вместе они образуют внутреннюю сферу. Во внешней сфере находятся хлорид-ионы.
Многие органические вещества, имеющие большое значение в жизнедеятельности организмов, представляют собой комплексные соединения. К ним относятся гемоглобин, хлорофилл, ферменты и др.
Координационная теория Вернера.
Теория была создана в 1893г.
Комплексные соединения характеризуются
наличием центрального иона –
комплексообразователя (d– элементы:Fe,Co,Cu,Zn,Mo,Mn; режеp–
элементы:Al,Sn,Pb; изs–
элементов толькоLi).Центральный ион окружен лигандами, в
качестве них могут быть частицы, имеющие
свободную пару электронов (Н 2
О:,
:NH 3
, :Cl —
).
Число лигандов определяется координационным
числом, которое обычно в два раза больше,
чем степень окисления комплексообразователя.В состав внешней сферы входят ионы
противоположного знака.
Химическая связь в комплексных соединениях и их строение
В кристаллических
комплексных соединениях с заряженными
комплексами связь между комплексом и
внешнесферными ионами ионная, связи
между остальными частицами внешней
сферы – межмолекулярные (в том числе и
водородные). В молекулярных комплексных
соединениях связь между комплексами
межмолекулярная.
В большинстве
комплексных частиц между центральным
атомом и лигандами связи ковалентные.
Все они или их часть образованы по
донорно-акцепторному механизму (как
следствие – с изменением формальных
зарядов). В наименее прочных комплексах
(например, в аквакомплексах щелочных и
щелочноземельных элементов, а также
аммония) лиганды удерживаются
электростатическим притяжением. Связь
в комплексных частицах часто называют
донорно-акцепторной или координационной
связью.
Рассмотрим ее
образование на примере аквакатиона
железа(II). Этот ион образуется по реакции:
Электронная формула
атома железа – 1 s
2
2 s
2
2 p
6
3 s
2
3 p
6
4 s
2
3 d
6
.
Составим схему валентных подуровней
этого атома:

При образовании
двухзарядного иона атом железа теряет
два 4 s
-электрона:
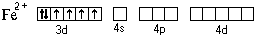
Ион железа
акцептирует шесть электронных пар
атомов кислорода шести молекул воды на
свободные валентные орбитали:
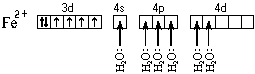
Образуется
комплексный катион, химическое строение
которого можно выразить одной из
следующих формул:
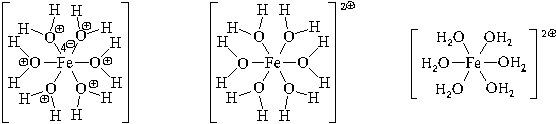
Пространственное
строение этой частицы выражается одной
из пространственных формул:
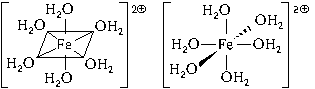
Форма координационного
полиэдра – октаэдр. Все связи Fe-O
одинаковые. Предполагается sp
3
d
2
-гибридизация
АО атома железа. Магнитные свойства
комплекса указывают на наличие неспаренных
электронов.
Если FeCl 2
растворять в растворе, содержащем
цианид-ионы, то протекает реакция
Тот же комплекс
получается и при добавлении к раствору
FeCl 2
раствора цианида калия KCN:
Это говорит о том,
что цианидный комплекс прочнее
аквакомплекса. Кроме того магнитные
свойства цианидного комплекса указывают
на отсутствие неспаренных электронов
у атома железа. Все это связано с несколько
иным электронным строением этого
комплекса:
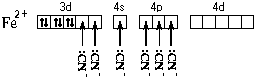
Более » сильные»
лиганды CN 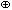
образуют более прочные связи с атомом
железа, выигрыша в энергии хватает на
то, чтобы » нарушить» правило Хунда
и освободить 3 d
-орбитали
для неподеленных пар лигандов.
Пространственное строение цианидного
комплекса такое же, как и аквакомплекса,
но тип гибридизации другой – d
2
sp
3
.
» Сила» лиганда
зависит прежде всего от электронной
плотности облака неподеленной пары
электронов, то есть, она увеличивается
с уменьшением размера атома, с уменьшением
главного квантового числа, зависит от
типа гибридизации ЭО и от некоторых
других факторов. Важнейшие лиганды
можно выстроить в ряд по возрастанию
их » силы» (своеобразный » ряд
активности» лигандов), этот ряд
называется
спектрохимическим рядом лигандов
.
В результате трудов многих ученых ряд
транс-влияния лигандов в настоящее
время выглядит следующим образом:
CO > CN
–
> NO 2
–
> ЭДТА
> NH 3
> SCN –
>
H 2
O
> OH –
> F –
>
Cl –
> SCN –
> Br –
> I –
Слева находятся
лиганды более сильного поля, справа –
более слабого.
Ряд транс-влияния
лигандов дает возможность делать важные
предсказания. В частности, с его помощью
можно судить о направлении реакций
замещения лигандов во внутренней сфере
координационных соединений.
Химические
свойства комплексных соединений
Для комплексных
соединений, прежде всего, характерны
те же свойства, что и для обычных
соединений тех же классов (соли, кислоты,
основания). Если комплексное соединение
кислота, то это сильная кислота, если
основание, то и основание сильное.
Электролитическая
диссоциация комплексных ионов подчиняется
закону действующих масс и количественно
характеризуется константой диссоциации,
которая носит название константы
нестойкости К н
,
и для последнего процесса диссоциации:
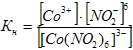
.
У типичных
комплексных ионов К н
очень мала и является мерой его
устойчивости.
Если комплексное
соединение кислота, то это сильная
кислота, если основание, то и основание
сильное. Эти свойства комплексных
соединений определяются только наличием
ионов H +
или OH —
.
Кроме этого
комплексные кислоты, основания и соли
вступают в обычные реакции
обмена
,
например:
Кроме этого в
реакцию может вступать и сама комплексная
частица, причем, тем активнее, чем она
менее устойчива. Обычно это реакции
замещения лигандов, протекающие в
растворе, например:
а также
кислотно-основные реакции типа
Последняя реакция
– простейший пример разложения
комплексного соединения. В данном случае
она протекает при комнатной температуре.
Другие комплексные соединения разлагаются
при нагревании, например:
Для оценки
возможности протекания реакции замещения
лигандов можно использовать
спектрохимический ряд, руководствуясь
тем, что более сильные лиганды вытесняют
из внутренней сферы менее сильные.
Последняя реакция
– простейший пример разложения
комплексного соединения. В данном случае
она протекает при комнатной температуре.
Другие комплексные соединения разлагаются
при нагревании, например:
Окислительно-восстановительные
реакции
с участием
комплексных соединений. Комплексные
соединения могут участвовать в
окислительно-восстановительных
реакциях. При этом изменяется степень
окисления центрального атома. Возможны
реакции двух типов:
а) Изменение степени
окисления без
разрушения комплекса
б) Изменение степени
окисления с
разрушением комплекса
в результате восстановления центрального
иона до металла
Метод валентных связей
Согласно
представлениям метода ВС химическая
связь в комплексных соединениях носит
донорно-акцепторный характер. Свободные
электронные пары, которыми обладают
лиганды, заполняют пустые орбитали
центрального иона. Эти орбитали объединяют
в гибридные комбинации в зависимости
от координационного числа (к.ч.).
Комплексные
соединения с к.ч., равным двум, описываются,
как правило, с позиции sp-гибридизации.
Примерами являются комплексные соединенияAg(I);Cu(I);Au(I).
Рассмотрим комплексный ионAgCl 2
–
.
Электронная конфигурация ионаAg +
4d 10
, орбитали 5s,
5p, 5d, 5fи 5gпустые. Самые низкие
по энергии из них 5sи 5p.
Именно туда “селятся” две электронные
пары от двух анионов хлора:

Таким образом,
рассматриваемый комплекс описывается
с позиции sp-гибридизации,
ион серебра и два аниона хлора расположены
на прямой.
Комплексные
соединения с к.ч., равным трём, обычно
описываются исходя из sp 2
-гибридизации,
например,Ag(CN) 3
2–
.
Три анионаCN –
расположены вокруг катионаAg +
по вершинам правильного треугольника.
В качестве примеров
комплексных соединений с к.ч., равным
четырём, рассмотрим два комплекса никеля
(II):NiF 4
2–
;Ni(CN) 4
2–
.
Электронная “макушка” ионаNi 2+
– 3d 8
, более высокие
по энергии орбитали пусты:

Как видно, возможны
два варианта – заполнение электронными
парами лигандов только пустых орбиталей
и освобождение одной 3d-орбитали за счёт
спаривания электронов с последующим
заполнением её электронной парой
лиганда, а затем – заполнение пустых
орбиталей. Очевидно, всё будет определяться
энергетическим балансом – выигрышем
в энергии, связанным с образованием
связи (Е св
), и энергетическим
проигрышем, равным энергии образования
электронной пары из неспаренных
электронов (Е пары
). Если Е пары
> Е св
, то спиновое состояние
центрального иона в комплексе останется
тем же, что и у свободного иона. В случае,
если Е св
> Е пары
, происходит
образование пары и освобождение одной
орбитали в 3d-оболочке.
Всё будет определяться прочностью связи
лиганд–центральный ион. На практике
Е св
> Е пары
в случае
только цианидных комплексов двухзарядных
центральных ионов, а для комплексов с
трёхзарядным ионом – комплексообразователем
со следующими лигандами:CN –
,NO 2
–
,NH 3
.
Вернёмся к
рассматриваемым комплексным ионам.
Для NiF 4
2–
Е пары
> Е св
и электронное
состояние центрального иона останется
неизменным:
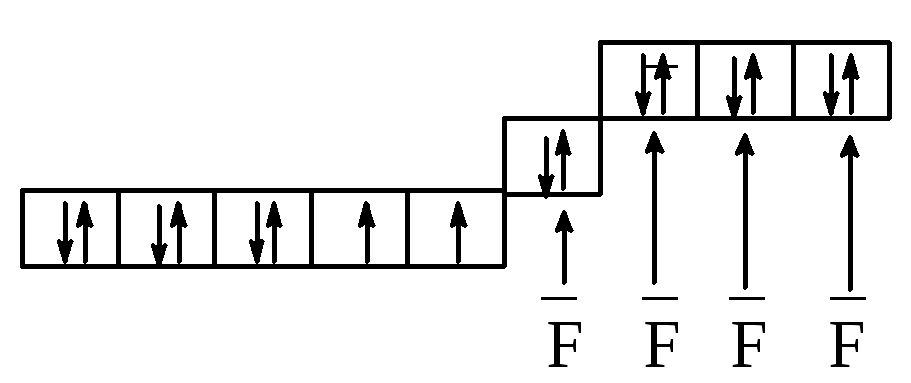
Связь в комплексном
анионе характеризует sp 3
-гибридизация,
комплексный ион имеет тетраэдрическое
строение и характеризуется высоким
значением спина.
Для цианидного
комплексного аниона Е св
> Е пары
,
электроны “загоняются” в пару, и
освободившаяся орбиталь будет занята
парой электронов:

Химическую связь
в этом комплексе описываем с позиций
dsp 2
-гибридизации,
комплексный анион имеет квадратное
строение и характеризуется низким
спином.
В связи со спиновым
состоянием рассматриваемых частиц
напомним, что наличие или отсутствие
неспаренных электронов имеет отношение
к магнитным характеристикам веществ.
Ферромагнитные вещества мощно
взаимодействуют с магнитным полем; это
в первую очередь железо, кобальт, никель
и комбинации на их основе. Парамагнитные
вещества слабо реагируют на магнитное
поле, фактически отзываются на него.
Частицы парамагнитных веществ содержат
в своём составе неспаренные электроны.
Наконец, диамагнитные вещества вообще
безразличны к магнитному полю. Частицы,
составляющие такие вещества (атомы,
молекулы, ионы), не содержат неспаренных
электронов. Перечисленные выше комплексные
анионы (кроме NiF 4
2–
)
являются диамагнетиками. ИонNiF 4
2–
обладает парамагнитными свойствами.
Парамагнетизм является основой
физико-химического метода – электронного
парамагнитного резонанса (ЭПР),
позволяющего изучать функциональные
особенности вещества.
Для описания
химической связи в комплексах с к.ч.,
равным пяти, как правило, привлекают
представления о dsp 3
-гибридизации.
Рассмотрим в качестве примера не совсем
традиционное комплексное соединение
– пентакарбонил железаFe(CO) 5
.
Карбонилы – соединения металлов с
оксидом углерода (II) могут
рассматриваться, по крайней мере в
отношении химической связи, как
своеобразные комплексные соединения.
При этом, говоря о карбонилах и других
соединениях с СО, следует иметь в виду,
что это очень сильные лиганды, дающие
прочную химическую связь.

Химическая связь
в молекуле Fe(CO) 5
описывается с позицииdsp 3
-гибридизации,
молекула имеет форму тригональной
бипирамиды, она диамагнитна.


Связь характеризуется
sp 3
d 2
-гибридной
комбинацией орбиталей; для того, чтобы
показать, что задействованы внешниеd-орбитали, говорят о
“внешней” гибридизации. Комплексный
катион имеет октаэдрическое строение
и является парамагнитным.
В случае цианидного
комплекса Е св
> Е пары
,
поэтому шесть 3d-электронов
займут три орбитали, а остальные две
будут заполняться электронами лигандов:

Тип гибридизации
орбиталей будет таким же, что и в
предыдущем случае, однако здесь
задействованы внутренние d-орбитали,
поэтому говорят о “внутренней”
гибридизации. Комплексный анион имеет
октаэдрическое строение и является
диамагнитным.
Номенклатура.
Сначала называют анион, а затем катион.
Если лиганд является кислотным остатком,
то к его названию добавляют приставки,
указывающие на их число, и окончание
«о». Затем называют нейтральные лиганды,
добавляя приставки, указывающие на их
число.Далее называют ион комплексообразователя
с указанием степени окисления (на письме
обозначается римскими цифрами в круглых
скобках). В анионных комплексах к
названию комплексообразователя
добавляют суффикс «ат». В катионных
комплексах даются латинские названия
ионам металлов.
- Комплексные соединения
— статья из Большой советской энциклопедии
. - Комплексообразование
Основателем координационной теории комплексных соединений является швейцарский химик Альфред Вернер
(1866—1919). Координационная теория Вернера 1893 года была первой попыткой объяснить структуру комплексных соединений. Эта теория была предложена до открытия электрона
Томсоном
в 1896 году, и до разработки электронной теории валентности
. Вернер не имел в своём распоряжении никаких инструментальных методов исследований, а все его исследования были сделаны интерпретацией простых химических реакций
.

Представления о возможности существования «дополнительных валентностей», зародившиеся при изучении четвертичных аминов
, Вернер применяет и к «комплексным соединениям». В статье «К теории сродства и валентности», опубликованной в 1891 г., Вернер определяет сродство как «силу, исходящую из центра атома
и равномерно распространяющуюся во всех направлениях, геометрическое выражение которой, таким образом, представляет собой не определённое число основных направлений, а сферическую поверхность».
Два года спустя в статье «О строении неорганических соединений» Вернер выдвинул координационную теорию, согласно которой в неорганических молекулярных соединениях центральное ядро
составляют комплексообразующие атомы. Вокруг этих центральных атомов расположено в форме простого геометрического полиэдра
определённое число других атомов или молекул
. Число атомов, сгруппированных вокруг центрального ядра, Вернер назвал координационным числом
. Он считал, что при координационной связи существует общая пара электронов
, которую одна молекула или атом отдает другой. Поскольку Вернер предположил существование соединений, которые никто никогда не наблюдал и не синтезировал
, его теория вызвала недоверие со стороны многих известных химиков, считавших, что она без всякой необходимости усложняет представление о химической структуре и связях. Поэтому в течение следующих двух десятилетий Вернер и его сотрудники создавали новые координационные соединения, существование которых предсказывалось его теорией. В числе созданных ими соединений были молекулы, обнаруживающие оптическую активность
, то есть способность отклонять поляризованный свет
, но не содержащие атомов углерода
, которые, как полагали, были необходимы для оптической активности молекул.
В 1911 г. осуществление Вернером синтеза более чем 40 оптически активных молекул
, не содержащих атомов углерода
, убедило химическое сообщество в справедливости его теории.
В 1913 г. Вернеру была присуждена Нобелевская премия
по химии «в знак признания его работ о природе связей атомов в молекулах, которые позволяли по-новому взглянуть на результаты ранее проведённых исследований и открывали новые возможности для научно-исследовательской работы, особенно в области неорганической химии
». По словам Теодора Нордстрема
, который представлял его от имени Шведской королевской академии наук, работа Вернера «дала импульс развитию неорганической химии», стимулировав возрождение интереса к этой области после того, как она какое-то время пребывала в забвении.
Комплексное соединение
— химическое вещество
, в состав которого входят комплексные частицы. В настоящее время строгого определения понятия «комплексная частица» нет. Обычно используется следующее определение.
Комплексная частица
, координационная частица
— сложная частица, способная к самостоятельному существованию в кристалле
или растворе
, образованная из других, более простых частиц, также способных к самостоятельному существованию. Иногда комплексными частицами называют сложные химические частицы, все или часть связей в которых образованы по донорно-акцепторному механизму
.
Комплексообразователь
— центральный атом
комплексной частицы. Обычно комплексообразователь — атом элемента
, образующего металл
, но это может быть и атом
кислорода
, азота
, серы
, иода
и других элементов, образующих неметаллы
. Комплексообразователь обычно положительно заряжен и в таком случае именуется в современной научной литературе металлоцентром
; заряд комплексообразователя может быть также отрицательным или равным нулю.
Лиганды
(Адденды)
— атомы или изолированные группы атомов, располагающиеся вокруг комплексообразователя. Лигандами могут быть частицы, до образования комплексного соединения представлявшие собой молекулы (H 2
O, CO, NH 3
и др.), анионы (OH −
, Cl −
, PO 4
3−
и др.), а также катион водорода H +
.
Внутренняя сфера
комплексного соединения — центральный атом со связанными с ним лигандами, то есть, комплексная частица.
Внешняя сфера
комплексного соединения — остальные частицы, связанные с комплексной частицей ионной или межмолекулярными связями
, включая водородные
.
Дентатность лиганда
определяется числом координационных мест, занимаемых лигандом в координационной сфере комплексообразователя. Различают монодентатные (унидентатные) лиганды, связанные с центральным атомом через один из своих атомов, то есть одной ковалентной связью, бидентатные (связанные с центральным атомом через два своих атома, то есть, двумя связями), три- , тетрадентатные и т. д.
Координационный полиэдр
— воображаемый молекулярный многогранник, в центре которого расположен атом-комплексообразователь, а в вершинах — частицы лигандов, непосредственно связанные с центральным атомом.
Координационное число
(КЧ)
— число связей, образуемых центральным атомом с лигандами.
Для комплексных соединений с монодентантными лигандами КЧ равно числу лигандов, а в случае полидентантных лигандов — числу таких лигандов, умноженному на дентатность.
Теория кристаллического поля
В
свободном атоме d-элемента
подуровень (n–1)d
пятикратно вырожден, т.е. все пять
(n–1)d-АО
имеют одинаковую энергию. Под воздействием
электростатического поля лигандов
энергия пяти (n–1)d-АО
комплексообразователя дифференцируется
и пятикратное вырождение снимается.
При
октаэдрическом расположении лигандов
вокруг центрального атома наибольшее
отталкивание испытывают электроны,
находящиеся на орбиталях d z
2
и d x
2 -y
2
, направленных к лигандам, поэтому их
энергия будет более высокой, чем у
электронов, находящихся на орбиталях
d xy
,d xz
,d yz
,
расположенных между лигандами. Таким
образом, если в свободном или находящемся
в сферическом поле пять d-орбиталей
имеют одинаковую энергию, то в
октаэдрическом поле лигандов они
разделяются на две группы с разными
энергиями — происходит расщепление на
два энергетических подуровня: более
высокий e g
(соответствует орбиталям d z
2,d x
2 -y
2
) и более низкий t 2g
(
соответствует орбиталям d xy
,d xz
,d yz
).
Следовательно, вырождение пяти d
–орбиталей иона снимается частично,
что приводит к образованию двукратно
вырожденного уровня e g
и трёхкратно вырожденного уровня t 2g
.
Разница в энергиях
уровней e g
и t 2g
называется энергией расщепления .
Величина
расщепления зависит от природы лиганда,
что определяется положением лиганда в
спектрохимическом ряду, определяемым
экспериментально:
I
<
Br
<
SCN
—
<
Cl
<
NO
3
—
<
F
<
OH
<
ONO
—
<
C
2
O
4
2
<
H
2
O
< NCS
< CH
3
CN
< NH
3
< глицин < пиридин < этилендиамин<
NC
—
< NO
 2
2
< CN
< CO.
Принято
считать, что левее аммиака в спектрохимическом
ряду располагаются лиганды “слабого
поля”, а правее — лиганды “сильного
поля”, дающие при прочих равных условиях
большую величину расщепления.
#
#
#
#
#
#
#
Изомерия координационных соединений
В статистическом аспекте стереохимии
центральным оказывается явление изомерии
координационных соединений.
Свойство изомерии химических соединений
было известно ещё при разработке классической
теории химического строения
.
Изомерия молекул открыта
в 1823 г. Ю. Либихом
, обнаружившим, что серебряная соль гремучей кислоты
и изоцианат серебра имеют один и тот же элементный состав, но разные физические и химические свойства.
Под изомерией понимают способность к разному взаимному расположению атомов
и атомных фрагментов в соединениях одинакового общего состава, диктующую отличия в химических и физических свойствах соответствующих соединений — изомеров
. В случае координационных соединений указанные различия могут быть связаны как со спецификой расположения лигандов
во внутренней координационной сфере, так и с распределением лигандов между внутренней и внешними сферами.
Изомерия прямо связана с наличием или отсутствием в соединении тех или иных элементов симметрии: поворотных осей, зеркально-поворотных осей, центра и плоскостей симметрии.
Стереохимическая конфигурация
характеризует относительное пространственное расположение атомов или групп атомов в молекуле
химического соединения. Смысл этого термина зависит от конкретного пространственного расположения атомов в структуре комплекса. Его используют для описания фигуры или многогранника вместе с дополнительным определением, характеризующим специфику пространственного расположения атомов. Так, можно говорить о цис- или транс-конфигурации; D (d), L(l), DL (dl) — соответственно право-, левовращающая конфигурация, рацемат
.
Существуют изомеры двух типов:
1) соединения, в которых состав внутренней сферы и строение координированных лигандов идентичны ( геометрические
, оптические, конформационные, координационного положения);
2) соединения, для которых возможны различия в составе внутренней сферы и строении лигандов (ионизационные, гидратные, координационные, лигандные).
Пространственная (геометрическая) изомерия
Этот вид изомерии
вызван неодинаковым размещением лигандов во внутренней сфере относительно друг друга. Необходимым условием геометрической изомерии является наличие во внутренней координационной сфере не менее двух различных лигандов. Геометрическая изомерия проявляется преимущественно у комплексных соединений, имеющих октаэдрическое строение, строение плоского квадрата или квадратной пирамиды. С увеличением числа различных лигандов во внутренней сфере растет число геометрических изомеров.
Оптическая изомерия связана со способностью некоторых комплексных соединений существовать в виде двух форм, не совмещаемых в трехмерном пространстве и являющихся зеркальным отображением друг друга, как левая рука и правая. Поэтому оптическую изомерию называют иногда ещё зеркальной изомерией.
Природа химических связей в комплексных соединениях.
В настоящее время для объяснения
химических связей в комплексных
соединениях используют метод
валентных связей (ВС)
. Исходя из
метода ВС, предполагается, что между
лигандом и комплексообразователем
возникает донорно-акцепторная связь
за счет неподеленной пары электронов
лиганда и свободной орбитали центрального
иона. Таким образом, лиганд является
донором, а комплексообразователь —
акцептором.
Была установлена связь между строением
молекулы и координационным числом.
Если координационное число равно двум,
то это говорит о том, что комплексообразователь
предоставляет 2 свободные sиp– гибридные орбитали
не поделенным парам лигандов, и комплекс
приобретает линейную структуру.





кч = 2 s + p = 2q +
= 2
Если координационное число равно
четырем, то это говорит о том, что
комплексообразователь предоставляет
свободные 1sи 3p– гибридные орбитали не поделенным
парам лигандов, и комплекс приобретает
тетраэдрическую структуру.
кч = 4 s + 3p = 4q
Если координационное число равно шести,
то это говорит о том, что комплексообразователь
предоставляет свободные 1s,
3pи 2d–
гибридные орбитали не поделенным парам
лигандов, и комплекс приобретает
октаэдрическую структуру.
кч = 6 s + 3p +2d = 6q
Структура и стереохимия
Строение комплексных соединений рассматривают на основе координационной теории
, предложенной в 1893 г
. швейцарским химиком Альфредом Вернером
, лауреатом Нобелевской премии
. Его научная деятельность проходила в Цюрихском университете. Ученый синтезировал много новых комплексных соединений, систематизировал ранее известные и вновь полученные комплексные соединения и разработал экспериментальные методы доказательства их строения.
В соответствии с этой теорией в комплексных соединениях различают комплексообразователь, внешнюю и внутреннюю сферы. Комплексообразователем
обычно является катион
или нейтральный атом
. Внутреннюю сферу
составляет определённое число ионов
или нейтральных молекул
, которые прочно связаны с комплексообразователем. Их называют лигандами
. Число лигандов определяет координационное число (КЧ) комплексообразователя. Внутренняя сфера может иметь положительный, отрицательный или нулевой заряд.
Остальные ионы, не разместившиеся во внутренней сфере, находятся на более далеком расстоянии от центрального иона, составляя внешнюю координационную сферу
.
Природа связи между центральным ионом (атомом) и лигандами может быть двоякой. С одной стороны, связь обусловлена силами электростатического притяжения. С другой — между центральным атомом и лигандами
может образоваться связь по донорно-акцепторному механизму
по аналогии с ионом аммония
. Во многих комплексных соединениях связь между центральным ионом (атомом) и лигандами обусловлена как силами электростатического притяжения
, так и связью, образующейся за счёт неподеленных электронных пар лигандов и свободных орбиталей комплексообразователя.
Комплексные соединения, имеющие внешнюю сферу, являются сильными электролитами
и в водных растворах
диссоциируют
практически нацело на комплексный ион и ионы внешней сферы.
При обменных реакциях комплексные ионы переходят из одних соединений в другие, не изменяя своего состава.
Наиболее типичными комплексообразователями являются катионы d-элементов. Лигандами могут быть:
а) полярные молекулы — NH 3
, Н 2
О, CO, NO;
б) простые ионы — F −
, Cl −
, Br −
, I −
, H +
;
в) сложные ионы — CN −
, SCN −
, NO 2
−
, OH −
.
Для описания взаимосвязи пространственного строения комплексных соединений и их физико-химических свойства используются представления стереохимии
. Стереохимический подход — удобный прием представления свойств вещества в части влияния того или иного фрагмента структуры вещества на свойство.
Объекты стереохимии — комплексные соединения, органические вещества
, высокомолекулярные
синтетические и природные соединения. А. Вернер, один из основоположников координационной химии, приложил большие усилия к развитию неорганической стереохимии. Именно стереохимия является центральной в этой теории, до сих пор остающийся ориентиром в координационной химии.
Устойчивость комплексных соединений.
Внешняя и внутренняя сферы комплексных
соединений сильно различаются по
устойчивости. Частицы, находящиеся во
внешней сфере комплекса легко отщепляются
(диссоциируют) – первичная диссоциация.
Она протекает полностью, как у сильных
электролитов.
Лиганды, находящиеся во
внутренней сфере комплекса, прочно
связаны с комплексообразователем,
отщепляться будут в меньшей степени.
Процесс будет идти обратимо. Обратимый
распад внутренней сферы – вторичная
диссоциация. Она подчиняется закону
действующих масс и характеризуется
константой равновесия, называемой константой нестойкости комплексного
иона — К
н
.
Чем
меньше величина константы нестойкости,
тем устойчивее комплекс.
Существует величина
обратная константе нестойкости — константа устойчивости комплексного
иона – К
уст
.
По значению константы устойчивости
можно рассчитать стандартную энергию
Гиббса образования комплекса.
Окраска комплексных соединений зависит от типа лигандов
и комплексообразователя. Из-за расщепления энергии d-орбиталей появляется возможность перехода электронов
с подуровней d xy
,
d zy
, d xz
на вакантные подуровни с более высокой энергией d z 2
,d z 2
-y 2
под действием поглощаемых квантов света. Эти явления можно наблюдать с помощью электронной спектроскопии
. В зависимости от разности расщепленных уровней комплексы поглощают кванты
света определённых диапазонов длин волн
, поэтому имеют соответствующую окраску.
Среди химических соединений, в том числе комплексных, различают парамагнитные и диамагнитные, по-разному взаимодействующие с внешним магнитным полем
. Парамагнитные комплексы
обладают моментом
µ и поэтому при взаимодействии с внешним магнитным полем втягиваются в него. Напротив, диамагнитные комплексы
, не имея собственного магнитного момента, выталкиваются из внешнего магнитного поля. Парамагнитные свойства веществ
обусловлены наличием в их структуре неспаренных электронов
и в случае комплексов объясняются специфическим заполнением электронами энергетических уровней.
Существуют два принципа, определяющих заполнение электронами
d-орбиталей, расщепленных на dε и dγ -подуровни.
1. Электроны заполняют орбитали так, чтобы число неспаренных электронов было максимальным ( правило Хунда
).
2. Сначала заполняются орбитали, имеющие меньшую энергию
.
С учетом этих правил при числе d-электронов в комплексообразователе от 1 до 3 или 8, 9, 10 их можно расположить по d-орбиталям только одним способом (в соответствии с правилом Хунда). При числе электронов
от 4 до 7 в октаэдрическом комплексе возможно либо занятие орбиталей
, уже заполненных одним электроном, либо заполнение свободных dγ -орбиталей более высокой энергии. В первом случае потребуется энергия на преодоление отталкивания между электронами, находящимися на одной и той же орбитали, во втором — для перехода на орбиталь более высокой энергии. Распределение электронов по орбиталям зависит от соотношения между величинами энергий расщепления
(Δ) и спаривания электронов (Р). При низких значениях Δ («слабое поле»), величина Δ может быть < Р, тогда электроны займут разные орбитали, а спины
их будут параллельны. При этом образуются внешнеорбитальные (высокоспиновые) комплексы, характеризующиеся определённым магнитным моментом µ. Если энергия межэлектронного отталкивания меньше, чем Δ («сильное поле»), то есть Δ > Р, происходит спаривание электронов на dε -орбиталях и образование внутриорбитальных (низкоспиновых) комплексов, магнитный момент которых µ = 0. Величину магнитного момента комплекса можно определить путем измерения зависимости его магнитной восприимчивости
от температуры
. При более точном анализе магнитной восприимчивости комплекса необходимо также учесть диамагнитные поправки, которые образуются от всех атомов, входящих в состав его молекулы. Эти поправочные коэффициенты называются константами Паскаля
.
Метод валентных связей
Согласно
представлениям метода ВС химическая
связь в комплексных соединениях носит
донорно-акцепторный характер. Свободные
электронные пары, которыми обладают
лиганды, заполняют пустые орбитали
центрального иона. Эти орбитали объединяют
в гибридные комбинации в зависимости
от координационного числа (к.ч.).
Комплексные
соединения с к.ч., равным двум, описываются,
как правило, с позиции sp-гибридизации.
Примерами являются комплексные соединения
Ag
(I);
Cu
(I);
Au
(I).
Рассмотрим комплексный ион AgCl 2
–
.
Электронная конфигурация иона Ag +
4d 10
,
орбитали 5s,
5p,
5d,
5f
и 5g
пустые. Самые низкие по энергии из них
5s
и 5p.
Именно туда “селятся” две электронные
пары от двух анионов хлора:

Таким
образом, рассматриваемый комплекс
описывается с позиции sp-гибридизации,
ион серебра и два аниона хлора расположены
на прямой.
Комплексные
соединения с к.ч., равным трём, обычно
описываются исходя из sp 2
-гибридизации,
например, Ag(CN) 3
2–
.
Три аниона CN –
расположены вокруг катиона Ag +
по вершинам правильного треугольника.
В
качестве примеров комплексных соединений
с к.ч., равным четырём, рассмотрим два
комплекса никеля (II):
NiF 4
2–
;
Ni(CN) 4
2–
.
Электронная “макушка” иона Ni 2+
– 3d 8
,
более высокие по энергии орбитали пусты:

Как
видно, возможны два варианта – заполнение
электронными парами лигандов только
пустых орбиталей и освобождение одной
3d-орбитали за счёт спаривания электронов
с последующим заполнением её электронной
парой лиганда, а затем – заполнение
пустых орбиталей. Очевидно, всё будет
определяться энергетическим балансом
– выигрышем в энергии, связанным с
образованием связи (Е св
),
и энергетическим проигрышем, равным
энергии образования электронной пары
из неспаренных электронов (Е пары
).
Если Е пары
> Е св
,
то спиновое состояние центрального
иона в комплексе останется тем же, что
и у свободного иона. В случае, если Е св
> Е пары
,
происходит образование пары и освобождение
одной орбитали в 3d-оболочке.
Всё будет определяться прочностью связи
лиганд–центральный ион. На практике
Е св
> Е пары
в случае только цианидных комплексов
двухзарядных центральных ионов, а для
комплексов с трёхзарядным ионом –
комплексообразователем со следующими
лигандами: CN –
,
NO 2
–
,
NH 3
.
Вернёмся
к рассматриваемым комплексным ионам.
Для NiF 4
2–
Е пары
> Е св
и электронное состояние центрального
иона останется неизменным:

Связь
в комплексном анионе характеризует
sp 3
-гибридизация,
комплексный ион имеет тетраэдрическое
строение и характеризуется высоким
значением спина.
Для
цианидного комплексного аниона Е св
> Е пары
,
электроны “загоняются” в пару, и
освободившаяся орбиталь будет занята
парой электронов:

Химическую
связь в этом комплексе описываем с
позиций dsp 2
-гибридизации,
комплексный анион имеет квадратное
строение и характеризуется низким
спином.
В
связи со спиновым состоянием рассматриваемых
частиц напомним, что наличие или
отсутствие неспаренных электронов
имеет отношение к магнитным характеристикам
веществ. Ферромагнитные вещества мощно
взаимодействуют с магнитным полем; это
в первую очередь железо, кобальт, никель
и комбинации на их основе. Парамагнитные
вещества слабо реагируют на магнитное
поле, фактически отзываются на него.
Частицы парамагнитных веществ содержат
в своём составе неспаренные электроны.
Наконец, диамагнитные вещества вообще
безразличны к магнитному полю. Частицы,
составляющие такие вещества (атомы,
молекулы, ионы), не содержат неспаренных
электронов. Перечисленные выше комплексные
анионы (кроме NiF 4
2–
)
являются диамагнетиками. Ион NiF 4
2–
обладает парамагнитными свойствами.
Парамагнетизм является основой
физико-химического метода – электронного
парамагнитного резонанса (ЭПР),
позволяющего изучать функциональные
особенности вещества.
Для
описания химической связи в комплексах
с к.ч., равным пяти, как правило, привлекают
представления о dsp 3
-гибридизации.
Рассмотрим в качестве примера не совсем
традиционное комплексное соединение
– пентакарбонил железа Fe(CO) 5
.
Карбонилы – соединения металлов с
оксидом углерода (II)
могут рассматриваться, по крайней мере,
в отношении химической связи, как
своеобразные комплексные соединения.
При этом, говоря о карбонилах и других
соединениях с СО, следует иметь в виду,
что это очень сильные лиганды, дающие
прочную химическую связь.

Химическая
связь в молекуле Fe(CO) 5
описывается с позиции dsp 3
-гибридизации,
молекула имеет форму тригональной
бипирамиды, она диамагнитна.


Связь
характеризуется sp 3
d 2
-гибридной
комбинацией орбиталей; для того, чтобы
показать, что задействованы внешние
d-орбитали,
говорят о “внешней” гибридизации.
Комплексный катион имеет октаэдрическое
строение и является парамагнитным.
В
случае цианидного комплекса Е св
> Е пары
,
поэтому шесть 3d-электронов
займут три орбитали, а остальные две
будут заполняться электронами лигандов:

Тип
гибридизации орбиталей будет таким же,
что и в предыдущем случае, однако здесь
задействованы внутренние d-орбитали,
поэтому говорят о “внутренней”
гибридизации. Комплексный анион имеет
октаэдрическое строение и является
диамагнитным.
Соседние файлы в папке Разное4
- #
Практикум по физической химии.djv
- #
- #
- #
- #
- #
1) В названии комплексного соединения первым указывают отрицательно заряженную часть — анион
, затем положительную часть — катион
.
2) Название комплексной части начинают с указания состава внутренней сферы. Во внутренней сфере прежде всего называют лиганды
— анионы, прибавляя к их латинскому названию окончание «о». Например: Cl −
— хлоро, CN −
— циано, SCN −
— тиоцианато, NO 3
−
— нитрато, SO 3
2−
— сульфито, OH −
— гидроксо и т. д. При этом пользуются терминами: для координированного аммиака
— аммин, для воды
— аква, для оксида углерода(II)
— карбонил.
3) Число монодентатных лигандов
указывают греческими числительными: 1 — моно (часто не приводится), 2 — ди, 3 — три, 4 — тетра, 5 — пента, 6 — гекса. Для полидентатных лигандов
(например, этилендиамин, оксалат) используют бис-, трис-, тетракис- и т. д.
4) Затем называют комплексообразователь, используя корень его латинского названия и окончание -ат, после чего римскими цифрами указывают (в скобках) степень окисления
комплексообразователя.
5) После обозначения состава внутренней сферы называют внешнюю сферу.
6) В названии нейтральных комплексных частиц комплексообразователь указывается в именительном падеже
, а степень его не указывается, так как она однозначно определяется, исходя из электронейтральности комплекса.
- Ахметов Н. С.
Общая и неорганическая химия. — М.: Высшая школа, 2003. — 743 с. - Глинка Н. Л.
Общая химия. — М.: Высшая школа, 2003. — 743 с. - Киселев Ю. М.
Химия координационных соединений. — М.: Интеграл-Пресс, 2008. — 728 с. - Ершов.
Общая химия. — Издание восьмое,стериотипное. — Москва: Высшая школа, 2010. — 560 с.
- Гальванические покрытия — защита одного металла другим. Комплексные соединения цианидов имеют важное значение в гальванопластике
, так как из обычной соли бывает невозможно получить настолько прочное покрытие, как при использовании комплексных соединений. - Электролитическое получение металлов. Например, алюминий в расплаве криолита образует комплекс Nа3[AlF6]. Из расплавов соединений комплексных солей получают такие металлы, как Nb, Tl, Th, Mg.
- Защита металлов от коррозии. Ингибиторы
— комплексные соли, где лигандами выступают и органические вещества. - Аналитическая химия
. Многие индикаторы
, реактивы, которые помогают распознать вещества, ионы и даже заряды ионов, — комплексные соединения. - Многие комплексные соединения обладают каталитической активностью существенно более высокой, чем соответствующие металлы в чистом виде, а их растворимость обеспечивает необходимую доступность атома катализатора в совершенно иных температурных условиях, нежели металл в твёрдой фазе. Поэтому их широко используют в неорганическом и органическом синтезах. Таким образом, с использованием комплексных соединений связана возможность получения многообразных химических продуктов: лаков
, красок
, фотоматериалов
и т. д. - Получение и очистка металлов.
- Химические методы извлечения металлов
из руд
связаны с образованием КС. Например, для отделения золота от породы руду обрабатывают раствором цианида натрия
в присутствии кислорода
. - Для получения чистых железа
, никеля
, кобальта
используют термическое разложение карбонилов металлов
. Эти соединения — летучие жидкости, легко разлагающиеся с выделением соответствующих металлов.
- Химические методы извлечения металлов
- Важнейшие органические соединения — гемоглобин
и хлорофилл
— тоже соединения комплексные, они представляют собой порфириновое кольцо с ионом металла в центре. - Синтез многих лекарственных препаратов, витаминов, биодобавок и многих других веществ связан с комплексными соединениями.
Типы комплексных соединений
Существует несколько типов комплексных соединений, в основу которых положены различные принципы.
По заряду комплекса
1) Катионные комплексы
образованы в результате координации вокруг положительного иона
нейтральных молекул (H 2
O, NH 3
и др.).
2) Анионные комплексы
: в роли комплексообразователя выступает ион с положительной степенью окисления
, а лигандами являются простые или сложные анионы.
3) Нейтральные комплексы
образуются при координации молекул вокруг нейтрального атома, а также при одновременной координации вокруг положительного иона
— комплексообразователя отрицательных ионов
и молекул
.
По числу мест, занимаемых лигандами в координационной сфере

, образованного катионом металла и анионом ЭДТА
1) Монодентатные лиганды
. Такие лиганды бывают нейтральными (молекулы Н 2
О, NH 3
, CO, NO и др.) и заряженными ( ионы
CN −
, F −
, Cl −
, OH −
, SCN −
, и др.).
2) Бидентатные лиганды
. Примерами служат лиганды: ион аминоуксусной кислоты
H 2
N — CH 2
— COO −
, оксалатный
ион −
O — CO — CO — O −
, карбонат-ион СО 3
2−
, сульфат-ион SO 4
2−
, тиосульфат-ион S 2
O 3
2−
.
3) Полидентатные лиганды
. Например, комплексоны
— органические лиганды, содержащие в своём составе несколько групп −С≡N
или −COOH
( этилендиаминтетрауксусная кислота
— ЭДТА). Циклические комплексы, образуемые некоторыми полидентатными лигандами, относят к хелатным
( гемоглобин
и др.).
![цис-[CoCl2(NH3)4]+](https://upload.wikimedia.org/wikipedia/commons/thumb/b/be/Cis-dichlorotetraamminecobalt%28III%29.png/132px-Cis-dichlorotetraamminecobalt%28III%29.png)
![транс-[CoCl2(NH3)4]+](https://upload.wikimedia.org/wikipedia/commons/thumb/5/56/Trans-dichlorotetraamminecobalt%28III%29.png/150px-Trans-dichlorotetraamminecobalt%28III%29.png)
![Гран- (fac-) граневой-[CoCl3(NH3)3]](https://upload.wikimedia.org/wikipedia/commons/thumb/6/69/Fac-trichlorotriamminecobalt%28III%29.png/109px-Fac-trichlorotriamminecobalt%28III%29.png)
![Ос- (mer-) реберный-[CoCl3(NH3)3]](https://upload.wikimedia.org/wikipedia/commons/thumb/5/54/Mer-trichlorotriamminecobalt%28III%29.png/136px-Mer-trichlorotriamminecobalt%28III%29.png)
![Λ-[Fe(ox)3]3−](https://upload.wikimedia.org/wikipedia/commons/thumb/d/df/Delta-tris%28oxalato%29ferrate%28III%29-3D-balls.png/110px-Delta-tris%28oxalato%29ferrate%28III%29-3D-balls.png)
![Δ-[Fe(ox)3]3−](https://upload.wikimedia.org/wikipedia/commons/thumb/6/6e/Lambda-tris%28oxalato%29ferrate%28III%29-3D-balls.png/111px-Lambda-tris%28oxalato%29ferrate%28III%29-3D-balls.png)
![Λ-цис-[CoCl2(en)2]+](https://upload.wikimedia.org/wikipedia/commons/thumb/1/12/Delta-cis-dichlorobis%28ethylenediamine%29cobalt%28III%29.png/78px-Delta-cis-dichlorobis%28ethylenediamine%29cobalt%28III%29.png)
![Δ-цис-[CoCl2(en)2]+](https://upload.wikimedia.org/wikipedia/commons/thumb/8/81/Lambda-cis-dichlorobis%28ethylenediamine%29cobalt%28III%29.png/78px-Lambda-cis-dichlorobis%28ethylenediamine%29cobalt%28III%29.png)
