Вале́нтность (от лат. — сила) — способность атомов образовывать определенное количество химических связей, которые образует атом, или число атомов, которое может присоединить или заместить атом данного элемента.
Эдуард Франкленд — основоположник современных представлений о валентности
Решающую роль в создании теории валентности сыграл Фридрих Август Кекуле. В 1857 году он показал, что углерод является четырёхосновным (четырёхатомным) элементом, и его простейшим соединением является метан СН4. Уверенный в истинности своих представлений о валентности атомов, Кекуле ввёл их в свой учебник органической химии: основность, по мнению автора — фундаментальное свойство атома, свойство такое же постоянное и неизменяемое, как и атомный вес. В 1858 году взгляды, почти совпадающие с идеями Кекуле, высказал в статье «О новой химической теории» Арчибальд Скотт Купер.
Уже три года спустя, в сентябре 1861-го, А. М. Бутлеров внёс в теорию валентности важнейшие дополнения. Он провёл чёткое различие между свободным атомом и атомом, вступившим в соединение с другим, когда его сродство «связывается и переходит в новую форму». Бутлеров ввёл представление о полноте использования сил сродства и о «напряжении сродства», то есть энергетической неэквивалентности связей, которая обусловлена взаимным влиянием атомов в молекуле. В результате этого взаимного влияния атомы в зависимости от их структурного окружения приобретают различное «химическое значение». Теория Бутлерова позволила дать объяснение многим экспериментальным фактам, касавшимся изомерии органических соединений и их реакционной способности.
Молекулярные модели Гофмана
Огромным достоинством теории валентности явилась возможность наглядного изображения молекулы. В 1860-х годах появились первые молекулярные модели. Уже в 1864 году А. Браун предложил использовать структурные формулы в виде окружностей с помещёнными в них символами элементов, соединённых линиями, обозначающими химическую связь между атомами; количество линий соответствовало валентности атома. В 1865 году А. фон Гофман продемонстрировал первые шаростержневые модели, в которых роль атомов играли крокетные шары. В 1866 году в учебнике Кекуле появились рисунки стереохимических моделей, в которых атом углерода имел тетраэдрическую конфигурацию.
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода — двум, азота — трём, углерода — четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента. Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода — двум, азота — трём, кремния — четырём, серы — шести.
Понятие «валентность»
было введено в науку для отражения
свойств, вполне определенного объекта
– свободного (изолированного) атома
ХЭ. Так, в работах Э. Франкланда (1852-1855),
А. Кекуле (1857-1858) и А. М. Бутлерова (1861-1871)
валентностью
(или атомностью) была названа целочисленная
величина, выражающая количество единиц
сродства свободного атома любого
элемента.
Фридрих Август Кекуле (1829-1896)
— экспериментальные работы Кекуле
относятся к органической химии. В 1854 он
получил тиоуксусную, а в 1856 — гликолевую
кислоту. В 1872 совместно с нидерландским
химиком А. Франшимоном синтезировал
трифенилметан и антрахинон. С целью
проверки гипотезы о равноценности всех
атомов водорода в бензоле он получил
его галоген-, нитро-, амино- и
карбоксипроизводные; занимался также
исследованиями ненасыщенных кислот и
синтетических красителей. Однако
основные работы Кекуле были посвящены
теоретической химии; главной
егозаслугой стало создание теории
валентности.
Валентность
устанавливалась по числу химических
связей, т.е. по следствию. Но путаницы
при этом не возникло, на первых порах.
Например, А. М. Бутлеров указывал, что
число химических связей может быть
меньше валентности: так при образовании
молекулы СО2,
все четыре единицы сродства углерода
участвуют в образовании химической
связи, а в случае образования молекулы
СО связываются лишь две единицы сродства,
а две остаются свободными.
Бутлеров
Александр Михайлович (1828-1886)-
русский химик, академик Петербургской
Академии Наук (с 1874). Создатель теории
химического строения органической
химии. Обосновал идею о взаимном влиянии
атомов в молекуле. Предсказал и объяснил
(1864) изомерию многих органических
соединений. Показал (1862) возможность
обратимой изомеризации, заложив основы
учения о таутомерии. Синтезировал
уротропин (сухой спирт).
Однако
многочисленные случаи совпадения числа
единиц сродства свободного атома и
числа образовавшихся химических связей
привели к отождествлению причины и
следствия. С 1870-х гг. и по сей день
валентностью стали называть чаще всего
«число
химических связей, осуществляемых
атомом при образовании соединений».
Т.е. понятие валентность стало
использоваться для отражения свойств
существенно другого объекта – не
свободного, а связанного
атома,
находящегося в молекуле и изменившего
свои свойства под влиянием других
атомов.
Но и на этом
сложности их не закончились. В конце
XIX
в. в работах Г. Амстронга, С. У.
Пикерлинга, и И. Тиле появились выводы
из обстоятельного эмпирического
материала, свидетельствующие о
существовании нецелочисленной
(или парциальной) валентности связанного
атома. Такая
валентность имела в то время лишь весьма
приблизительную оценку, не выходящую
за пределы одной единицы сродства.
Примерно в тоже
время А. Вернер выдвинул и обосновал
понятие
координационного числа, идентичное
понятию валентности связанного атома,
но явно альтернативное кекулевскому
понятию валентности.
Координационное число представляло
собой целочисленную величину, как
правило, намного превосходящую кекулевское
число единиц сродства. В результате
всех этих взглядов понятие «валентность»
стало не только «аморфным» «шатким»
(по мнению Д. И. Менделеева, Л. А. Чугаева
и др. химиков), но и неясным по своей
сущности.
Вернер
Альфред (1866–1919) — швейцарский химик.
Основоположник химии
комплексных (координационных) соединений.
Выдвинул и развил (1893) координационную
теорию строения комплексных соединений,
опровергающую представления о постоянстве
чисел валентности. Предсказал
существование оптически активных
изомеров, не имеющих асимметрического
углеродного атома. Нобелевская премия
(1913).
В XX
в. кризис понятия валентности ещё более
углубился. Изучение водородных связей
подорвало авторитет водорода, как
эталона одновалентного элемента.
Открытие сэндвичевых соединений
наделяло, по тому же определению,
некоторые элементы числами валентности
10, 12 и даже 16.
Квантовая химия
дала всем толкованиям валентности свое
обоснование. А историко-логический
анализ развития всего учения о валентности
позволил создать систему понятий
валентности, которую можно представить
следующим образом:
0,838
0,391 0,391 0,838
4. Сущность понятия
«координационное число по Вернеру»
разъяснило посредством представлений
о делокализованных химических связях
в методе МО.
Таким образом,
понятие «валентность» расщепилось на
четыре понятия, отличные друг от друга.
Все четыре понятия являются рабочими
в химии.
- Валентность — что это за способность у атомов
- История возникновения понятия
- Современные представления о валентности
- Чем отличается от степени окисления
- Виды валентности, как определить для химических элементов
- Атомы химических элементов и их валентные возможности
- Чем определяются, какие факторы влияют
- Определение валентности элемента по электронно-графическим формулам
- Селен, углерод, фосфор, сера, азот, хлор и другие примеры
- Элементы, имеющие несколько значений валентности
- Что такое степень окисления
- В чем отличие валентности и степени окисления
- Эволюция понятия «валентность» и его роль в истории химии
- Нахождение стехиометрической валентности
Валентность — что это за способность у атомов
Валентность — это выраженная в числовом виде способность атома химического элемента образовывать химические связи с определенным количеством других атомов.
Валентность записывают римскими цифрами над химическим элементом. Она принимает значения от 1 до 8, не может быть равна нулю.
— атом кислорода образовывает ковалентную связь с двумя атомами водорода. Валентность водорода равна одному, а валентность кислорода — двум.
История возникновения понятия
Термин «валентность» начали использовать около 1425 года — тогда его использовали в значениях «препарат» или «экстракт». В современном понимании его впервые употребили в 1884 году, когда ученые объяснили и описали феномен валентности.
Открытие феномена валентности произошло не сразу. Уильям Хиггинс в 1789 году предположил в своей работе, что между малейшими частицами вещества, т. е. атомами в современной терминологии, существуют связи.
Полную концепцию предложил Эдуард Франкленд, которого считают основоположником представлений о валентности. Это произошло в 1852 году, когда химик ввел понятие «соединительной силы». Свои выводы Франкленд сделал на основе предыдущих работ, а также наблюдений за способностью разных металлов к насыщению. К тому же, он сравнивал составы органических производных металлов с неорганическими соединениями. Так он установил частные закономерности, которые впоследствии послужили основой современного понимания валентности.
В 1857 годуФридрих Август Кекуле показал четырехвалентный характер углерода и установил, что простейшее соединение углерода — это метан
. Кекуле посчитал «валентность» фундаментальным неизменным свойством атома, как, например, атомный вес. Похожие взгляды изложил в 1858 году в своей статье Арчибальд Скотт Купер.
Всего три года спустя, в 1861 А. М. Бутлеров сформулировал основу современной теории валентности. Он установил различия между свободными атомами и атомами в соединении, а также обнаружил, что «химическое значение» атомов, т. е. их валентность, в разных соединениях может быть разной.
Впоследствии ученые обобщили знания о валентности и сформировали полную систему знаний по этой теме.
Современные представления о валентности
Как показывает история возникновения понятия «валентность», теория химической связи прошла через долгую эволюцию.
В современной науке валентность в соединениях с ковалентной связью определяется как число двухэлектронных двухцентровых связей. При этом к соединениям с ионной кристаллической структурой применять понятие валентность некорректно из-за характера связи в них. Химическая связь в таких вещества формируется не за счет образования общих электронных пар.
В неорганической химии понятие валентности используется нечасто, оно более распространено в органической химии. В неорганической более распространено понятие степень окисления, т. к. большинство неорганических веществ, в отличие от органических, имеет немолекулярное строение.
Чем отличается от степени окисления
Степень окисления (СО) — это условный заряд атома химического элемента в соединении и характеристика его поведения в окислительно-восстановительной реакции.
Особенность степени окисления в том, что в простых соединениях она всегда равна нулю. В сложных веществах СО определяют на основе постоянных степеней окисления составляющих элементов.
При определении СО элементов в бинарном веществе одному элементу приписывают условный положительный заряд «+», а другому условный отрицательный заряд «−». Так происходит, поскольку электроны связи смещаются от менее электроотрицательных элементов к более электроотрицательным, в результате атомы приобретают частичные заряды.
Электроотрицательность — это способность атома притягивать к себе электроны.
Более электроотрицательный элемент притягивает электроны и получает знак «−», поскольку электроны — отрицательно заряженные частицы. Менее электроотрицательный элемент отдает электроны и становится положительно заряженным.
Таким образом, понятия валентность и степень окисления родственны, но не тождественны. С О обозначает условный электрический заряд атома, если считать, что электроны полностью переходят от более электроотрицательного атома к менее электроотрицательному. Валентность характеризует количество общих электронных пар, которые может образовать атом.
Еще одно различие заключается в том, что степень окисления может быть положительной, отрицательной, равной нулю и даже дробной величиной. А валентность — это целое положительное число.
Валентность и степень окисления можно определить у элемента в одном и том же веществе. Они могут как совпадать, так и различаться.
Валентность кислотного остатка азотной кислоты
Виды валентности, как определить для химических элементов
Выделяют два вида валентности:
Элементы с постоянной валентностью представлены в сводной таблице ниже.
У элементов с переменной валентностью обычно выделяют два типа валентности:
Высшая валентность обычно равна номеру группы элемента.
Низшую валентность находят как разность между количеством групп в периодической таблице элементов Менделеева (то есть числом 8) и номером группы элемента.
Элементы VII группы основной подгруппы A называют галогенами. В школьном курсе химии в соединениях галогены чаще всего имеют валентность I, но в некоторых соединениях их валентность может быть другой.
Атомы химических элементов и их валентные возможности
В начале прошлого века научная общественность была потрясена открытием британского физика Э. Резерфорда, который в своем докладе «Рассеяние α- и β-лучей и строение атома» говорил об открытии атомного ядра.
Данное открытие в тандеме со знанием о электронах сместило главенствующую тогда теорию о валентности, заменив ее на теорию о химических связях.
Однако понятие о валентности не пропало из научного мира. Вклад в научное развитие этого термина внесли Э. Франкленд, Ф. А. Кекуле и А. М. Бутлеров.
Согласно проделанным открытиям, атомы химических элементов состоят из:
Свойства атомов химических элементов определяет количество электронов на их последнем (внешнем) электронном слое. Именно они участвуют в образовании химических связей разных типов. Такие электроны называются валентными.
Валентность — количество связей образованных атомом при участии его валентных электронов.
Для определения валентных возможностей атома необходимо рассмотреть распределение электронов на его энергетических уровнях.
Только атомы образовавшие химические связи могут характеризоваться понятием валентности.
Валентность обозначают римскими цифрами от I до VIII.
Число валентных электронов или число общих электронных пар определяет валентность.
Понятие валентности сопряжено со степенью окисления и часто совпадает с его значением.
Чем определяются, какие факторы влияют
Валентность атома определяется количеством валентных электронов:
Атомы могут иметь основное и возбужденное состояние, из-за чего большинство химических элементов имеют переменную валентность.
В основном состоянии валентность зависит от неспаренных электронов последнего (иногда и предпоследнего) энергетических уровней. Обычное состояние фиксируется в Периодической таблице Менделеева.
Определение валентности элемента по электронно-графическим формулам
Для определения количества электронов на энергетических уровнях необходимо полагаться на номер и место химического элемента в Периодической системе Д. И. Менделеева.
Определив количество электронов, необходимо распределить их по свободным орбиталям в порядке заполнения по шкале энергии:
В одной ячейке или на одной орбитали могут располагаться либо 1 электрон, либо 2 электрона с противоположными спинами — разными направлениями вращения.
Орбитали разных уровней могу размещать в своих свободных ячейках разное количество электронов:
По количеству электронов, оставшихся неспаренными в ячейках, можно узнать валентность атомов химических элементов. Электронные формулы обычно записываются не полностью, а в кратком варианте, указывая только крайние электронные уровни каждого слоя.
Можно сформулировать следующие закономерности электронного строения атома:
Селен, углерод, фосфор, сера, азот, хлор и другие примеры
Рассмотрим заполнение электронных уровней на примерах.
Углерод С обладает номером 6 в Периодической системе химических элементов Д. И. Менделеева, соответственно, он обладает 6 электронами.
Они полностью заполняют уровни 1s / 2s и частично уровень 2р. В обычном состоянии углерод обладает валентностью II. Свободная орбиталь 2р подуровня позволяет орбитали 2s распариваться. Тогда валентность углерода может изменяться на IV.
Азот N обладает номером 7 в ПСХЭ Менделеева и 7 электронами.
Они полностью занимают уровни 1s / 2s и частично 2р. В обычном состоянии азот обладает валентностью III. Перейти в возбужденное состояние путем распаривания 2s-электронов атом не способен, так как относится ко второму периоду, а на втором энергетическом уровне больше нет свободных подуровней и орбиталей, способных принять распарившиеся электроны. Максимальная валентность азота равна IV (за счет образования связи, не только по обменному, но и по донорно-акцепторному механизму), валентность V — не достигается.
Особенностью азота является несоответствие его валентности номеру группы ПС. Азот не обладает валентностью равной V, однако обладает соответствующей степенью окисления +5. Н Есоответствие значений валентностей и степеней окисления атомов азота в некоторых его соединениях является еще одной особенностью этого элемента.
Кислород О обладает номером 8 в ПСХЭ Менделеева и 8 электронами. Возбужденного состояния у кислорода так же нет.
Электроны полностью занимают уровни 1s / 2s и частично 2р. Валентность кислорода равна II — постоянная валентность.
Фтор F обладает номером 9 в ПСХЭ Менделеева и 9 электронами. Они полностью занимают уровни 1s / 2s и частично 2р. Фтор обладает только валентностью I, которая не меняется.
Алюминий Al обладает номером 13 в ПСХЭ Менделеева и 13 электронами. Они полностью занимают уровни 1s / 2s, 2p / 3s и частично уровень 3р. Несмотря на электронную конфигурацию основного (стационарного) состояния атома, валентность I практически не встречается. У алюминия постоянная валентность III (из этого следует что энергия перехода в возбужденное состояние для этого элемента не высока и атомы алюминия всегда пребывают именно в возбужденном состояние).
Фосфор P обладает номером 15 в ПСХЭ Менделеева и 15 электронами.
Они полностью заполняют уровни 1s / 2s, 2p / 3s и частично уровень 3р. В обычном состоянии фосфор обладает валентностью III. Распаривание 3s электронов создает возбужденное состояние, в котором пять валентных электронов занимают 5 ячеек, и валентность в таком случае поднимается до V.
Сера S занимает 16 место в ПСХЭ Менделеева и обладает 16 электронами.
Они полностью занимают 1s / 2s, 2p / 3s и частично 3р. В обычном состоянии сера обладает валентностью II. Распаренные электроны могут занимать ячейки подуровня 3d, валентность поднимается до IV и VI.
Хлор Cl обладает номером 17 в ПСХЭ Менделеева и 17 электронами.
Они полностью занимают уровни 1s / 2s, 2p / 3s и частично 3р. В обычном состоянии валентность хлора равна I. В возбужденном состоянии хлор может повышать свою валентность до III, V или VII. Формально данный ХЭ может обладать валентностью IV и VI.
Селен Se обладает номер 34 в ПСХЭ Менделеева, соответственно, он обладает 34 электронами.
Они полностью заполняют уровни 1s / 2s, 2p / 3s, 3p / 4s, 3d, отдав 30 электронов. Еще 4 заполняют орбиталь 4р — (1 ячейка занята полностью, еще 2 содержат по одному электрону). Валентность селена в обычном состоянии равна II.
Однако селен относится к элементам с переменной валентностью, поэтому также может обладать значением валентности IV и VI.
Элементы, имеющие несколько значений валентности
Значение валентности зависит от состояния атома — обычного или возбужденного.
Не все атомы химических элементов могут переходить в возбужденное состояние. По этому признаку они делятся на химические элементы с переменной и постоянной валентностью.
Постоянная валентность наблюдается у щелочных, щелочноземельных металлов, водорода, кислорода, фтора и алюминия.
Все остальные химические элементы обладают переменной валентностью, обусловленными существованием как возбужденных, так и обычных (стационарных) состояний.
Что такое степень окисления
Степень окисления — условная величина электрического заряда атома, входящего в состав химического соединения. Расчет значений этой величины основывается на предположении, что при образовании химической связи происходит полная передача электрона от атома с меньшей электроотрицательностью к атому с большей электроотрицательностью. В результате таких представлений каждому атому можно приписать целочисленный электрический заряд. В неорганической химии степень окисления очень часто совпадает с валентностью.
Степень окисления зачастую не совпадает с реальным значением электрического заряда атома, (совпадение наблюдается только в случае ионных соединений). Она используется лишь для систематизации и классификации химических элементов. Степень окисления широко используется при составлении формул, международных названий элементов, объяснения их окислительно-восстановительных свойств.
Степень окисления указывается как заряд рядом с символом химического элемента, как правый верхний индекс. Сначала указывается знак заряда, затем число (в обозначение реального электрического заряда ионов наоборот). Она равна количеству электронов, которые атом отдает (тогда рядом со значением ставится +), либо присоединяет (тогда ставится знак -).
СО обозначается арабскими цифрами (валентность римскими).
В чем отличие валентности и степени окисления
Валентность и степень окисления не являются равнозначными понятиями, хоть их числовое значение может совпадать.
Валентность используется для определения числа химических связей атома, причем как полярных, так и неполярных.
Степень окисления используется для выражения значения электрического заряда, сосредоточенного на атоме.
Эволюция понятия «валентность» и его роль в истории химии
В начале 19 в.
Дж. Дальтоном
был сформулирован закон кратных
отношений, из которого следовало, что
каждый атом одного элемента может
соединяться с одним, двумя, тремя и т.д.
атомами другого элемента (как, например,
в окислах азота —N2O,
NO, N2O3,
NO2
и N2O5).
В середине 19 в., когда были определены
точные относительные веса атомов (И. Я.
Берцелиус
и др.), стало ясно, что наибольшее число
атомов, с которыми может соединяться
данный атом, не превышает определённой
величины, зависящей от его природы.
Например, атом F может соединяться лишь
с одним атомом Н, О — с двумя, N — с тремя,
С — с четырьмя, образуя соответственно
HF, H2O,
NH3
и CH4.
Два или четыре атома Н в метане CH4
могут быть замещены одним или двумя
атомами О с образованием формальдегида
CH2O
и двуокиси углерода CO2
соответственно, три атома Н в CH4
могут замещаться одним атомом N с
образованием цианистого водорода HCN, и
т.д. Эта способность связывать или
замещать определённое число других
атомов и была названа «Валентность»
(Э. Франкленд,
1853).
В таком
определении валентность, естественно,
всегда выражается целыми числами.
Поскольку в то время для водорода не
были известны соединения, где он был бы
связан более чем с одним атомом любого
другого элемента, атом Н был выбран в
качестве стандарта, обладающего
валентностью, равной 1. В «водородной»
шкале кислород и сера имеют валентность,
равную 2, азот и фосфор 3, углерод и кремний
4. Однако «водородной» шкалы оказалось
недостаточно: в других соединениях,
например в окислах, один и тот же элемент
может реализовать валентности, которые
не осуществляются в гидридах (существуют
окислы P2O5,
SO3
и Cl2O7,
но неизвестны гидриды PH5,
SH6
и ClH7).
В качестве второго стандарта с
валентностью, равной 2, был выбран
кислород.
В конце 50-х гг.
19 в. А. С. Купер
и А. Кекуле
постулировали принцип постоянной
четырёхвалентности углерода в органических
соединениях. Представления о валентности
составили важную часть теории химического
строения А. М. Бутлерова
(1861). Образование химической связи
рассматривалось как результат взаимного
насыщения двухвалентной пары
взаимодействующих атомов (по одной
валентности от каждого), кратные
связи
соответствовали насыщению нескольких
валентностей от каждого атома, и т.д.
Каждая связь считалась локализованной
между двумя атомами и изображалась
одной чертой, соединяющей эти атомы.
Молекулы стали изображать с помощью
структурных формул, получивших особенно
широкое распространение в органической
химии.
Положения
Бутлерова в дальнейшем легли в основу
структурной теории, рассматривающей и
пространственное расположение атомов
в молекуле. Было найдено, что простые
молекулы типа MXk
с одинаковым центральным атомом M и
разными заместителями Х имеют схожее
геометрическое строение. Независимость
геометрического строения от типа связи
в широких пределах привела к мысли, что
пространственное расположение атомов
в молекулах MXk
определяется валентностью центрального
атома М и что эти валентности имеют
направленный характер.
Периодический
закон Д. И. Менделеева (1869) вскрыл
зависимость валентности элемента от
его положения в периодической системе.
Элементы одинаковых групп системы
обладают одинаковой высшей валентностью,
в большинстве случаев равной номеру
той группы, в которой находится этот
элемент; высшая валентность меняется
на 1 при переходе от одной группы к
соседним.
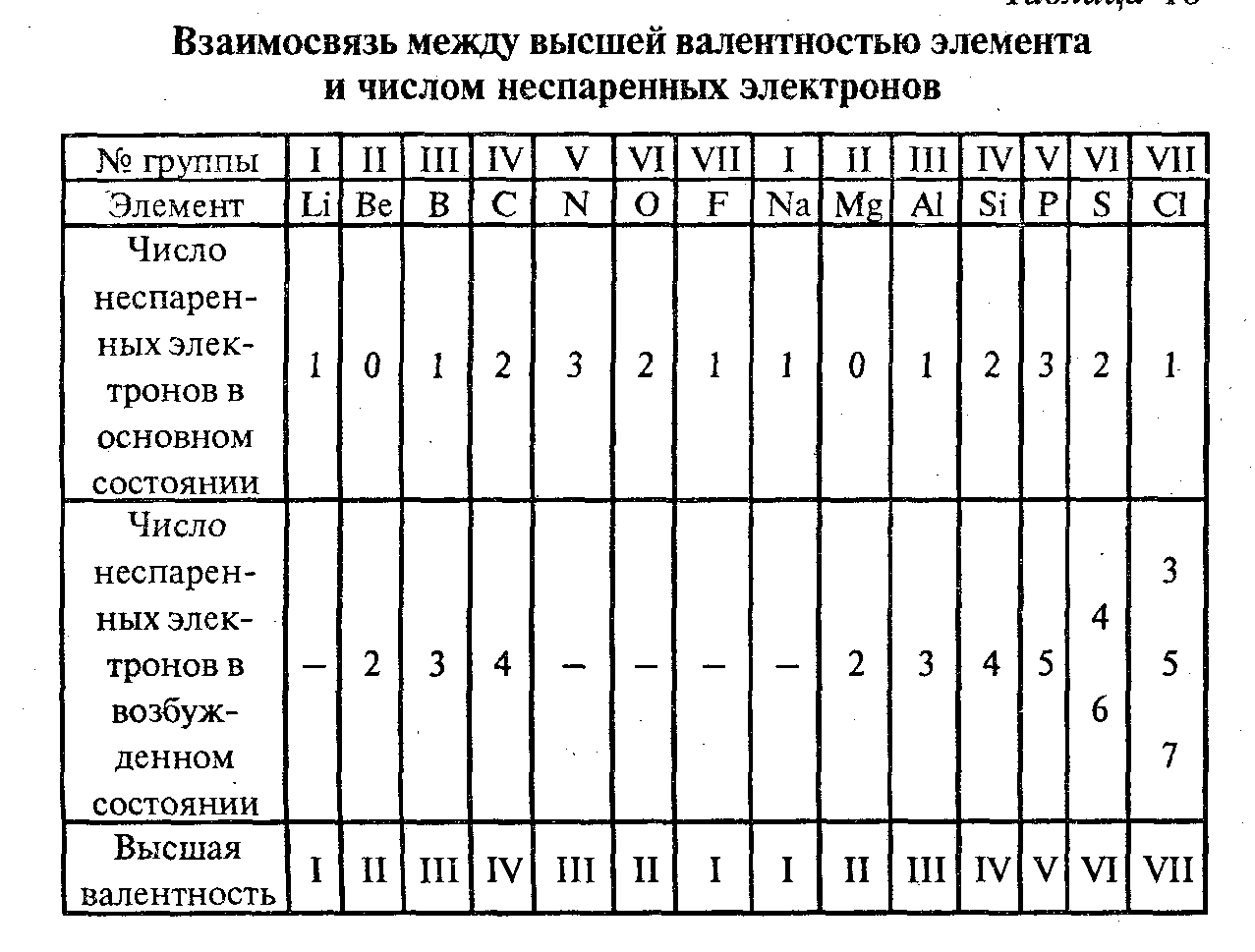
Эта зависимость
сыграла чрезвычайно важную роль в
развитии химии: зная лишь положение
элемента (в том числе элементов, которые
в то время ещё не были открыты) в
периодической системе, можно было
определить его валентные возможности,
предсказать состав его соединений и
впоследствии синтезировать их. С помощью
представлений о формальной
(стехиометрической) валентности химикам
удалось обобщить и систематизировать
огромный экспериментальный материал
по строению, стехиометрическому составу
и свойствам многих десятков и сотен
тысяч органических и неорганических
соединений.
Первые
электронные теории ковалентности и
гетеровалентности.
До электронных представлений о строении
вещества валентность трактовалась
формально. Лишь в 20 в. было установлено,
что химическая связь осуществляется
за счёт электронов внешних (валентных)
оболочек атомов.
В 1916 Г. Льюис
постулировал, что химическая связь
осуществляется парой электронов,
принадлежащих одновременно обоим
взаимодействующим атомам. В 1917 Коссель
выдвинул гипотезу, согласно которой
электронная пара связи переходит целиком
к одному из атомов с образованием ионной
пары катион — анион, удерживающихся в
молекуле электростатическими силами.
Согласно обеим гипотезам наиболее
устойчивыми оказываются соединения, в
которых валентные электроны распределялись
так, чтобы каждый атом был окружен
оболочкой, имитирующей электронную
оболочку ближайшего инертного газа
(правило октета). Гипотеза Льюиса положила
начало электронной теории ковалентной
связи и ковалентности, гипотеза Косселя
— теории ионной связи и гетеровалентности.
Обе представляли крайние случаи общей
картины полярной связи, когда электронная
пара смещена к одному из атомов лишь
частично и степень смещения может
варьироваться от 0 до 1. Валентность
атома в соединении, согласно классической
электронной теории, равна числу его
неспаренных электронов, участвующих в
связях, а максимальная валентность —
обычно полному числу электронов в его
валентной оболочке, то есть номеру
группы периодической системы, в которой
находится элемент. Элементы одинаковых
групп имеют одинаковое число валентных
электронов, а внутри одинаковых подгрупп
— и одинаковые или очень близкие
электронные конфигурации. Сходство
строения валентных оболочек атомов
обусловливает сходство их соединений.
Ковалентность
и гетеровалентность отражают специфику
соответствующего типа химической связи.
Для ковалентности важна насыщаемость
связей, обусловливающая существование
молекул в виде дискретных частиц с
определённым составом и структурой.
Ковалентность эффективна для органических
и большинства простых неорганических
соединений. Напротив, в случае
гетеровалентности максимальное число
ионов противоположного знака, способное
разместиться вокруг данного иона, в
основном определяется соотношениями
их размеров. Ионная валентность эффективна
для сравнительно ограниченного класса
соединений, в основном для различных
солей, щелочных, щёлочноземельных и
некоторых др. металлов.
Сейчас
установлено, что подавляющее большинство
элементов может проявлять переменную
валентность, образуя весь ряд
«валентноненасыщенных» соединений со
всеми значениями валентности от 1 до
максимальной с изменением на 1 (например,
известны молекулы BF, BF2
и BF3;
CF, CF2,
CF3
и CF4
и т.д.). Валентность не может считаться
жестко специфической характеристикой
элемента, можно говорить лишь об
относительной типичности или относительной
устойчивости разных значений валентности.
У непереходных элементов чётных и
нечётных групп наиболее устойчивы
соответственно чётные и нечётные
валентности, например в молекулах типа
PF3,
PF5,
SF2,
SF4,
SF6,
IF, IF3,
IF5,
IF7
и т.д., где типичная валентность атомов
Р, S и I изменяется на 2 единицы.
Радикалы типа
·PF4,
·SF3,
·SF5,
·IF2,
·IF4
и т.д. с четырёхвалентным фосфором,
нечётновалентными аналогами серы и
инертными газами и чётновалентными
галогенами значительно менее стабильны,
обладают отчётливо выраженной склонностью
к отщеплению одного электрона (с
образованием более устойчивых катионов
типа PF4+,
SF3+,
SF5+,
IF2+,
IF4+)
или одного атома заместителя и
характеризуются значительно меньшими
временами существования. У элементов
побочных групп соотношения между
типичными и менее типичными валентностями
имеют более сложный характер.
Изучение
электронных спектров показало, что
двухатомные молекулы типа O2,
S2,
OS и др. имеют два неспаренных электрона;
в рамках классических представлений
это следовало бы интерпретировать так,
будто в подобных молекулах каждый атом
сохраняет неиспользованной одну свою
валентность, хотя нет никаких видимых
препятствий для их использования.
Таким образом,
поиск общего определения валентности,
охватывающего все известные типы
соединений и тем более способного
предсказать возможность или принципиальную
невозможность существования ещё не
известных классов соединений, представляет
сложную проблему. Конечно, параллельно
с «неклассическими» соединениями
химиками были синтезированы многие
сотни тысяч соединений, которые могут
быть интерпретированы в рамках обычных
классических представлений о валентности.
Однако ясно, что все существующие частные
определения валентности ограничены
определёнными классами и типами
соединений, в которых преобладает
какой-либо один тип химического
взаимодействия. В общем же случае связи
имеют промежуточный характер между
чисто ионными и чисто ковалентными, в
них принимают участие все типы
взаимодействия одновременно, но в
различных количественных соотношениях,
резко изменяющихся от класса к классу
и более плавно — от соединения к
соединению внутри одного класса. При
отсутствии общего определения валентности
трудность заключается в том, чтобы
определить границы, где перестаёт быть
справедливым одно частное определение
валентности и его заменяет другое.
Решить эту проблему только на основании
экспериментальных фактов и классических
представлений невозможно. Существенную
помощь здесь может оказать квантовая
теория химической связи и валентности.
Нахождение стехиометрической валентности
где MA — атомная масса элемента, ME — его эквивалентная масса в химическом соединении, V — валентность элемента в данном соединении. Важно, что атомная и эквивалентная массы представляют собой экспериментально измеримые величины, так что стехиометрическую валентность по этой формуле можно рассчитать, в том числе, и для элементов, не образующих гидридов или оксидов, то есть тех элементов, для которых невозможно напрямую определить валентность по водороду или кислороду. Валентность, определяемая по этой формуле, находится по стехиометрическому составу соединения, откуда и название — стехиометрическая валентность. Поскольку при этом руководствуются формальным признаком — формулой химического соединения, то становится ясным и происхождение второго названия — формальная (формульная) валентность.
В соответствии с установленными эмпирически формулами химических соединений были составлены таблицы валентностей элементов. Элементы, стехиометрическая валентность которых всегда равна 1: H, Li, F, Nа, К, Rb, Cs; элементы, стехиометрическая валентность которых всегда равна 2: Be, Mg, Ca, Sr, Ba, Zn; элементы, стехиометрическая валентность которых всегда равна 3: B, Al, Sc, Y, La. Большинство химических элементов обладают переменной стехиометрической валентностью. Так, в оксидах азота, формулы которых приведены выше, стехиометрическая валентность азота изменяется от 1 до 5.
В скобках указаны редко проявляемые значения стехиометрической валентности.
Стехиометрическая валентность химического элемента зависит от его положения в периодической системе. Высшая валентность химического элемента не может превышать номера группы короткой формы периодической системы, в которой этот элемент находится (медь Cu, серебро Ag и золото Au — исключения). Стехиометрическую валентность 8 могут проявлять рутений Ru, осмий Os и ксенон Xe. Низшая валентность равна разности (8 — N), где N — номер группы, в которой находится данный элемент. Валентность элементов по водороду имеет максимальное значение 4, которое достигается элементами IV группы периодической системы. Элементы V—VII групп в своих соединениях с водородом проявляют низшую валентность. В бинарных соединениях низшую валентность проявляет тот элемент, который находится в периодической таблице элементов правее или выше, а высшую валентность — элемент, расположенный левее или ниже. Например, в соединении с кислородом сера проявляет высшую валентность 6, соответственно формула оксида серы (серного ангидрида) SO3. Для неметаллов, как правило, для большей части соединений характерны две валентности — высшая и низшая. Так, сера имеет высшую валентность 6 и низшую (8 — 6) = 2; для фосфора характерны валентности 5 и (8 — 5) = 3.
- Л. Паулинг Природа химической связи. М., Л.: Гос. Н ТИ хим. литературы, 1947.
- Коулсон Ч. Валентность. М.: Мир, 1965.
- Маррел Дж., Кеттл С., Теддер Дж. Теория валентности. Пер. с англ. М.: Мир. 1968. (недоступная ссылка)
С момента возникновения теории химической связи понятие «валентность» претерпело существенную эволюцию. В настоящее время оно не имеет строгого научного толкования, поэтому практически полностью вытеснено из научной лексики и используется, преимущественно, в методических целях.
Резонансная модель образования ковалентных связей в молекуле HNO3
Структурная формула молекулы этана
Особенно это справедливо для молекул с делокализованными химическими связями; например, в азотной кислоте степень окисления азота равна +5, тогда как азот не может иметь валентность выше 4. Известное из многих школьных учебников правило — «Максимальная валентность элемента численно равна номеру группы в Периодической таблице» — относится исключительно к степени окисления. Понятия «постоянной валентности»
и «переменной валентности» также преимущественно относятся к степени окисления.
Семиполярные и донорно-акцепторные (дативные) связи по своей сути являются «двойными» связями, поскольку при их образовании происходят оба процесса: перенос электрона (образование ионной связи) и обобществление электронов (образование ковалентной связи).
Некорректным будет использование валентности для описания соединений с ионной кристаллической структурой. Так в кристалле хлорида натрия NaCl у каждого иона Na+ или Cl− — центра элементарной ячейки — реальное число соседних ионов — координационное число — равно 6, а степень окисления — +1 и −1 соответственно. Локализованных же электронных пар вовсе нет.
V — Стехиометрическая валентность
M — Молекулярная масса (г/моль)
E — Эквивалентная масса (г/моль)
Так, стехиометрическая валентность углерода в CO 12 (г/моль) /6 (г/моль) = 2, а в CO2 12 /3 = 4.
В неорганической химии во многих случаях понятие валентности элемента теряет определённость: эта величина зависит от знания химического строения соединения, во многих случаях она может быть больше номера группы (таблицы ПСХЭ). В неорганической химии обычно применяется понятие степень окисления, а в органической химии — валентность, так как большинство неорганических веществ имеет немолекулярное строение, а органических — молекулярное. Нельзя отождествлять эти два понятия, даже если они численно совпадают. Широко применяется также термин «валентные электроны», то есть наиболее слабо связанные с ядром атома, чаще всего внешние электроны.
По валентности элементов можно составлять истинные формулы соединений, и, наоборот, исходя из истинных формул, можно определять валентности элементов в данных соединениях. При этом необходимо придерживаться принципа, согласно которому произведение валентности одного элемента на число его атомов равно произведению валентности второго элемента на число его атомов. Так, чтобы составить формулу оксида азота (III), следует записать сверху над символом валентности элементов . Определив наименьшее общее кратное и разделив его на соответствующие валентности, получим атомное соотношение азота к кислороду, а именно 2 : 3. Следовательно, формула оксида азота (III) соответствует . Для определения валентности поступают таким же образом наоборот.

