В твёрдых телах молекулы расположены в определённом порядке. Это лёд, соль, металлы, минералы и т. д.
Такие тела называются .


(от греч. κρύσταλλος «лёд», «горный хрусталь; кристалл») — твёрдые тела, в которых частицы (атомы и молекулы) расположены закономерно, образуя кристаллическую решётку.
— условный пространственный каркас, соединяющий частицы твёрдого вещества, для лучшего понимания геометрического строения кристалла.
Кристаллическое строение есть у веществ: поваренная соль, кварц, сахар, алмаз, графит, лёд.
Строение кристалла соли имеет форму правильного гексаэдра
, в вершинах которого находятся атомы \(Na\) и \(Cl\) поочерёдно.
<img alt="ф4_т4
кристалл поваренной соли2.jpg» src=»https://8b08ab88-ee1b-4b04-9ae9-321e0da71ae2.selcdn.net/e61ebd26-678e-43e5-a492-2eff64e88103/%D1%844_%D1%824%284%29%D0%BA%D1%80%D0%B8%D1%81%D1%82%D0%B0%D0%BB%D0%BB%20%D0%BF%D0%BE%D0%B2%D0%B0%D1%80%D0%B5%D0%BD%D0%BD%D0%BE%D0%B9%20%D1%81%D0%BE%D0%BB%D0%B82.jpg»>
<img alt="ф4_т4
кристаллич решетка поваренной соли.jpg» src=»https://8b08ab88-ee1b-4b04-9ae9-321e0da71ae2.selcdn.net/f1587a3a-9bb1-4168-a9f2-894967973fdd/%D1%844_%D1%824%285%29%20%D0%BA%D1%80%D0%B8%D1%81%D1%82%D0%B0%D0%BB%D0%BB%D0%B8%D1%87%20%D1%80%D0%B5%D1%88%D0%B5%D1%82%D0%BA%D0%B0%20%D0%BF%D0%BE%D0%B2%D0%B0%D1%80%D0%B5%D0%BD%D0%BD%D0%BE%D0%B9%20%D1%81%D0%BE%D0%BB%D0%B8.jpg»>
Самая распространённая форм — гексагональная (шестиугольная). В \(1955\) году русский учёный А. Заморский разделил снежинки на \(9\) классов (пластинки, иглы, звёзды, ежи, столбики, пушинки, запонки, призмы, групповые) и \(48\) видов.

Международная комиссия по снегу и льду приняла в \(1951\) году довольно простую классификацию кристаллов льда: пластинки, звёздчатые кристаллы, столбцы или колонны, иглы, пространственные дендриты, столбцы с наконечниками и неправильные формы. И ещё три вида обледенелых осадков: мелкая снежная крупка, ледяная крупка и град.
- Зависимость агрегатного состояния от дальнего и ближнего порядка расположения
- Примеры аморфных веществ
- Кристаллические вещества
- Зависимость свойств от типа кристаллической решетки
- Полиморфизм
- Аллотропия, текучесть аморфных тел
- Текучесть аморфных веществ
- Подведение итога урока
- Особенности существования кристаллических тел.
- Свойства металлического u и его терморадиационная стойкость
- Кристаллические и аморфные тела
- Твердые тела
- Аморфные тела
- Кристаллические тела
- Что мы узнали?
- Тест по теме
- Оценка доклада
Зависимость агрегатного состояния от дальнего и ближнего порядка расположения
В зависимости от давления и температуры, все вещества могут существовать в различных агрегатных состояниях: твердом, жидком, газообразном или в виде плазмы. При низких температурах и высоком давлении все вещества существуют в твёрдом агрегатном состоянии. Твердое и жидкое состояние вещества называют конденсированным.
В твердых телах частицы располагаются компактно, в определенном порядке. В зависимости от степени упорядоченности частиц в твердых телах определяют 2 фазовых состояния: кристаллическое и аморфное. Если частицы располагаются таким образом, что между соседними частицами есть некоторая упорядоченность в расположении, а именно: постоянное расстояние и углы между ними
, такое явление называют наличие ближнего порядка в расположении
(рис. а).

a b
Рис. 1. Наличие ближнего и дальнего порядка в расположении частиц
Если же частицы расположены таким образом, что упорядоченность наблюдается и между ближайшими соседями, и на гораздо больших расстояниях
, это называют наличие дальнего порядка
(рис. б).
Примеры аморфных веществ
Аморфное тело
(от греч А – не, morfe – форма) – бесформенные вещества. В них существует только ближний порядок и нет дальнего порядка.
Примеры аморфных тел приведены на рис. 2.

Рис. 2. Аморфные тела
Это воск, стекло, пластилин, смола, шоколад.
Свойства аморфных веществ
- Имеют только ближний порядок (как в жидкостях).
- Твердое агрегатное состояние при нормальных условиях.
- Нет четкой температуры плавления. Плавятся в интервале температур.
Кристаллические вещества
В кристаллическом
теле существует и ближний, и дальний порядок. Если мысленно соединить точки, обозначающие линии, получится пространственный каркас, который называется кристаллической решеткой. Точки, в которых размещены частицы – ионы, атомы или молекулы – называют узлами кристаллической решетки (рис. 3). Частицы не жестко фиксированы в узлах, они могут немного колебаться, не убегая из этих точек. В зависимости от того, какие частицы находятся в узлах кристаллической решетки, выделяют её типы (табл. 1).

Рис. 3. Кристаллическая решетка
Зависимость свойств от типа кристаллической решетки
Физические свойства веществ с различными типами кристаллических решеток
Табл.1. Физические свойства веществ
Существует несколько подтипов кристаллических решеток, различающихся расположением атомов в пространстве.
В веществах с атомной, ионной, металлической кристаллической решетками нет молекул – это немолекулярные вещества.
Молекулярные вещества
– с молекулярной кристаллической решеткой.
Полиморфизм
Полиморфизм — это явление, при котором сложные вещества одинакового состава имеют разные кристаллические решетки.
Например, пирит и марказит. Их формула – FeS 2
. Но они и выглядят по-разному, и обладают различными физическими свойствами. Аналогично, различными физическими свойствами обладают минералы состава CaCO 3
:
арагонит, мрамор, исландский шпат, мел.
Аллотропия, текучесть аморфных тел
Явление существования химических элементов в виде нескольких простых веществ называется аллотропией
, а вещества – аллотропными модификациями
.
Это объясняется различным составом вещества или различием в их кристаллической решетке. Кислород и озон – аллотропные модификации химического элемента кислорода. Углерод образует графит, алмаз, фуллерен, карбин. Расположение атомов в их кристаллических решетках разное, и поэтому они проявляют разные свойства. У фосфора аллотропные вещества – красный, белый и черный фосфор. Аллотропия характерна и для металлов. Например, железо может существовать в виде α, β, δ, γ.
Текучесть аморфных веществ
Одним из свойств, по которым отличаются аморфные тела от жидких, является их текучесть. Если положить кусочек смолы на нагретую поверхность, то он постепенно растечется по этой поверхности.
Вязкость
– это способность сопротивляться перемещению одних частей тела относительно других для жидкостей и газов: чем она выше, тем сложнее изменить форму тела. Оконные стекла – это типичные аморфные вещества. Теоретически они должны постепенно стекать вниз. Но вязкость стекла высокая, и его деформацией можно пренебречь. Вязкость стекла примерно в 1000 раз выше вязкости смолы. За год деформация стекла составляет 0,001 %. За 1000 лет деформация стекла составляет 1 %.
Подведение итога урока
На уроке рассмотрены типы кристаллических решеток, типы агрегатных состояний вещества, твердые тела с кристаллической структурой. Введено понятие полиморфизма и аллотропии. Объяснялась зависимость физических и химических свойств от разных типов кристаллических решеток в веществе.
- Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е издание. – М.: Просвещение, 2012.
- Попель П. П. Химия: 11 кл.: учебник для общеобразовательных учебных заведений / П. П. Попель, Л. С. Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
- Габриелян О. С. Химия. 11 класс. Базовый уровень. 2-е изд., стер. – М.: Дрофа, 2007. – 220 с.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- №№ 7, 8, 9 (с. 41) Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е издание. – М.: Просвещение, 2012.
- Приведите примеры веществ молекулярного строения.
- Что такое полиморфизм?
К особенностям
кристаллического строения металлов
относят зернистость
и анизотропность
.
Зернистость
структуры
– это проявление кристаллического
строения металлов и их сплавов. Образование
зерна происходит в процессе охлаждения
расплавленного металла.
Кристаллическое
строение хорошо наблюдается на изломе.
Причем, легкие металлы и их сплавы имеют
мелкозернистую структуру, которую можно
увидеть только в микроскоп.
В разных
кристаллографических плоскостях,
проведенных через центры атомов в
кристаллических решетках, число атомов
и расстояние между ними неодинаковы.
Например, в
плоскости, проведенной через основание
гексагональной решетки, размещаются
семь, а в плоскости ее грани – четыре
атома.
В связи с этим
свойства кристаллов в разных направлениях
неодинаковы. Это явление называется
анизотропией
.
Анизотропия проявляется в неодинаковости
сопротивления электрическому току,
отличии механических свойств и др.
Реальные металлы
являются телами поликристаллическими,
т.е. состоящими из большого числа
по-разному ориентированных в пространстве
кристаллов (зерен). Поэтому свойства
таких металлов в любом направлении
усредненно-одинаковые. В случае, когда
обработка металлов благоприятствует
ориентированию отдельных кристаллов
(при ковке, прокатывании), поликристаллические
металлы становятся также анизотропными.
Так, прочность образцов, вырезанных из
листа вдоль направления прокатывания,
выше прочности образцов, вырезанных
поперек прокатывания.
Особенности существования кристаллических тел.
Некоторые металлы
(железо, олово, титан) способны испытывать
превращения в твердом состоянии, они
изменяют тип кристаллической решетки
при изменении температуры, т.е. подвергаются
так называемой вторичной кристаллизации
(перекристаллизации). Например, железо
имеет четыре аллотропические формы:
α-Fe; β-Fe, γ-Fe, δ-Fe. Практическое значение
имеют α-Fe и γ-Fe, так как β-Fe и δ-Fe отличаются
от α-Fe только величиной межатомного
расстояния, а для β-Fe характерно отсутствие
магнитных свойств.
Температура, при
которой происходит переход металла из
одного аллотропического вида в другой,
называется критической
.
Величины этих температур видны на
диаграмме охлаждения и нагревания
чистого железа (рис. 2.4), которые
соответствуют горизонтальным участкам
графика, свидетельствующих о том, что
фазовые превращения происходят с
выделением тепла при охлаждении и
поглощением его при нагревании.
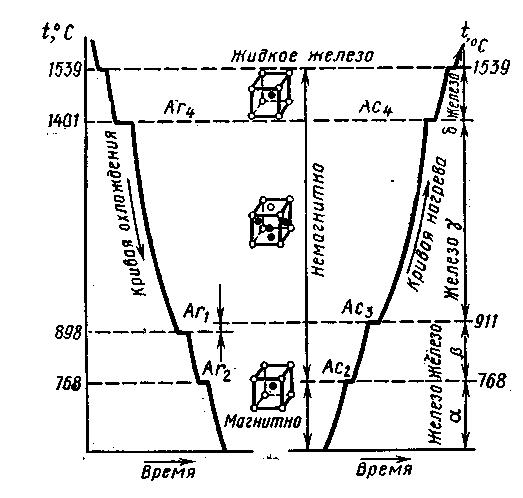
Рис.
2.4.
Кривые охлаждения и нагревания железа
Существование
одного и того же металла в нескольких
кристаллических формах (модификациях)
называется – полиморфизмом
.
А переход из одной модификации в другую
– полиморфным
превращением,
которое
сопровождается выделением или поглощением
теплоты.
Разные
полиморфные модификации обозначают
буквами греческого алфавита α, β, γ, δ,
которые добавляют к названиям металлов,
например α-Fe, γ-Fe.
При
полиморфных превращениях изменяется
не только строение кристаллической
решетки металла, но и его свойства –
прочность, пластичность и др.
Полиморфизм
металлов имеет большое значение, т.к.
определяет свойства металлов при
механической и термической обработке,
его работе в условиях низких и высоких
температур.
А 
томы
(частицы) твердого тела стремятся к
такому расположению в пространстве,
чтобы энергия их взаимодействия была
минимальной. Этому соответствует
определенный порядок в пространственном
размещении частиц, определяемый понятием
«кристаллическая решётка». На рис. 4
приведена модель кристаллической
решетки. В узлах решетки располагаются
атомы (ионы) вещества.
В
кристаллической решетке можно выделить
элемент объема из минимального количества
частиц (атомов), многократным переносом
(трансляцией) которого в пространстве
можно построить весь кристалл. Такой
элементарный объем, который характеризует
особенности строения данного типа
кристалла, называется элементарной
ячейкой.
Имеется
относительно небольшое количество
типов кристаллических решеток,
свойственных элементам периодической
системы.
Наиболее
часто элементы имеют кристаллические
решетки следующих типов:
гексагональную,
которая бывает плотноупакованная
(г.п.у.) и неплотноупакованная (н.г.п.у).
Подавляющее
большинство металлов имеет
отмеченные типы кристаллических
решеток. На рис. 5 приведены схемы
решеток о.ц.к., г.ц.к. и г.п.у.
М 
енее
распространены ромбоэдрическая,
тетрагональная и более сложные
решетки. На рис. 1 в клетках элементов
отмечены
характерные
для них типы кристаллических решеток.
Кристаллические
решетки характеризуют следующие основные
параметры: период решетки; координационное
число; атомный радиус; энергия решетки;
базис и коэффициент компактности
решетки.
Периодом
решетки называется расстояние между
центрами двух соседних частиц (атомов,
ионов) в элементарной ячейке решётки
(а
bc
на
рис. 4). Периоды решетки измеряются в
ангстремах (А)
или
килоиксах (1а=10 -8
см
; кХ= 1,00202
•10 8
см).
Координационное
число
К
показывает
количество атомов, находящихся па
наиболее близком и равном расстоянии
от любого выбранного
атома
в
решетке.
Под
атомным радиусом в общем случае понимают
половину межатомного расстояния между
центрами ближайших атомов в кристаллической
решетке элемента при равновесных
условиях. Атомный радиус не является
неизменной величиной, а изменяется в
зависимости от ряда факторов, важнейшими
из которых являются координационное
число и тип химической связи между
атомами в кристалле.
Энергия
кристаллической решетки определяется
как энергия, выделяющаяся при образовании
кристалла из ионов, атомов или других
частиц, образующих кристалл, когда эти
частицы в исходном состоянии находятся
в газообразном состоянии. Количественно
энергию связи оценивают по теплоте
сублимации, показывающей величину
энергии, которую необходимую затратить,
чтобы перевести валентные электроны
твердого тела на уровни свободного
атома. От величины энергии решетки
зависят важные свойства тела: температура
плавления, модуль упругости, прочность,
твердость и др. Увеличение валентности
атомов приводит к увеличению энергии
решетки.
Базисом
решетки называется количество атомов,
приходящихся на одну элементарную
ячейку решетки.
Коэффициент
компактности
решетки
определяется отношением объема,
занимаемого атомами Va
ко
всему объему решетки Vp
,
т.е.

Решетки
о.ц.к., г.ц.к. и г.п.у. являются типичными
решетками подавляющего большинства
технических материалов. Поэтому
следует рассмотреть их более подробно.
Представленные на рис. 5, слева, типы
кристаллических решеток схематично
отражают взаимное расположение
атомов (ионов) в кристалле. Если условно
считать атомы шарами одинакового
диаметра, то рис. 5, справа, дает более
точное представление о действительном
расположении атомов в о.ц.к., г.ц.к.
и г.п.у. кристаллах.
Кубическая
объемно-центрированная решетка (о.ц.к.),
рис. 5 а
,
имеет восемь атомов по вершинам и один
атом в центре куба. Период решетки а,
координационное
число
К=8
(атом
в центре куба имеет восемь соседей на
минимальном расстоянии

).
Базис решетки равен двум (каждый атом
в вершине принадлежит данной элементарной
ячейке на 1/8, атом в центре — целиком,
значит 1/8X8+4=2). Коэффициент компактности
решетки
о.ц.к. равен 68%.
2.
Кубическая гранецентpированная
решетка (г. ц.к.), рис. 5, б,
характеризуется
периодом а. Для установления координационного
числа рассмотрим атом в вершине куба.
Ближайшими к нему являются атомы в
центре граней куба на расстоянии

.
Таких атомов в одной ячейке 3. К атому
в вершине примыкает 8 элементарных
ячеек. Тогда общее число ближайших
соседей будет 
,
т. е. координационное число К=12. Коэффициент
компактности
решетки
г.ц.к. равен 74%.
№ 5.
Каков базис решетки г.ц.к.? (Учтите, что
в кристалле к ячейке со всех сторон
примыкают другие ячейки, поэтому не все
атомы изображенные на рис. 5, б,
принадлежат
только дайной ячейке). Ответ (см. на с.
26): базис равен 1) 6; 2) 14; 3) 4.
Гексагональная
плотноупакованная решетка (г.п.у.) рис.
5, в,
имеет
периоды а
и
с,
причем

.
№ 6.
Чему равно координационное число
решетки г. п. у.? (при решении этой задачи
рассмотрите атомы, примыкающие к атому
в центре основания призмы и учтите, что
основание призмы является общим для
двух элементарных ячеек). Ответ (см. на
с. 26): 1)6; 2) 9; 3) 12.
Для
решетки г. п. у. ( 
)
координационное число К
=12,
базис равен 6. Коэффициент компактности
= 74%.
В
общем случае элементарная ячейка
представляет собой косоугольный
параллелепипед (на рис. 4 обведен
жирно),Вершины параллелепипедов в
кристаллической решетке называются
узлами решетки. Прямые, проведенные
через узлы решетки, называются
кристаллографическими направлениями.
Плоскости, проведенные через узлы
решетки, называются кристаллографическими
плоскостями. Легко видеть, что плотность
атомов в различных кристаллографических
плоскостях и направлениях различна;
поэтому свойства кристаллического тела
в различных и направлениях также
различны. Это явление называется
анизотропией.
Для
обозначения кристаллографических
плоскостей и направлений пользуются
индексами Миллера. Для того, чтобы
установить индексы Миллера, кристалл
вписывается в пространственную систему
координат, как показано на рис. 4. Оси
координат X
,
Y
,
Z
называются
кристаллографическими осями. За единицу
измерения вдоль каждой оси принимается
период решетки, т. е. длина ребра
элементарной ячейки. Рис. 4 иллюстрирует
сказанное для наиболее общего случая.
№ 7
.
Каковы координаты узла 1, рис. 4? Ответ
(см. на с. 26): 1) х=а,
у =
b
,
z
=
c
;
2) х=а,
у=а,
z
=
a
;
3) х=0,
y
=
b
,
z
=
c
.
Индицирование
кристаллографических плоскостей
рассмотрим на примере простой кубической
решетки (рис. 6 а).
В
данном случае единица измерения вдоль
осей — длина ребра куба равная а.
Для
определения индексов кристаллографической
плоскости необходимо:
установить
координаты точек пересечения плоскости
с осями координат в единицах периодов
решетки;
взять
обратные значения этих величин;
привести
их к наименьшему целому, кратному каждому
из полученных чисел.
П 
олученные
значения простых целых чисел, не имеющие
общего множителя, заключенные в круглые
скобки, являются индексами Миллера
плоскости.
Рассмотрим
индексы Миллера плоскости, пересекающей
оси координат в точках

(где
a
период
решетки, рис. 6 а).
Обратные
значения этих чисел 2, 1, 3. Эти числа
являются простыми и не имеют общего
множителя. Поэтому индексы этой плоскости
будут (213). Следует читать: «дна», «одни»,
«три».
Индекс
по оси показывает, на сколько равных
частей данная система плоскостей
делит осевую единицу по данной координатной
оси.
№ 8.
Какие точки пересекает плоскость (211)?
Ответ (см. на с. 27): плоскость пересекает
1) ось X
в
точке 1/2а, оси Y
и
Z
в
точках 1а; 2) ось X
в
точке 2а, оси У
и
Z
в точках 1а.
Плоскость,
параллельная какой-либо координатной
оси, имеет индекс по этой оси нуль, т. к.

Так, например, плоскость qmrn
(рис.
6 а
)
имеет
индексы .
Если
плоскость пересекает ось в области
отрицательных значений координат, то
соответствующий индекс будет отрицательным
и знак минус становится над индексом.
Непараллельные
плоскости, имеющие одинаковое атомное
строение, кристаллографически
эквивалентны, например: (001) и
или
и (011) и т. д.
Зная
индексы ( hRl
)
плоскости, можно подсчитать межплоскостное
расстояние d
между
плоскостями ( hRl
)
данного семейства, которое для кубических
кристаллов с периодом решетки d
определяется
по формуле:
Эта
зависимость широко используется при
рентгеноструктурном анализе кристаллических
тел, имеющих кубическую решетку.
№ 9.
Чему равно межплоскостное расстояние
d
системы
плоскостей в кубическом кристалле,
имеющем период решетки, а=2
А?
Ответ (см. с. 27): 1)

;
2)

;
3)

.
Индицирование
кристаллографических направлений
рассмотрим по рис. 6 б.
Ориентация
прямой определяется координатами двух
ее точек. При определении индексов
направлений необходимо, чтобы:
одна
точка направления совпадала
с
началом координат (если прямая не
проходит через начало координат, то
необходимо путем параллельного переноса
совместить ее с началом координат или
перенести начало координат
на
прямую);
установить
координаты любой другой
точки,
лежащей
на данной прямой, в единицах решетки;
привести
отношения
этих координат к отношению трех наименьших
целых чисел;
заключив
полученные числа в квадратные скобки,
получим индексы кристаллографического
направления.
Для
получения индексов прямой, проходящей
через точки l
и центр граня k
(рис.
6б), необходимо перенести линию lk
параллельно
самой себе так, чтобы она проходила
через начало координат и определить
новые координаты точки k
,
которые
будут

После
открытия лучей Рентгена, длина волны
которых соизмерима с периодами решеток,
появилась возможность непосредственного
исследования расположения атомов в
кристаллической решетке.
Как
известно из курса физики, основой
рентгеноструктурного анализа является
формула Вульфа-Брегга, показывающая
условия интерференции отраженных
рентгеновских лучей от атомов в
параллельных кристаллографических
плоскостях кристалла (рис. 7, а). Лучи,
отраженные от этих плоскостей будут
усиливать друг друга при условии, что
разность пути для лучей
равна
целому числу длин волн
где
n
— —
целое
число,
— длина волны рентгеновских лучей, d
—
межплоскостное расстояние,
—
угол падения и отражения лучей.
На
рис. 7, 6
показана
схема наиболее часто используемого
метода съемки поликристаллических
материалов. Стрелками показаны образующие
двух конусов рентгеновских лучей,
отраженных от двух различных семейств
параллельных кристаллографических
плоскостей. На рис. 7, в
показана
схема рентгенограммы. Симметрично
расположены темные дуги па развернутой
пленке от воздействия отраженных лучей
на эмульсию пленки. Легко видеть, что
по расстоянию 21
между
дугами можно определить угол отражения
из формулы

,
где А
радиус
цилиндра, по которому была изогнута
пленка в камере. На рис. 8 показана
рентгенограмма, снятая с поликристаллической
меди. Индексы линий соответствуют
индексам отражающих плоскостей кристалла.
Формула
для расшифровки линий рентгенограмм,
снятых с материалов с кубической
решеткой, получена из формул
и
№ 11.
При съемке поликристаллического железа
(период решетки а=2,8605 kХ)
с
использованием
рентгеновской трубки с железным
антикатодом (=1,934
кХ)
получена линия с углом отражения
= 28°34′ (sin
= 0,477). От какой кристаллографической
плоскости получена эта линия? Ответ
(см. на с. 27): от плоскости 1) (211); 2)
; 3)
(321).
Все
металлы представляют собой кристаллические
вещества.
Твердое
состояние вещества характеризуется
тем, что расстояние между частицами
имеет величину порядка их размера, а
сами частицы совершают колебательные
движения относительно положения
равновесия.
Кристалл
– твердое тело, состоящее из упорядоченных
периодически повторяющихся в пространстве
частиц. Обычно они образуются и растут
из растворов и расплавов.
Кристаллическая
решетка
– присущее веществу в кристаллическом
состоянии правильное расположение
атомов, характеризующееся периодической
повторяемостью в 3х измерениях.
Аморфное
тело
– вещество, не имеющее кристаллической
решетки.
Элементарная
ячейка
– элемент объема из минимального числа
атомов, многократным переносом которого
в пространстве можно построить весь
кристалл.
размеры ребер
элементарной ячейки (a,b,c)
– периоды решетки – расстояния между
центрами ближайших атомов;углы между осями (α,β,γ);
координационное число – число атомов,
расположенных на ближайшем одинаковом
расстоянии от любого атома в решетке;базис решетки – количество атомов,
приходящихся на одну элементарную
ячейку;плотность упаковки – отношение объема,
занятого атомами к объему ячейки
(реальному объему).
примитивный – узлы решетки совпадают
с вершинами кристаллической решетки;базоцентрированный – атомы занимают
вершины ячеек и два места в противоположных
гранях;
По форме:
1 )
триклинная
(a
≠ b
≠ c,
α ≠ β ≠ γ, тип 1); 2)моноклинная (a
≠ b
≠ c,
α = β = 90°, γ < 90°, тип 1, 2);
ромбическая (a
≠ b
≠ c,
α = β = γ = 90°, тип 1, 2, 3, 4);ромбоэдрическая
(a
= b
= c,
α = β = γ ≠ 90°, тип 1);гексогональная (a
= b
≠ c,
α = β = 90°, γ = 120°, тип 2);тетрагональная (a
= b
≠ c,
α = β = γ = 90°, тип 1, 3);кубическая (a
= b
= c,
α = β = γ = 90°, тип 1, 3, 4).
Свойства металлического u и его терморадиационная стойкость
Природный
Me
U
– смесь изотопов: U 239
– 99,282 %; U 235
– 0,712 %; U 234
– 0,006 %.
Структура
Me
U
имеет три модификации: α,β,γ. ρ = 18,7-19,6
г/см 3
,
t°плавления
= 1130 °
C.
U
α – t°плавления
= 663 °
C,
орторомбическая структура.
U
β – t°плавления
= 663-775 °
C,
тетрагональная решетка.
U
γ – t°плавления
= 775-1130 °
C,
ОЦК.
Теплофизические
свойства U
определяются его кристаллической
структурой. Механические свойства
образца почти целиком определяются
способом приготовления, они сильно
зависят от чистоты материала (этим
пользуются при создании сплавов) и от
способа изготовления деталей. Механические
свойства очень чувствительны к примесям.
В
интервале температур от 373 до 77 К
пластичность U
резко падает с уменьшением температуры.
Одновременно понижается предел прочности,
уран из пластичного становится хрупким.
Температура перехода зависит от
содержания примесей, размеров зерна и
т.п. Пластичность U
при комнатной температуре может быть
повышена отжигом в вакууме. Наилучшие
результаты дает отжиг в течение одних
суток при 623-673 К. С ростом температуры
прочность урана снижается, а пластичность
растет. В случае больших зерен пластичность
и предел прочности меньше. С увеличением
температуры выше порога кристаллизации
(643-703 К) скорость ползучести U
резко возрастает.
В
условиях циклического изменения
температуры скорость ползучести
возрастает (из-за внутренних напряжений,
возникающих из-за анизотропии термического
расширения α-урана при изменении
температуры). Внутренние напряжения
возрастают до предела текучести и
вызывают пластическую деформацию зерен.
Термические
циклы вызывают изменение размера изделий
из U.
Наибольшая скорость роста (увеличения
длины изделий) урана отмечена при
максимальной разнице температур
термического цикла (причем наибольшее
влияние оказывает верхнее значение
температуры), низкой скорости нагрева
и высокой скорости охлаждения. В процессе
изменения температуры в тепловом цикле
происходит некоторое распухание изделий
из поликристаллического U
(т.е. уменьшения плотности), возникает
шероховатость поверхности – «жеванность»
и даже происходит растрескивание.
Рост
урана при термических циклах связывается
с тем, что в двух смежных различно
ориентированных зернах, имеющих
вследствие этого в определенном
направлении различные коэффициенты
теплового расширения, при нагревании
возникают внутренние напряжения. В
случае перехода через точки фазовых
превращений рост U
связывают с различием плотности и
прочности кристаллических модификаций
U.
Под
действием облучения происходит изменение
формы и размеров изделий из U.
При температуре ниже 673 К эти явления
обусловлены радиационным ростом U.
В мелкозернистом поликристаллическом
U
при малом выгорании поверхность изделий
становится шероховатой (эффект
апельсиновой корки). В случае крупного
зерна и больших выгораний неровности
на поверхности увеличиваются, появляются
чередующиеся гребешки и впадины
(жеванность). Одновременно может
происходить деформация изделий, например
прутов из U.
Поведение
поликристаллического урана под облучением
существенно зависит от размера зерна
и совершенства его структуры, от характера
текстуры.
2.максимальное
содержание делящегося материала (U).
В чистом виде Me
U
не применим как топливо для ЯР. При
облучении в АЗ реактора образец Me
U
быстро теряет свои (невысокие) коррозионные
и механические (прочностные) свойства,
изменяются его форма, размеры и даже
целостность. Причина этому ряд
специфических эффектов:
1)твердое
распухание; 2)термоциклирование – цикл
термообработки (разогрев / охлаждение),
приводит к изменению объема ΔV
= 2-5%; 3)радиационный рост;4)газовое
распухание; 5)радиационная ползучесть.
Для
того чтобы уменьшить эффекты 2 и 3 (см.
выше) нужно выбирать такие способы
обработки U,
которые способствуют измельчению зерен
и их произвольной ориентации в пространстве
между собой.
Рис. 3. Общественное достояние, дата обращения: 2021.08.01, https://commons.wikimedia.org/wiki/File:Allotropy_arabic.jpg.
Рис. 4. Указание автора не требуется, 2021.08.03, Pixabay License, https://pixabay.com/ru/photos/карандаш-графитный-карандаш-запись-1510731/. Указание авторства не требуется, 2021.08.03, Pixabay License, https://pixabay.com/ru/illustrations/алмаз-блестящий-gem-жемчужина-1186139/.
Рис. 1. http://www.astroguide.ru/files/article/55171/main-image/0706_16.jpg
1. Какие тела называют твёрдыми?
Твёрдыми называют тела, которые сохраняют форму и объём при отсутствии внешнего воздействия, например тела из металлов, пластмассы, льда, стекла.
2. Каковы особенности строения кристаллических твёрдых тел?
Частицы кристалла образуют упорядоченную пространственную структуру в виде кристаллической решётки. Упорядоченное размещение частиц повторяется во всём объёме кристалла. Основой строения кристалла является элементарная кристаллическая ячейка.
3. Какие типы кристаллов вы знаете? Чем они отличаются друг от друга?
Существуют ионные, атомные, металлические и молекулярные типы кристаллов. Друг от друга они отличаются составом: в узлах кристаллической решётки ионных кристаллов размещены положительно и отрицательно заряженные ионы, в узлах атомных кристаллов — нейтральные атомы, в узлах металлических кристаллов — положительные ионы, в узлах молекулярных кристаллов — молекулы.
4. В чём отличие между моно- и поликристаллами?
Монокристаллы имеют во всём объёме единую кристаллическую решётку, а поликристаллы состоят из из большого числа сросшихся между собой маленьких кристаллов. Также монокристаллы анизотропны, а поликристаллы изотропны.
5. В чём отличие между понятиями «анизотропия» и «изотропия»?
Анизотропия заключается в зависимости физических свойств от направления внутри кристалла. Изотропия заключается в одинаковости физических свойств по всем направлениям.
6. Чем отличаются основные физические свойства кристаллических и аморфных тел?
Аморфные тела не имеют определённую температуру плавления, кристаллические — имеют. В своём строении аморфные тела имеют ближний порядок расположения частиц, кристаллические — дальний порядок. Расположение атомов в аморфных телах беспорядочно, в кристаллических атомы находятся в узлах кристаллической решетки.
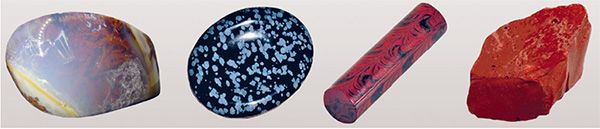
Аморфные тела.
К аморфным (от греч. аmorphous
— бесформенный) телам относят опал, обсидиан, эбонит, сургуч (рис. 50), стекло, различные пластмассы, смолы (вар, канифоль, янтарь) и др.
1
Аморфное состояние — твёрдое некристаллическое состояние вещества, характеризующееся изотропией свойств и отсутствием определённой температуры плавления.
Зависимость температуры аморфного тела от полученного им количества теплоты представлена на рисунке 49, график 2
. При повышении температуры аморфное вещество размягчается и постепенно переходит в жидкое состояние. В аморфном состоянии вещество не имеет строгого порядка в расположении атомов и молекул. Аморфное состояние — бесформенное состояние со слабо выраженной текучестью.
Аморфные тела называют переохлаждёнными жидкостями, так как у них, как и у жидкостей, существует только ближний порядок расположения частиц.
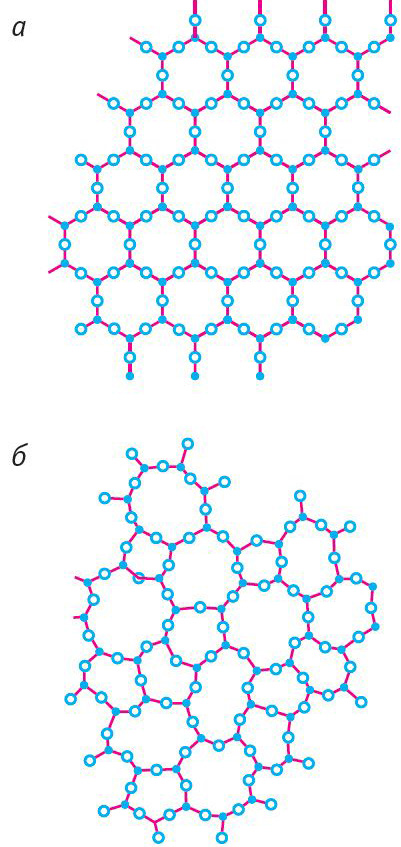
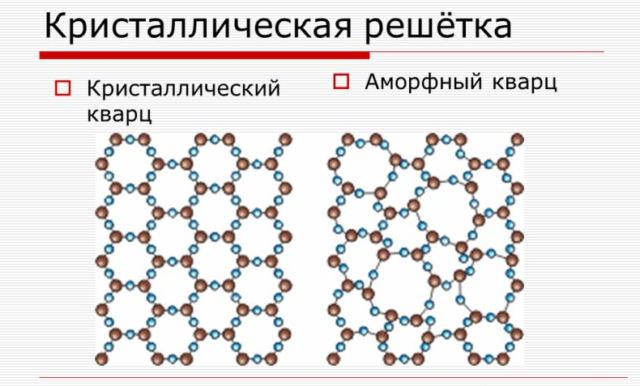
На рисунках 51 схематически представлено строение кристаллического кварца (рис. 51, а
) и аморфного кварца (рис. 51, б
).

Аморфные тела при определённых условиях могут кристаллизоваться. Сахар-песок является кристаллическим телом (рис. 52, а
). Если его расплавить, то, застывая, он превращается в прозрачный стеклообразный леденец (рис. 52, б
), который является аморфным телом. Через некоторый промежуток времени леденец «засахаривается», т. е. опять становится кристаллическим.
При скоростях охлаждения, превышающих миллион градусов в секунду, удалось получить аморфные металлические сплавы — стеклообразные металлы. Аморфный металл чрезвычайно твёрд и прочен. Его используют как режущий инструмент. Он обладает сильновыраженными магнитными свойствами, поэтому незаменим при изготовлении магнитных головок для звуко- и видеозаписи. Кроме того, аморфные металлы обладают высокой антикоррозийной стойкостью.
От теории к практике
1.
Имеются две тонкие пластинки, покрытые воском. К пластинкам поочерёдно прикоснулись раскалённой спицей. На одной пластинке при плавлении воска образовалось круглое пятно, а на другой — овал. Какое из этих тел кристаллическое, а какое аморфное?
2.
В двух сосудах необходимо расплавить два твёрдых тела. Как, наблюдая за процессом плавления, можно определить, какое из этих тел кристаллическое, а какое аморфное?
Стекло обладает текучестью даже при нормальных условиях, хотя и течёт крайне медленно. В старинных зданиях, где окна не меняли достаточно долго, можно заметить постепенное утолщение стёкол книзу.
![]()
1.
Какие тела называют твёрдыми?
2.
Каковы особенности строения кристаллических твёрдых тел?
3.
Какие типы кристаллов вы знаете? Чем они отличаются друг от друга?
4.
В чём отличие между моно- и поликристаллами?
5.
В чём отличие между понятиями «анизотропия» и «изотропия»?
6.
Чем отличаются основные физические свойства кристаллических и аморфных тел?
Теория
решётчатого строения кристаллов была
создана в середине 19 века французским
кристаллографом О. Бравэ, а затем русский
кристаллограф академик Е. С. Фёдоров и
немецкий учёный А. Шенфлис завершили
математическую разработку этой теории.
При создании и разработке теории
решетчатого строения кристаллов Бравэ,
Фёдоров и др. кристаллографы основывались
исключительно на некоторых важных
свойствах кристаллического вещества.
Основными
свойствами кристаллов являются их
однородность, анизотропность, способность
самоограняться и симметричность.
Однородным
обычно называют тело, которое обнаруживает
одинаковые свойства во всех своих
частях. Кристаллическое тело однородно,
т. к. различные участки его имеют
одинаковое строение, т. е. одинаковую
ориентировку слагающих частиц,
принадлежащих одной и той же пространственной
решётке. Однородность кристалла следует
отличать от однородности жидкости или
газа, которая имеет статистический
характер.
Анизотропным
называется такое однородное тело,
которое обладает неодинаковыми свойствами
по непараллельным направлениям.
Кристаллическое тело анизотропно, т.
к. строение пространственной решётки,
а значит и самого кристалла, в общем
случае неодинаково по непараллельным
направлениям. По параллельным же
направлениям частицы слагающие кристалл,
как и узлы его пространственной решётки,
расположены строго одинаковым образом,
поэтому и свойства кристалла по таким
направлениям должны быть одними и теми
же.
Приведенные
примеры, конечно, исключительны по своей
характерности. Однако точными
исследованиями установлено, что абсолютно
все кристаллы в том или ином отношении
обладают анизотропностью.
Однородностью
и в некоторой степени анизотропностью
могут обладать также и аморфные тела.
Но ни при каких условиях аморфные
вещества не могут сами по себе принимать
форму многогранников. Образовываться
в виде плоскостных многогранников могут
лишь кристаллические тела. В
способности самоограняться
,
т. е. принимать многогранную форму,
проявляется наиболее характерный
внешний признак кристаллического
вещества.
Правильная
геометрическая форма кристаллов с
давних пор привлекала внимание человека,
и её загадочность вызывала в прошлом у
людей различные суеверия. Кристаллы
таких веществ, как алмаз, изумруд, рубин,
сапфир, аметист, топаз, бирюза, гранат
и др., ещё в 18 в. считались носителями
сверхъестественных сил и использовались
не только как драгоценные украшения,
но и как талисманы или средство от многих
болезней и укусов ядовитых змей.
На
самом же деле способность самоограняться,
как и первые два свойства, является
следствием правильного внутреннего
строения кристаллического вещества.
Внешние границы кристаллов как бы
отражают эту правильность их внутреннего
строения, ибо каждый кристалл можно
рассматривать как часть его пространственной
решётки, ограниченной плоскостями
(гранями).
Необходимо
вместе с тем отметить, что способность
кристаллического вещества самоограняться
проявляется не всегда, а только при
особо-благоприятных условиях, когда
внешняя окружающая среда не мешает
образованию и свободному росту кристаллов.
При отсутствии таких условий получаются
или совершенно неправильные или частично
деформированные кристаллы. Несмотря
на это они сохраняют все свои внутренние
свойства, в том числе и причины,
заставляющие кристаллы принимать форму
многогранника. Поэтому, если кристаллическое
зерно неправильной формы поместить в
определённые условия, в которых кристалл
сможет свободно расти, то оно примет
через некоторое время форму плоскостного
многогранника, присущую данному веществу.
Симметрия
кристаллов
также является отражением их закономерного
внутреннего строения. Все кристаллы в
той или иной степени симметричны, т. е.
состоят из закономерно повторяющихся
равных частей, так как их строение
выражается пространственной решёткой,
которая по своей природе всегда
симметрична.
Открытие
мюнхенским физиком М. Лауэ в 1912 г. явления
дифракции рентгеновских лучей при их
прохождении через кристалл явилось
первым экспериментальным подтверждением
правильности теории решетчатого строения
кристаллического вещества. С этого
момента стало возможным, с одной стороны,
посредством кристаллов исследовать
рентгеновские лучи, а с другой — с помощью
рентгеновских лучей исследовать
внутреннее строение кристаллов. Таким
путём было доказано, что абсолютно все
кристаллы состоят из частиц, расположенных
друг относительно друга закономерно,
наподобие узлов пространственной
решётки.
После
опытов Лауэ теория решетчатого строения
кристаллов перестала быть только лишь
умозрительным построением и приобрела
форму закона.
Кристаллические и аморфные тела


Всего получено оценок: 408.
Всего получено оценок: 408.
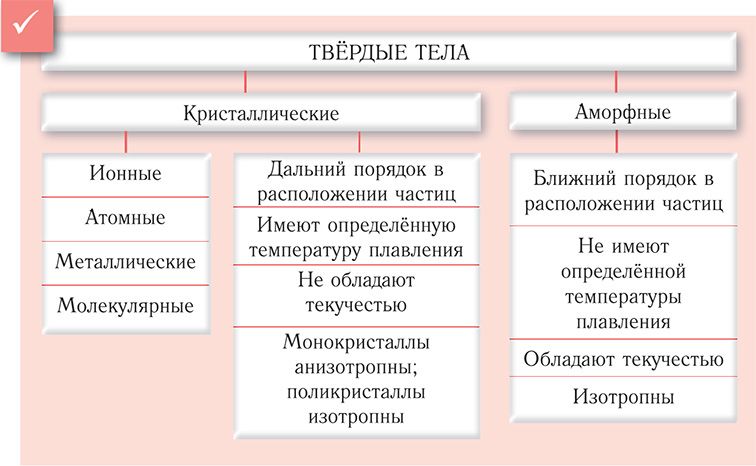
В зависимости от внутреннего строения твердые тела бывают либо кристаллическими, либо аморфными. Молекулы и атомы кристаллов расположены в определенной, повторяющейся последовательности на больших расстояниях, сохраняя так называемый дальний порядок. Атомы и молекулы в аморфных телах размещены неупорядоченно, для них характерен ближний порядок со строением аналогичным жидкому состоянию вещества. Рассмотрим основные отличия кристаллических тел от аморфных, которые проявляются в их физических свойствах.
Твердые тела
Все твердые тела обладают следующими общими свойствами:
- Способностью долгое время сохранять форму и объем (геометрические размеры);
- Наличием упругих сил, которые возникают при небольших изменениях объема от внешнего воздействия (сжатия, растяжения или сдвига).
Современные ученые исследуют пространственное расположение атомов и молекул в твердых телах с помощью электронных микроскопов, которые позволяют получить изображение объекта с сильным увеличением (до 10 6
раз). Первый электронный микроскоп был изобретен в 30-х годах прошлого века. В 2018 г. с помощью последних версий этого прибора было получено разрешение 0,39 ангстрем. Напомним, что 1 ангстрем равен 10 -8
см. В большинстве кристаллов это соответствует шагу атомной решетки.
Аморфные тела
Смола, воск, графит, изделия из стекла и янтаря, пластмассы — все это примеры аморфных тел (от греч.слова Amorphous — бесформенный, некристаллический).
Отсутствие дальнего порядка в расположении частиц вещества у аморфных тел приводит к тому, что их физические свойства одинаковы во всех направлениях. Такие тела называют изотропными (слово “изотропный” составлено из двух греческих слов: isos — ровный, tropos — направление). Изотропность физических свойств аморфных тел является следствием хаотичного расположения составляющих их молекул и атомов.
Характерной особенностью аморфных тел является отсутствие определенной температуры плавления, то есть отсутствует четкий переход от твердого состояния к жидкому: при нагревании аморфное тело становится только более текучим.
Кристаллические тела
Твердые тела, в которых молекулы и атомы расположены упорядоченно и образуют периодически повторяющуюся структуру, называются кристаллами. Физические свойства кристаллов (упругие, механические, тепловые, электрические, магнитные, оптические) в разных направлениях неодинаковы. Такое свойство называется анизотропностью. Анизотропия кристаллов объясняется тем, что при упорядоченном расположении частиц расстояния между ними и силы взаимодействия (притяжения и отталкивания) оказываются неодинаковыми в разных направлениях.
Различают кристаллические тела двух видов: монокристаллы и поликристаллы. Главным признаком монокристаллов является повторяющееся внутреннее строение (структура) во всем объеме тела.
Поликристалл — это совокупность (набор) сросшихся друг с другом, хаотически ориентированных, небольших кристаллов. Каждый маленький кристалл обладает свойствами анизотропии, но их совокупность — поликристалл — изотропен.

Часто встречаются кристаллические тела одинаковые по своему химическому составу, но обладающие очень разные физические свойства. Самый известный пример — это углерод, имеющий две модификации: графит и алмаз. Разное строение кристаллических решеток является причиной того, что алмаз имеет рекордные показатели твердости, а графит из-за его мягкости используется в качестве грифелей для карандашей.


Что мы узнали?
Итак, мы узнали, что кристаллические и аморфные тела кроме общих признаков, которые относят их к твердым телам, имеют совершенно разные физические свойства. Аморфные тела обладают изотропными свойствами, а для кристаллов характерна анизотропия физических параметров. Кристаллические тела делятся на монокристаллы и поликристаллы.
Тест по теме

Чтобы попасть сюда — пройдите тест.
Оценка доклада
Всего получено оценок: 408.
А какая ваша оценка?
Теория
решётчатого строения кристаллов была
создана в середине 19 века французским
кристаллографом О. Бравэ, а затем русский
кристаллограф академик Е. С. Фёдоров и
немецкий учёный А. Шенфлис завершили
математическую разработку этой теории.
При создании и разработке теории
решетчатого строения кристаллов Бравэ,
Фёдоров и др. кристаллографы основывались
исключительно на некоторых важных
свойствах кристаллического вещества.
Основными
свойствами кристаллов являются их
однородность, анизотропность, способность
самоограняться и симметричность.
Однородным
обычно называют тело, которое обнаруживает
одинаковые свойства во всех своих
частях. Кристаллическое тело однородно,
т. к. различные участки его имеют
одинаковое строение, т. е. одинаковую
ориентировку слагающих частиц,
принадлежащих одной и той же пространственной
решётке. Однородность кристалла следует
отличать от однородности жидкости или
газа, которая имеет статистический
характер.
Анизотропным
называется такое однородное тело,
которое обладает неодинаковыми свойствами
по непараллельным направлениям.
Кристаллическое тело анизотропно, т.
к. строение пространственной решётки,
а значит и самого кристалла, в общем
случае неодинаково по непараллельным
направлениям. По параллельным же
направлениям частицы слагающие кристалл,
как и узлы его пространственной решётки,
расположены строго одинаковым образом,
поэтому и свойства кристалла по таким
направлениям должны быть одними и теми
же.
Приведенные
примеры, конечно, исключительны по своей
характерности. Однако точными
исследованиями установлено, что абсолютно
все кристаллы в том или ином отношении
обладают анизотропностью.
Однородностью
и в некоторой степени анизотропностью
могут обладать также и аморфные тела.
Но ни при каких условиях аморфные
вещества не могут сами по себе принимать
форму многогранников. Образовываться
в виде плоскостных многогранников могут
лишь кристаллические тела. В
способности самоограняться
,
т. е. принимать многогранную форму,
проявляется наиболее характерный
внешний признак кристаллического
вещества.
Правильная
геометрическая форма кристаллов с
давних пор привлекала внимание человека,
и её загадочность вызывала в прошлом у
людей различные суеверия. Кристаллы
таких веществ, как алмаз, изумруд, рубин,
сапфир, аметист, топаз, бирюза, гранат
и др., ещё в 18 в. считались носителями
сверхъестественных сил и использовались
не только как драгоценные украшения,
но и как талисманы или средство от многих
болезней и укусов ядовитых змей.
На
самом же деле способность самоограняться,
как и первые два свойства, является
следствием правильного внутреннего
строения кристаллического вещества.
Внешние границы кристаллов как бы
отражают эту правильность их внутреннего
строения, ибо каждый кристалл можно
рассматривать как часть его пространственной
решётки, ограниченной плоскостями
(гранями).
Необходимо
вместе с тем отметить, что способность
кристаллического вещества самоограняться
проявляется не всегда, а только при
особо-благоприятных условиях, когда
внешняя окружающая среда не мешает
образованию и свободному росту кристаллов.
При отсутствии таких условий получаются
или совершенно неправильные или частично
деформированные кристаллы. Несмотря
на это они сохраняют все свои внутренние
свойства, в том числе и причины,
заставляющие кристаллы принимать форму
многогранника. Поэтому, если кристаллическое
зерно неправильной формы поместить в
определённые условия, в которых кристалл
сможет свободно расти, то оно примет
через некоторое время форму плоскостного
многогранника, присущую данному веществу.
Симметрия
кристаллов
также является отражением их закономерного
внутреннего строения. Все кристаллы в
той или иной степени симметричны, т. е.
состоят из закономерно повторяющихся
равных частей, так как их строение
выражается пространственной решёткой,
которая по своей природе всегда
симметрична.
Открытие
мюнхенским физиком М. Лауэ в 1912 г. явления
дифракции рентгеновских лучей при их
прохождении через кристалл явилось
первым экспериментальным подтверждением
правильности теории решетчатого строения
кристаллического вещества. С этого
момента стало возможным, с одной стороны,
посредством кристаллов исследовать
рентгеновские лучи, а с другой — с помощью
рентгеновских лучей исследовать
внутреннее строение кристаллов. Таким
путём было доказано, что абсолютно все
кристаллы состоят из частиц, расположенных
друг относительно друга закономерно,
наподобие узлов пространственной
решётки.
После
опытов Лауэ теория решетчатого строения
кристаллов перестала быть только лишь
умозрительным построением и приобрела
форму закона.

