
- Основные положения, при помощи которых объясняется различие строения веществ в твердом, жидком и газообразном состоянии
- Расположение частиц в твердом состоянии, жидком и газообразном
- Движение частиц в твердом, жидком и газообразном состоянии
- Взаимодействие частиц в твердом, жидком и газообразном состоянии
- Форма и объем которую принимают вещества в твердом, жидком и газообразном состоянии
- Кристаллические и аморфные тела
- Твердые тела
- Кристаллические тела
- Что мы узнали?
- Тест по теме
- Оценка доклада
- Строение газообразных, жидких и твердых тел
- Агрегатные состояния вещества
- Строение газа
- Строение жидкого вещества
- Строение твердого тела
Основные положения, при помощи которых объясняется различие строения веществ в твердом, жидком и газообразном состоянии
Дети назовите вещество которое находится в трех агрегатных состояниях. Верно это вода. Которая может находиться в жидком, твёрдом и газообразном состоянии. Вода это жидкое состояние, пар газообразное состояние и лёд — твёрдое состояние. Скажите а какие положения веществ отличают одно состояние от другого. Это расположение частиц, движение частиц и взаимодействие частиц.
Расположение частиц в твердом состоянии, жидком и газообразном
И так, рассмотрим отличие одного состояния веществ от другого. В твёрдом состоянии частицы располагаются в строгом порядке, образуя кристалл. Частицы не имеют строгого положения в жидком состоянии. В газообразном состоянии нет строгого порядка.
Движение частиц в твердом, жидком и газообразном состоянии
Частицы в твердых телах совершают колебательное движение. Подобно маятнику часов. В жидкостях молекулы совершают бестолковое движение. В газообразном состоянии частицы движутся хаотично, беспорядочно, с очень большой скоростью. Она равна скорости пули из ружья. Примеры: при 20 градусах по Цельсию скорость молекулы водорода — 2000 м/с, а кислорода 1600 м/с, азота 600 м/с.
Взаимодействие частиц в твердом, жидком и газообразном состоянии
В твёрдом состоянии частицы взаимодействуют очень сильно между собой. Так как между частицами промежутки меньше размера одной частицы. В жидком состоянии взаимодействие слабее. Между частицами промежутки увеличиваются и равны размеру одной частицы. В газообразном состоянии взаимодействие частиц самое слабое. В промежутках между частицами можно поместить до десяти таких частиц.
Форма и объем которую принимают вещества в твердом, жидком и газообразном состоянии
Но кроме трёх положений агрегатные состояния характеризуются объемом и формой. В твёрдом состоянии форма неизменная. Жидкость принимает форму сосуда. И газы принимают форму сосуда. Объём твердых тел неизменный. Для изменения объема твердого тела, необходимо приложить огромные усилия. Объем жидкости изменить нельзя. Пример: возьмем свинцовый шар и заполнили его водой. Запаяли шар. Стали ударять молотом по нему, пытаясь уменьшить объем. Шар лопнул. Вода вылилась. Возникают силы отталкивания. Которые не дают возможности уменьшить объем. А в газах занимает наибольший, предоставленный объем. Примеры: возьмем медные опилки и поместим в мензурку большого объема. Нальем азотной кислоты. Закроем мензурку наполовину. Образуется бурый дым, который заполняет половину мензурки. Передвинем крышку вверх, до полного объема. Бурый дым заполняет все пространство. Это доказывает, что газы занимают наибольший предоставленный объем.
Кристаллические и аморфные тела

Всего получено оценок: 408.
В зависимости от внутреннего строения твердые тела бывают либо кристаллическими, либо аморфными. Молекулы и атомы кристаллов расположены в определенной, повторяющейся последовательности на больших расстояниях, сохраняя так называемый дальний порядок. Атомы и молекулы в аморфных телах размещены неупорядоченно, для них характерен ближний порядок со строением аналогичным жидкому состоянию вещества. Рассмотрим основные отличия кристаллических тел от аморфных, которые проявляются в их физических свойствах.
Твердые тела
Все твердые тела обладают следующими общими свойствами:
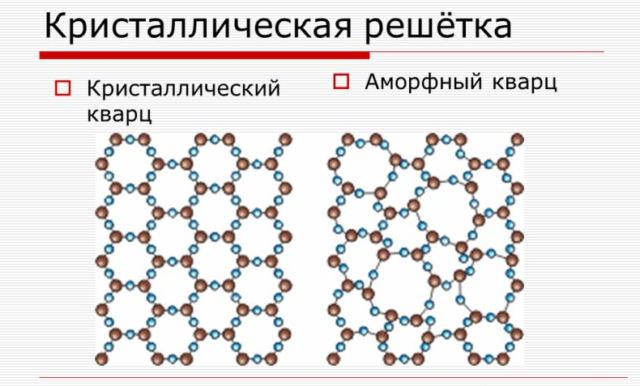
Рис. 1. Примеры решеток кристаллических и аморфных тел – кварц аморфный и кристаллический.
Современные ученые исследуют пространственное расположение атомов и молекул в твердых телах с помощью электронных микроскопов, которые позволяют получить изображение объекта с сильным увеличением (до 106 раз). Первый электронный микроскоп был изобретен в 30-х годах прошлого века. В 2018 г. с помощью последних версий этого прибора было получено разрешение 0,39 ангстрем. Напомним, что 1 ангстрем равен 10-8 см. В большинстве кристаллов это соответствует шагу атомной решетки.
Смола, воск, графит, изделия из стекла и янтаря, пластмассы — все это примеры аморфных тел (от греч.слова Amorphous — бесформенный, некристаллический).
Отсутствие дальнего порядка в расположении частиц вещества у аморфных тел приводит к тому, что их физические свойства одинаковы во всех направлениях. Такие тела называют изотропными (слово “изотропный” составлено из двух греческих слов: isos — ровный, tropos — направление). Изотропность физических свойств аморфных тел является следствием хаотичного расположения составляющих их молекул и атомов.
Характерной особенностью аморфных тел является отсутствие определенной температуры плавления, то есть отсутствует четкий переход от твердого состояния к жидкому: при нагревании аморфное тело становится только более текучим.
Кристаллические тела
Твердые тела, в которых молекулы и атомы расположены упорядоченно и образуют периодически повторяющуюся структуру, называются кристаллами. Физические свойства кристаллов (упругие, механические, тепловые, электрические, магнитные, оптические) в разных направлениях неодинаковы. Такое свойство называется анизотропностью. Анизотропия кристаллов объясняется тем, что при упорядоченном расположении частиц расстояния между ними и силы взаимодействия (притяжения и отталкивания) оказываются неодинаковыми в разных направлениях.
Различают кристаллические тела двух видов: монокристаллы и поликристаллы. Главным признаком монокристаллов является повторяющееся внутреннее строение (структура) во всем объеме тела.
Поликристалл — это совокупность (набор) сросшихся друг с другом, хаотически ориентированных, небольших кристаллов. Каждый маленький кристалл обладает свойствами анизотропии, но их совокупность — поликристалл — изотропен.

Рис. 2. Монокристаллы и поликристаллы.
Часто встречаются кристаллические тела одинаковые по своему химическому составу, но обладающие очень разные физические свойства. Самый известный пример — это углерод, имеющий две модификации: графит и алмаз. Разное строение кристаллических решеток является причиной того, что алмаз имеет рекордные показатели твердости, а графит из-за его мягкости используется в качестве грифелей для карандашей.

Рис. 3. Графит и алмаз.
Что мы узнали?
Итак, мы узнали, что кристаллические и аморфные тела кроме общих признаков, которые относят их к твердым телам, имеют совершенно разные физические свойства. Аморфные тела обладают изотропными свойствами, а для кристаллов характерна анизотропия физических параметров. Кристаллические тела делятся на монокристаллы и поликристаллы.
Тест по теме
Чтобы попасть сюда — пройдите тест.
Оценка доклада
А какая ваша оценка?
Строение газообразных, жидких и твердых тел

Всего получено оценок: 316.
Все вещества в природе, независимо от температуры и давления, состоят из молекул одного и того же состава. Однако строение вещества отличается при различных внешних условиях. Кратко рассмотрим строение газообразных, жидких и твердых тел.
Агрегатные состояния вещества
Внешний вид одного и того же вещества существенно зависит от температуры и давления. Правда, далеко не любое вещество легко наблюдать в разных состояниях (особенно это касается плазмы). Но для подготовки доклада в 10 классе достаточно изучить свойства обычной воды. Любой знает, что обычная вода при низкой температуре превращается в лед, а при высокой — в пар, причем эти изменения обратимы.
Влияние давления проследить сложнее, однако тоже возможно: например, измеряя температуру кипения воды в горах, где атмосферное давление заметно ниже. Так, на Крестовом перевале (Военно-Грузинская дорога) вода кипит уже при 92 ⁰С.
Лед, жидкость и пар — это агрегатные состояния воды, строение которых имеет свои особенности. Рассмотрим их с точки зрения молекулярно-кинетической теории (МКТ).
Строение газа
При достаточно высокой температуре и не слишком большом давлении молекулы вещества обладают большой энергией, и сил их взаимодействия недостаточно, чтобы удерживать их рядом. Сила гравитации также оказывается недостаточной, чтобы заметно влиять на поведение молекул. Поэтому при таких условиях молекулы могут свободно перемещаться в пространстве, заполняя весь предоставленный объем.
Молекулы сталкиваются друг с другом и с другими телами, создавая давление газа, однако путь их свободного полета многократно превышает размеры молекул. Взаимодействия происходят лишь в короткое время столкновения. Связь давления с объемом и температурой описывается газовыми законами.

Рис. 1. Три газовых закона.
Строение жидкого вещества
Если уменьшать температуру газа, то энергия молекул будет всё меньше, свободный пробег — тоже. Наконец, молекулы в среднем станут находиться настолько близко друг к другу, что силы притяжения начнут играть заметную роль в поведении вещества, выражаясь в виде поверхностного натяжения. Сила тяжести будет также вносить свою лепту: в результате вещество займет нижнюю часть предоставленного объема.
В жидком состоянии молекулы находятся очень близко друг к другу. Поэтому сжать их можно лишь за счет изменения формы молекул, для чего требуется гораздо больше энергии по сравнению со сжатием за счет уменьшения расстояний между молекулами. Большую часть времени молекулы жидкости проводят в беспорядочных колебаниях, но появление даже небольшой внешней силы способно двигать молекулы жидкости, что обеспечивает текучесть.

Рис. 2. Молекулы в жидкости.
Строение твердого тела
Если уменьшать температуру жидкости, то наступает момент, когда энергия молекулы становится меньше энергии связи между соседними молекулами. В таком состоянии молекулы выстраиваются в регулярную пространственную структуру с наименьшей потенциальной энергией, называемую кристаллом. Порядок, в котором находятся молекулы внутри кристалла, называется кристаллической решеткой.
В кристалле молекулы не могут менять свое расположение относительно соседей. Уменьшению расстояний мешают силы отталкивания положительных ядер в молекулах, увеличению расстояний — силы притяжения между электронными оболочками и ядрами соседних молекул.
Кристалл сохраняет свою форму даже под действием достаточно больших внешних нагрузок потому, что для ее изменения необходимо разрушить сразу много молекулярных связей.
Сравнительная таблица строения твердых, жидких и газообразных тел представлена ниже:
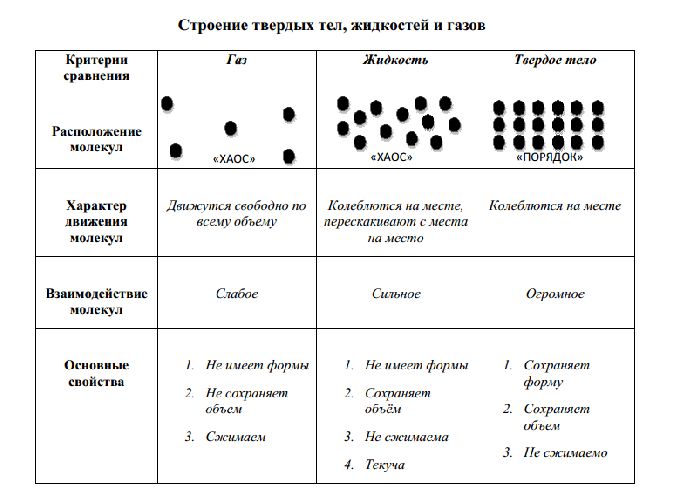
Рис. 3. Таблица строения твердых жидких и газообразных тел.
С точки зрения МКТ, газ представляет собой молекулы вещества, имеющие достаточно большую энергию, чтобы независимо двигаться на относительно больших расстояниях друг от друга. В жидкостях молекулы располагаются рядом и начинают взаимодействовать, но всё еще способны двигаться независимо. В твердых телах молекулы выстраиваются в строгую пространственную структуру и не могут двигаться относительно друг друга.
