одновременно используются обе разновидности пустоты — и вакансии, и межузельные ячейки. Если в междоузлии находится атом, почти такой же по размерам, как и атомы в узлах, ему очень трудно «проскочить» в соседнее междоузлие, поскольку при этом должны возникнуть слишком большие искажения решетки. Искажения будут меньше, если атом, находящийся в междоузлии, вытеснит из узла решетки себе подобный атом в соседнее междоузлие, создаст вакансию и займет ее, передав «инициативу» движения атому, оказавшемуся в междоузлии.
Такой механизм называется механизмом вытеснения. Именно по механизму вытеснения диффундирует серебро в монокристалле бромистого серебра. Ион серебра ненамного меньше иона брома, и «просочиться» между двумя ионами брома ему трудно. Для иона серебра более легким оказывается другой путь: вытеснить ион серебра из «серебряной» подрешетки кристалла бромистого серебра в межузельную ячейку, занять его позицию, а затем вытесненному иону предоставить возможность проделать то же (рис. 15). Для иона серебра есть еще и другая возможность — сидеть в узле «серебряной» подрешетки и терпеливо ждать, пока рядом окажется «серебряная» вакансия. Видимо, эта возможность энергетически менее предпочтительна, чем возможность вытеснения. О том, что осуществляется именно механизм вытеснения, свидетельствует опыт.
Реальный кристалл
состоит из скопления большого числа
мелких кристаллов неправильной формы,
которые называются зернами или
кристаллитами (рис. 2.4).

Рис.
2.4. Блочная структура кристалла: схема
(а); реальная блочная структура в алюминии
(б), наблюдаемая в электронном микроскопе
на просвет, (х 35000)
Зерно не является
монолитным кристаллом, построенным из
строго параллельных атомных слоев. В
действительности оно состоит как бы из
мозаики отдельных блоков, кристаллографические
плоскости в которых повернуты друг
относительно друга на небольшой угол
– порядка нескольких минут. Такое
строение зерна носит название мозаичной
структуры, а составляющие ее
блоки называются блоками мозаики.
Часто блоки
объединяются в более крупные агрегаты
– так называемые фрагменты.
Фрагменты в свою очередь разориентированы
относительно друг друга в несколько
градусов. Зерна ориентированы случайно
по отношению друг к другу. Преимущественная
ориентация зерен называется текстурой.
Поверхность раздела зерен называется
границей.
Технические металлы
являются поликристаллами,
т.е. состоят из совокупности кристаллитов
с различной ориентацией, что приводит
к изменению свойств металлов при
различных процессах их обработки.
При определенных
условиях, обычно при очень медленном
контролируемом отводе тепла при
кристаллизации, может быть получен
кусок металла, представляющий собой
один кристалл, который называют
монокристаллом.
2.2. Дефекты
кристаллического строения
Строение реальных
кристаллов отличается от идеальных.
Реальные кристаллы всегда содержат
несовершенства (дефекты) кристаллического
строения, которые нарушают связи между
атомами и оказывают влияние на свойства
металлов.
Дефекты в кристаллах
принято классифицировать по характеру
их измерения в пространстве:
К точечным дефектам
относятся вакансии, межузельные атомы,
примеси замещения, примеси чужеродных
атомов внедрения (рис. 2.5).
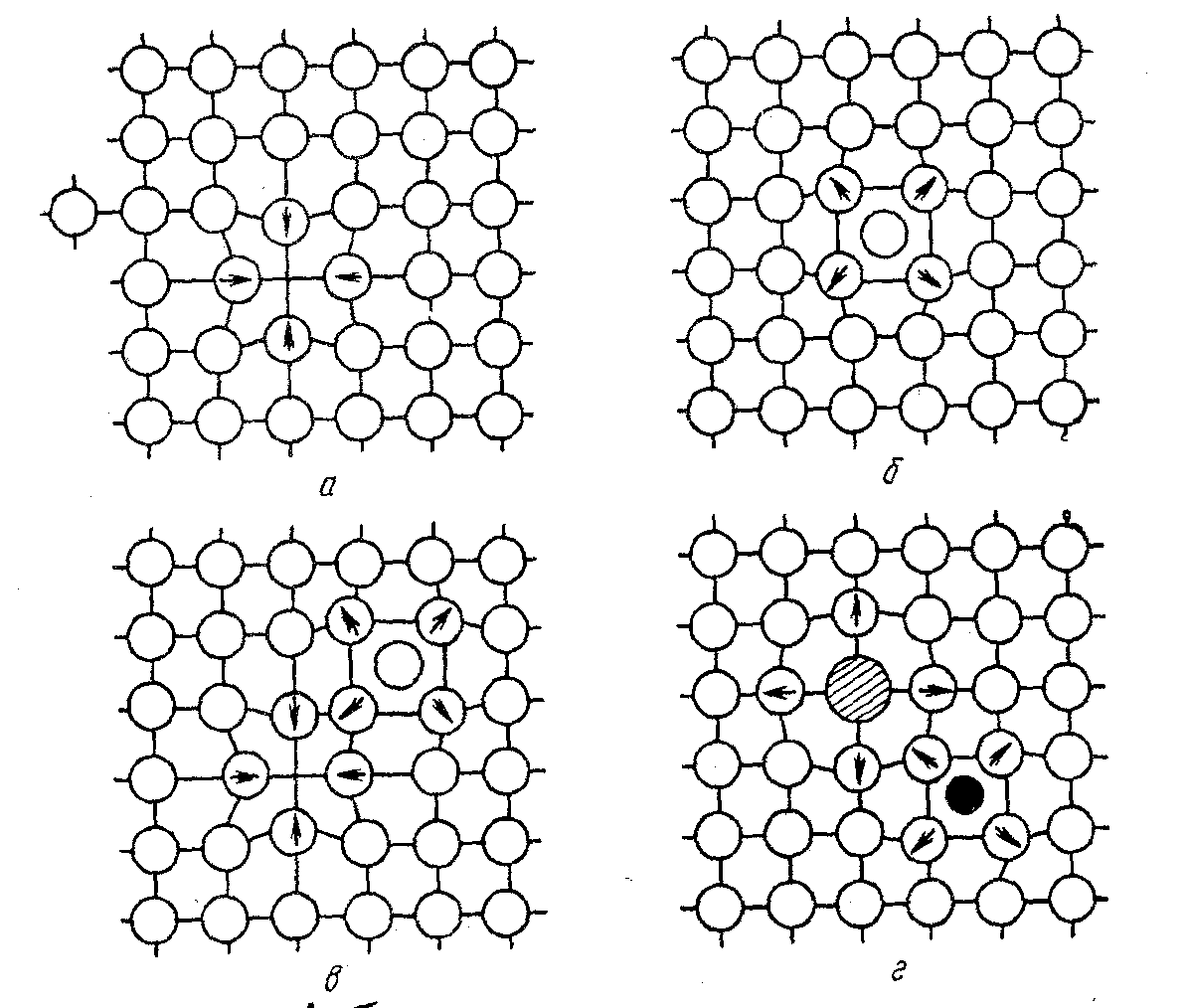
Рис.
2.5. Точечные дефекты в кристаллической
решетке: а- вакансия;
б
— межузельный атом; в- дефект Френкеля;
г- примесные атомы замещения (большой)
и внедрения (маленький).
Стрелками указаны
направления смещений атомов в решетке.
Вакансии и
межузельные атомы появляются в кристаллах
при любой температуре выше абсолютного
нуля из-за тепловых колебаний атомов.
Каждой температуре соответствует
равновесная концентрация вакансий, а
также межузельных атомов. Например, в
меди при температуре 20-25 оС
содержится 10-13 ат. % вакансий, а
вблизи точки плавления — уже 0,01 ат. %
(одна вакансия приходится на 104
атомов).
Пересыщение
точечными дефектами достигается при
резком охлаждении после высокотемпературного
нагрева, при пластическом деформировании
и при облучении нейтронами. Чем выше
температура, тем больше концентрация
вакансий и тем чаще они переходят от
узла к узлу. Вакансии являются самой
важной разновидностью точечных дефектов;
они ускоряют все процессы, связанные с
перемещениями атомов: диффузию, спекание
порошков и т. д.
2. Линейные.
Линейные дефекты в кристаллах
характеризуются тем, что их поперечные
размеры не превышают нескольких
межатомных расстояний, а длина может
достигать размера кристалла. К линейным
дефектам относятся дислокации – линии,
вдоль и вблизи которых нарушено правильное
периодическое расположение атомных
плоскостей кристалла.
Важнейшие виды
линейных несовершенств — краевые и
винтовые дислокации (рис.2.6).
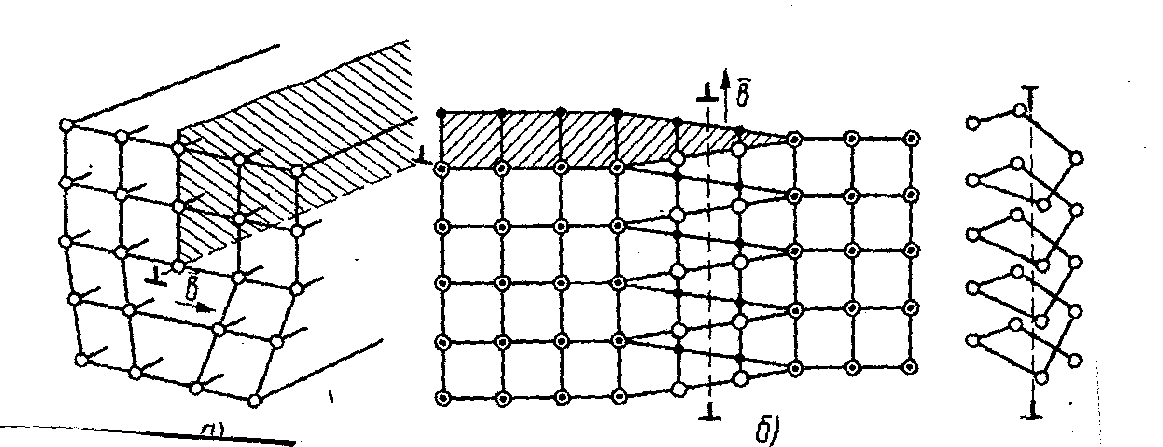
Рис.
2.6. Схема дислокаций: а – краевая; б —
винтовая
Краевая дислокация
в сечении представляет собой край
«лишней» полуплоскости в решетке
(рис.2.7)
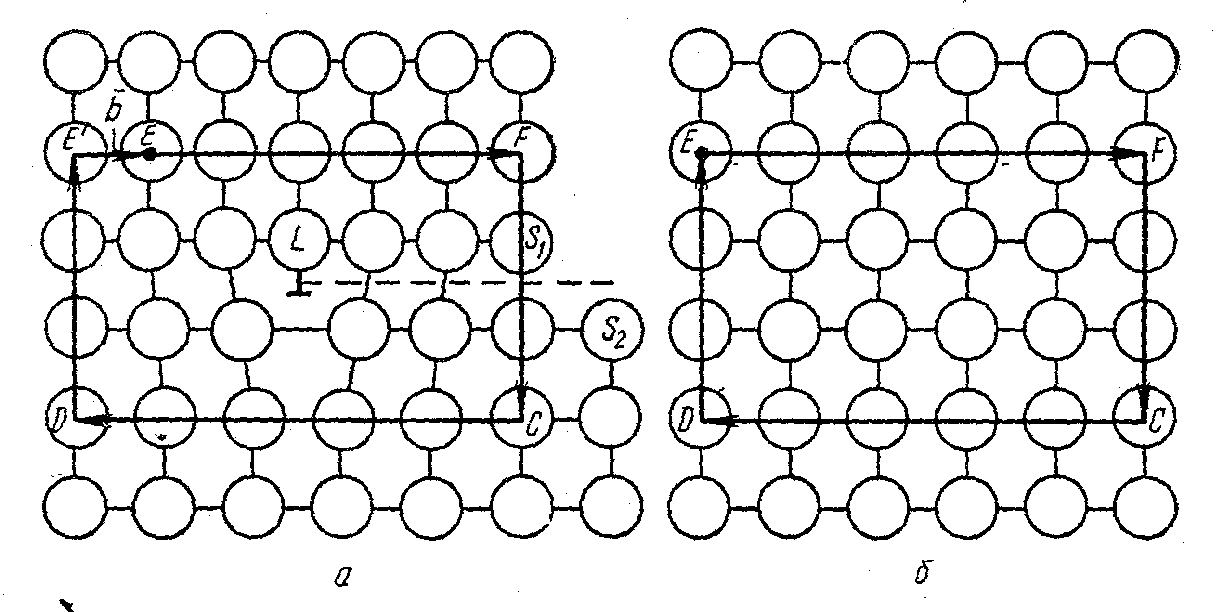
Рис.
2.7. Сечение простой кубической решетки:
а — с краевой дислокацией; б — без
дислокации.
Вокруг дислокаций
решетка упруго искажена. Схема образования
атмосферы Коттрелла в кристалле
представлена на рисунке 2.8.
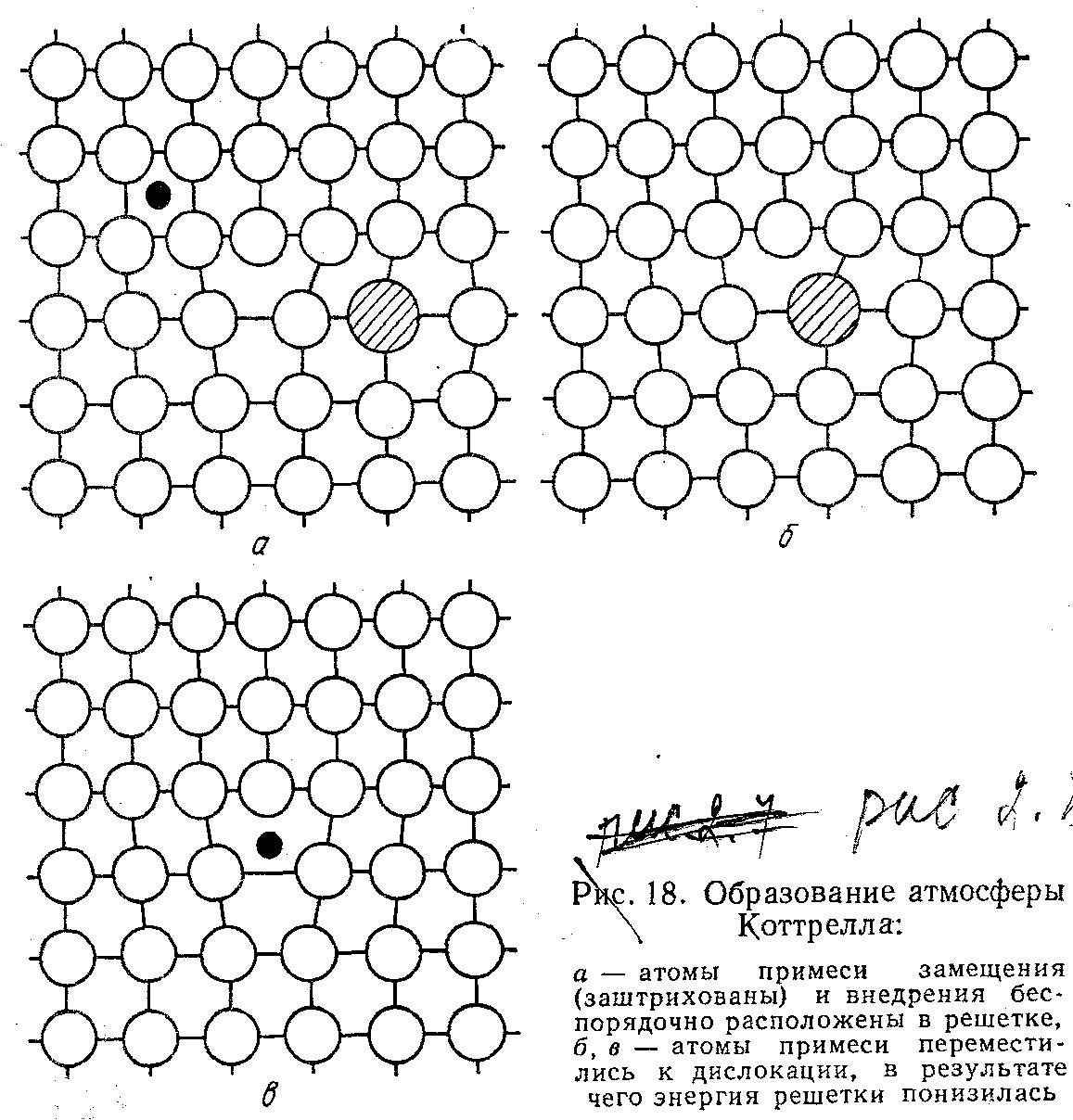
Рис.
2.8. Образование атмосферы Коттрелла: а
– атомы примеси замещения (заштрихованы)
и внедрения беспорядочно расположены
в решетке; б, в – атомы примеси переместились
к дислокации, в результате чего энергия
решетки понизилась.
3. Поверхностные
(двумерные). Под этими дефектами
понимают нарушения, которые обладают
большой протяженностью в двух измерениях
и протяженностью лишь в несколько
межатомных расстояний в третьем
измерении.
К поверхностным
дефектам относятся дефекты упаковки,
двойниковые границы, границы зерен.
4. Объемные
(трехмерные). Под ними понимают
нарушения, которые в трех измерениях
имеют неограниченные размеры. К таким
нарушениям относят трещины, поры,
усадочные раковины.
2.3. Превращения в
твердом состоянии. Полиморфизм
Атомы данного
элемента могут образовать, если исходить
только из геометрических соображений,
любую кристаллическую решетку. Однако
устойчивым, а следовательно, реально
существующим типом является решетка,
обладающая наиболее низким запасом
свободной энергии.
Так, разные металлы
образуют разные виды кристаллической
решетки:
Однако в ряде
случаев при изменении температуры или
давления может оказаться, что для одного
и того же металла более устойчивой будет
другая решетка, чем та, которая существует
при данной температуре или давлении.
Так, например, существует железо с
решетками объемно-центрированного и
гранецентрированного кубов, обнаружен
кобальт с гранецентрированной и с
гексагональной решетками.
Существование
одного и того же металла (вещества) в
нескольких кристаллических формах
носит название полиморфизма или
аллотропии. Различные кристаллические
формы одного вещества называются
полиморфными или аллотропическими
модификациями (таблица 2.1).
Все
кристаллические поверхности можно
подразделить по их термодинамическим
свойствам, атомному строению, особенностям
кинетики процессов на них на три типа:сингулярные, вицинальные и диффузные,
или несингулярные. Такую классификацию
предложили Кабрера и Франк.
Рассмотрим
классификацию с термодинамических
позиций. Возможность такого рассмотрения
основана на том, что различные
кристаллические поверхности
характеризуются различной поверхностной
энергией σ. Это означает, что поверхностная
энергия границы кристалла с любой
средой анизотропна, т. е. зависит от
кристаллографической ориентации этой
границы. Основной вклад в поверхностную
энергию вносят цепочкинаиболее
сильных связей между атомами. По этой
причинезначения
σ минимальны для тех поверхностей, в
которых находится
наибольшее число цепочек сильных
связей. Для простой кубической
решетки это, прежде всего, грани куба
(100). Они параллельны двум из трех
систем цепочек связей между первыми
ближайшими соседями и перпендикулярны
цепочкам третьей системы, а также
пересекаются всеми четырьмя системамицепочек вторых
соседей.
Грани
любой решетки, параллельные, по крайней
мере, двум системам цепочек наиболее
сильных связей, называют F-гранями;
грани,
параллельные одной такой системе, —
S-гранями; грани,
не содержащие ни одной из них, -К-гранями.
Поверхностная плотность атомов обычно
наибольшая для
F-граней,
поэтому они наиболее плотноупакованные.
ОбозначенияF,
S иК происходят
от начальных букв английскихслов
flat
(плоский), stepped
(ступенчатый) и kinked
(покрытый изломами). Для
термодинамического анализа используют
зависимость поверхностной энергии от
наклона при ориентации
поверхности Р
(рис. 6.4).
Рис.6.4. Зависимость
энергии поверхности от ее кристаллографической
ориентации
Поверхности,
которым на зависимости поверхностной
энергии от ее ориентировкиР
отвечает острый минимум или излом
(рис. 6.4, Р=0 и
р
= ±рo),
называются
сингулярными.
Направления в непосредственной близости
от ориентировки для
сингулярной поверхности соответствуют
вицинальным поверхностям. Для случая
вицинальных
поверхностей поверхностная
энергия практически линейно изменяется
с изменением
ориентировки поверхности.
Диффузная, или несингулярная,
поверхность
характеризуется тем, что ее поверхностная
энергия плавно
изменяется с изменением ориентировки.
С
позиций атомного строения сингулярная
поверхность представляет собой
гладкую поверхность, на которой атомы
поверхности располагаются в одной
плоскости (рис. 6.5). Вицинальная поверхность
состоит из плоских террас, высота
которых зависит
от наклона этой поверхности к сингулярной.
Диффузная
поверхность характеризуется наличием
изломов. Изломы на такой поверхности
распределены по всей площади равномерно
и имеют значительно большую плотность,
чем навицинальных
гранях.
Различия
рассмотренных типов поверхностей
существенно влияют на процесс роста
кристалла. Сингулярная поверхность
может расти только за счет движения
атомного слоя вдоль поверхности, тогда
как несингулярная граница раздела
междуфазами может
перемещаться в направлении,
перпендикулярном поверхности.
Всем ориентировкам с рациональными
миллеровскими
индексами должны соответствовать
острые минимумы
на диаграмме изменения поверхностной
энергии от ориентировки, и
соответствующие им поверхности должны
быть сингулярными.
Рис.6.5.
Схемы профилей кристаллической
поверхности:
а
— сингулярная; б
– вицинальная; в
– диффузная
Поверхности
с другими ориентировками являются
в этом случае вицинальными. Однако
большинство из этих острых минимумов
размывается из-за колебаний атомовуже
при очень низких температурах, и
сохраняются лишь наиболее
важные минимумы, соответствующие
поверхностям с более высокой симметрией
решетки. В общем случае для всех граней
должна существовать критическая
температура, выше
которой исчезает острый минимум
поверхностной энергии; область
перехода в этом случае увеличивается
бы от одного до нескольких атомных
слоев. Чаще всего все поверхности
по своей атомной структуре подразделяются
на атомно-гладкие
(рис. 6.6, а) и
атомно-шероховатые (рис.6.6, б).
Атомно-шероховатой
называют поверхность, на которой доля
поверхностных
узлов, занятых атомами и вакансиями, в
первом
приближении составляет ~50%.
Рассмотрим
однокомпонентный кристалл с простой
кубической решеткой, граничащей
с паровой фазой. В случае атомно-гладкой
поверхности граница между фазами
составлена плоскостями, в которых
идеальная упаковка атомов (или молекул)
нарушена вакансиями и адсорбированными
атомами. Края
недоукомплектованных плоскостей
образуют ступени. Следовательно,
поверхности, ориентировка которых мало
(на несколько
градусов) отличается от ориентировки
поверхностей с плотнейшей
упаковкой, должны быть ступенчатыми всилу геометрической
необходимости.
Ступень — одномерная
система и при
температурах, отличных от абсолютного
нуля, должна быть не прямолинейной,
а извилистой, поскольку вследствие
теплового движения атомы или молекулы
могут покидать торец ступени (как и
поверхностный слой) и переходить
либо в окружающую среду, либо на
поверхность.

Рис.
6.6. Схема атомной структуры поверхности:
а
– атомно-гладкая поверхность;
б
– атомно-шероховатая
Извилистость
определяется изломами (рис. 6.6, а). Присоединение новой частицы к излому
не ведет к его исчезновению и потому
изломы называют активными местами
роста. Это означает, что к излому
присоединяетсябольшинство
частиц, встраивающихся в кристаллическую
решетку.
Аналогичный
анализ структуры границы раздела
кристалл
— расплав требует уже определенной
модели для жидкой фазы.
Наиболее
проста решеточная модель, когда атомы
жидкости считаются расположенными в
той же решетке, что и в кристалле, но
энергия их связей между собой Eж-жотлична от энергий связи атомов в
кристаллеЕк-к и на
поверхностираздела
кристалл —
жидкость
Ек-ж.
Для
рассматриваемой однокомпонентной
системы кристалл
— расплав при постоянном давлении
в условиях фазового равновесия
температура поверхности (и кристалла)
равна температуре плавления. Равновесная
структура поверхности в этом случае
будет либо гладкой, либо шероховатой.
В бинарной системе ситуация иная:
меняя концентрацию компонентов расплава,
можно менять как равновесную температуру,
так иэффективную
поверхностную энергию. Это может
изменить атомную структуру поверхности
кристалла. Расчеты для границы
раздела однокомпонентный
кристалл —
идеальный бинарный растворпоказали, что, действительно, на линии
ликвидуса фазовой диаграммы существует
такая точка, по однусторону
от которой поверхность атомно-шероховатая,
а по другую —
атомно-гладкая.
Процесс
роста кристаллов с атомно-гладкими
гранями происходит
послойно путем тангенциального движения
ступеней, причем непрерывность
роста реализуется путем возникновенияступеней. Шероховатая
поверхность равномерно покрыта
изломами, и присоединение новых
частиц происходит на ней практически
в любом месте; грань растет в
перпендикулярном
направлении — нормальный
механизм роста.
Соседние файлы в папке Конспект лекций
Рельеф поверхности кристалла
Истинная структура поверхности кристаллов очень отличается от идеализированного представления о ней.
Поверхность реального кристалла — это совсем не плоская, идеально гладкая, безупречно чистая граница кристалла. В действительности на поверхности множество чужеродных атомов, которые адсорбировались из газовой фазы либо вышли на поверхность из твердой фазы. Рельеф реальной поверхности богат различными отклонениями от идеальной гладкости. Только при низких температурах поверхности, ограняющие кристалл, могут быть гладкими. При высоких температурах эти поверхности покрываются системой одноили многоатомных ступеней и изломов на них. Так ведут себя поверхности кристалла, которыми он огранен, в случае равновесной формы. В отношении гладкости это лучшие поверхности. А на поверхностях произвольного сечения кристалла кроме неровностей на атомном уровне возникают еще и макроскопические ступени «естественной» шероховатости.
Рассказать об этих деталях поверхностного рельефа необходимо, так как они в существенных чертах определяют закономерности поверхностной диффузии.
Вначале о деталях рельефа поверхностей, ограняющих кристалл равновесной формы, о том, почему они появляются и как их можно увидеть.
Появляются они потому, что не появиться не могут, поскольку с ростом температуры степень беспорядка в кристалле должна возрастать. В объеме кристалла этих беспорядок проявляется в образовании вакансий и межузельных атомов, а на поверхности — в образовании атомного рельефа. Он возникает вследствие того, что отдельные атомы, устилавшие гладкую поверхность, при низкой температуре перескакивают на поверхность в состояние адсорбции. В данном случае речь идет о состоянии, при котором атом, не окруженный соседними атомами, оказывается на гладком участке поверхности. Иногда эти адсорбированные атомы называют «адатомами». Второму атому вслед за первым, который ранее находился рядом, перейти в состояние адсорбции уже легче. В этом процессе, определяемом термическими флуктуациями, формируется рельеф поверхности и возникают одиночные адсорбированные атомы (рис. 16). Об этом рельефе иногда говорят так: термические разрушения поверхности.

Рис. 16. Элементы структуры «термически разрушенной» поверхности. Рядом с каждым атомом на поверхности указано число ближайших соседей.
Рельеф «естественной» шероховатости обусловлен иными причинами и образуется поиному. Равновесная форма аморфного тела, например кусочка стекла, сферическая. В этом можно убедиться, нагрев в пламени газовой горелки стеклянную крупинку произвольной формы. При высокой температуре крупинка станет сферической. Такой результат опыта обусловлен тем, что при данном объеме вещества сфера имеет наименьшую поверхность, а в случае аморфного тела и наименьшую поверхностную энергию.
Ранее нам не встречалось это понятие — «поверхностная энергия». Она обусловлена тем, что у атомов на поверхности меньшее число соседей, чем в объеме кристалла или жидкости, и, следовательно, меньшее число связей. Значит, чтобы перевести атом из объема на поверхность некоторое количество связей надо порвать. Каждая связь имеет определенную прочность, и, чтобы ее порвать, надо затратить энергию. Это и означает, что с атомами на поверхности, или, попросту говоря, с поверхностью, связана энергия, которая и называется поверхностной.

Рис. 17. Структура поверхности кристалла NaCl.
В случае кристалла дело обстоит сложнее, чем в случае аморфного тела: наименьшая поверхностная энергия не обязательно соответствует наименьшей поверхности. Дело в том, что энергия поверхности кристалла зависит от ориентации этой поверхности, и поэтому задачу о наименьшей поверхностной энергии кристалл «решает» следующим образом: он принимает форму, отличную от сферической, и, значит, поверхность его при данном объеме не наименьшая но при этом кристалл ограняет себя такими плоскостями с малой поверхностной энергией, чтобы общая энергия, т. е. сумма произведений площадей поверхности на характерную для них поверхностную энергию, оказалась наименьшей. При других формах кристалла эта энергия будет большей.
Из этого следует, что для кристалла неприемлемы произвольно ориентированные поверхности, и, если такую поверхность создать принудительно, например рассечь его произвольной плоскостью, кристалл «постарается» от такой поверхности избавиться. Конечная цель при этом — восстановить равновесную форму. На пути к конечной цели имеется, однако, промежуточная возможность понизить поверхностную энергию. Эта возможность заключается в образовании ступеней «естественной шероховатости». Каждая из ступеней имеет тонкую структуру и состоит из более мелких ступеней. Эта шероховатость потому и называется естественной, что кристаллу она необходима, при ее формировании поверхностная энергия кристалла уменьшается.
Рельеф «естественной шероховатости» можно увидеть с помощью обычного оптического микроскопа, а измерить — с помощью микроскопа специальной конструкции, который называется интерферометрическим.
Здесь, пожалуй, уместно обратиться к микрофотографиям — обычным и интерферометрическим (рис. 18, 19). Изломы черных линий на интерферометрической фотографии свидетельствуют о ребристости поверхности.
На свежих поверхностях, которые не подвергались никакой обработке, после выращивания кристалла часто можно наблюдать спиралевидный рельеф. Кристаллофизики такой рельеф наблюдали задолго до того, как было понято его происхождение. Еще в 1948 г. Г.Г. Леммлейн наблюдал спиральные горки на поверхности монокристалла карбида кремния (подобная горка изображена на рис. 5). Теперь ясна причина их образования. В отличие от «равновесного» и «естественного», спиралевидный рельеф следовало бы назвать «кинетическим», подчеркнув названием его происхождение. Спиральная горка на поверхности кристалла образуется в процессе его роста вблизи области, где имеется выход винтовой дислокации на поверхность. Атомы, которые должны пристроиться к растущему кристаллу, находят себе пристанище у ступеньки, образованной дислокацией. Пристраивая к себе атомы, ступенька движется, образуя спиральный холмик. Если кристалл не растет, а испаряется, то на поверхности будет образовываться спиральная впадина.

Рис. 18. Ступени «естественной шероховатости», образующей угол 30 с плоскостью естественной огранки, на поверхности кристалла NaCl, сфотографированной в обычном (а)
и интерферометрическом (б) микроскопах. Увеличение 500.
Рис. 19. Поверхность одного из верен в поликристаллическом образце меди. Обычная (а)
интерферометрическая (б) фотографии. Увеличение 500.
холмик, и впадина — детали поверхностного рельефа, которые отчетливо чувствуют атомы, диффундирующие по поверхности.
Поверхность кристалла
У атомов, расположенных на поверхности кристалла, часть ковалентных связей неизбежно нарушается из-за отсутствия «соседей» по другую сторону границы раздела. Количество нарушенных связей зависит от кристаллографической ориентации поверхности. Например, для кремния в плоскости (111) оказывается оборванной одна из четырех связей, а в плоскости (100) — две (рис. 1.17).
Рис. 1.17. Нарушение ковалентных связей на поверхности кристалла:
а—в плоскости (100); б—в плоскости (111)
Нарушение ковалентных связей влечет за собой нарушение энергетического равновесия на поверхности. Равновесие восстанавливается разными путями:
может измениться расстояние между атомами в приповерхностном слое, т.е. структура элементарных ячеек кристалла;
может произойти захват — адсорбция — чужеродных атомов из окружающей среды, которые полностью или частично восстановят оборванные связи;
может образоваться химическое соединение (например, окисел), не имеющее незаполненных связей на поверхности, и т.п.
В любом случае структура тонкого приповерхностного слоя (толщиной несколько нанометров и менее) отличается от структуры основного объема кристалла.
Как следствие, электрофизические параметры приповерхностного слоя заметно отличаются от параметров объема, причем этот вывод не зависит от того, граничит ли кристалл с вакуумом, воздушной средой или другим твердым телом. Поэтому приповерхностный или граничный слой (часто говорят просто — поверхность или границу) следует рассматривать как особую область кристалла.
Эта область играет важную роль в микроэлектронике, поскольку элементы планарных ИС расположены непосредственно под поверхностью, а размеры рабочих областей часто соизмеримы с толщиной граничных слоев.
Поверхность кристалла, разумеется, может быть загрязнена самыми различными веществами: остатками кислот или щелочей, использованных при ее обработке, жировыми пятнами и т.п.
Строение реальных кристаллов
Реальный кристалл металла всегда отличается своим строением от идеального. Это зависит от условий кристаллизации, в результате которой может искажаться внешняя его форма. Дефекты строения подразделяются по геометрическим признакам, а именно по характеру их измерения в пространстве, на точечные (нульмерные), линейные (одномерные), поверхностные (двухмерные) и объемные (трехмерные).
Точечные дефекты – это нарушения периодичности кристаллической решетки. Размеры их во всех направлениях сопоставимы с таковыми для атомов. К ним относятся: вакансии – свободные узлы в кристаллической решетке, межузельные элементы – те, которые располагаются вне узлов решетки (рис. 1.9).
Рис. 1.9 — Типы точечных дефектов решеток
Эти искажения называют соответственно дефектами Шоттки и Френкеля. Примесные атомы – примеси замещения и внедрения. Это ядерные остовы, которые способны замещать таковые в основном металле или внедряться в свободные места (поры или междоузлия). Вакансии образуются в результате выхода ядерного остова из узла на поверхность кристалла. Дефекты Френкеля возникают вследствие трансформации ядра из равновесного положения в междоузлие. Эти искажения формируются в основном при изменении температуры и называются тепловыми вакансиями. Они вызывают местное модифицирование решетки кристалла и влияют на электропроводность и магнитные свойства металла, а также на их фазовые превращения.
Линейные несовершенства весьма малы в двух измерениях, например, по поперечным осям, т. е. не превышают расстояний между катионами, но в третьем достигают достаточно больших размеров, которые соизмеримы с длиной кристалла. Сюда входят цепочки вакансий, межузельных ядер и дислокации.
Последние являются особым и важным видом линейных дефектов. Дислокации – линии, вдоль и вблизи которых нарушено правильное периодическое расположение ионных плоскостей кристалла. Впервые представления о дислокациях были введены в 1934 году физиками Орованом, Поляни и Тейлором. Различают краевую и винтовую дислокации (рис. 1.10 и 1.11).
Краевая дислокация — локализованное искажение кристаллической решетки, вызванное появлением или наличием в ней неполной или лишней плоскости ядер, называемой экстраплоскостью (АВСD, рис. 1.10, а).
Рис. 1.10. Краевые дислокации: а – сдвиг, создавший дислокацию; б – пространственнаясхема
Винтовую дислокацию определяют как сдвиг одной части кристалла относительно другой. Такое смещение нарушает параллельность слоев атомов в кристаллической решетке. При этом кристалл превращается как бы в одну плоскость, закрученную по винту вокруг линии, являющейся границей между частями плоскости, где сдвиг уже произошел и где еще не начинался (рис. 1.11).
Рис. 1.11. Пространственная модель образования винтовой дислокации в результате неполного сдвига по плоскостям (a) и расположение ядерных остовов в ее области (б)
Обе дислокации консервативны, но винтовая не связана с одной какой-то определенной плоскостью, она перемещается по любой из них, проходящей через линию дислокации. Возможно образование частичных и смешанных дислокаций. Формирование их повышает энергию кристалла.
Характеристикой дислокационной структуры является плотность дислокаций r — суммарная длина всех ее линий в единице объема r = ål/v см-2. Ее можно определить и как число дислокаций, пересекающих единицу площади. Плотность дислокации зависит от состояния металла. В монокристаллах она равна 103 — 106 см-2, в отожженных поликристаллических металлах r = 107 — 108 см-2, после холодной деформации ее значение увеличивается до 1011 — 1012 см-2.
В кристаллах встречаются и так называемые смешанные дислокации. Дислокации не могут обрываться внутри кристалла — они должны быть либо замкнутыми, либо выходить на поверхность кристалла. Плотность дислокации, т. е. число линий дислокации, пересекающих внутри металла площадку в 1 см2, составляет 103 — 104 в наиболее совершенных монокристаллах до 1012 в сильно деформированных металлах. Дислокации создают в кристалле вокруг себя поля упругих напряжений, убывающих обратно пропорционально расстоянию от них. Наличие упругих напряжений вокруг дислокации приводит к их взаимодействию, которое зависит от типа дислокации и их векторов Бюргерса. Под действием внешних напряжений дислокации двигаются (скользят), что определяет дислокационный механизм пластической деформации. Перемещение дислокации в плоскости скольжения сопровождается разрывом и образованием вновь межатомных связей только у линии дислокации, поэтому пластическая деформация может протекать при малых внешних напряжениях, гораздо меньших тех, которые необходимы для пластической деформации идеального кристалла путем разрыва всех межатомных связей в плоскости скольжения. Обычно дислокации возникают при образовании кристалла из расплава. Основным механизмом размножения дислокации при пластической деформации являются так называемые источники Франка-Рида. Это отрезки дислокации, закрепленные на концах, которые под действием напряжений могут прогибаться, испуская при этом дислокации, и вновь восстанавливаться.
Поверхностные искажения – нарушения в кристаллической решетке по поперечным плоскостям и связям, т. е. в двух направлениях наблюдается большая протяженность кристаллов, а длина очень маленькая. Это дефекты упаковки, двойниковые границы, границы зерен и внешние поверхностные кристаллы.
Дефекты упаковки – локальные изменения расположения плотноупакованных плоскостей в кристалле.
Двойникование – образование двойников, симметричная переориентация областей решетки. Обычно она осуществляется в том случае, когда затруднена деформация путем движения дислокаций.
Объемные дефекты – искажения решетки во всех трех ее направлениях. Это трещины, поры и др.
Вопросы для самопроверки
1. Дайте определение металлов по Ломоносову, Майеру и современное.
2. На какие две группы подразделяют металлы по окраске? Перечислите металлы входящие в них.
3. Приведите классификацию цветных металлов по некоторым их физико-механическим параметрам.
4. Что такое кристаллическое строение вещества?
5. Какие кристаллические решетки характерны для металлов?
6. Что называется периодом и координационным числом кристаллической решетки?
7. Сколько ядерных остовов приходится на элементарную ячейку гранецентрированной, объемноцентрированной кубической и гексагональной плотноупакованной решетки?
8. Напишите кристаллографическое обозначение плоскостей куба и индексы их направления
9. Что такое полиморфное превращение, какие условия необходимы для его протекания и как оно осуществляется?
10. Какие Вы знаете дефекты кристаллической решетки?
11. Что такое дислокации? Чем отличаются ее разновидности друг от друга и как они влияют на свойства металла?
12. Какие Вы знаете поверхностные несовершенства в поликристалле?
Перекати-поле и двумерный газ
О перекати-поле в толковом словаре можно прочесть, что это степное растение, при высыхании отрывающееся от корня и переносимое ветром в виде шаровидного кустика на большие расстояния. Кустик может надолго застрять у случайно встреченного пригорка или долгое время пролежать в ложбине, а затем очередной порыв ветра покатит его в новом направлении. А там опять горка или ложбинка и опять — ожидание случайного порыва ветра.
В судьбе перекати-поля и атомов на поверхности кристалла много общего. Не тех атомов, которые, плотно прижавшись друг к другу, образуют поверхностный слой кристалла, а атомов, которые, случайно выскочив из этого слоя или осев на него из окружающей среды, оказались на поверхности кристалла в одиночестве. В роли «адатомов» могут быть атомы не данного кристалла, а иного вещества. Эти атомы, как и перекати-поле, подвержены воле случая: случайная флуктуация энергии может заставить каждого из них совершить элементарный диффузионный скачок. Его длина может оказаться большей, чем межатомное расстояние. И, как в случае шаровидного кустика, направление последующего скачка совсем не зависит от направления предыдущего.
И на пути атома встречаются «пригорки» и «ложбинки» в виде деталей структуры поверхности: террас, ступеней и изломов на них. Пристроившись к этим деталям структуры, атом может надолго остановиться.
Как и множество других аналогий, аналогия между атомом и кустиком перекати-поля
неполна, неглубока. Все похоже, только ветер дует длительное время, а катящийся кустик останавливается только у препятствий. Энергетическая же флуктуация кратковременна, и запаса энергии, который при этом сообщается атому, может не хватить на то, чтобы атом проскользнул от препятствия к препятствию. Атом может остановиться «во чистом поле», т. е. на участке атомно гладкой поверхности, в ожидании очередной порции энергии. Возможно, точнее будет сказать: в ожидании случайного изменения взаимного положения соседних атомов, которое сопровождается выделением энергии. Длительность такой остановки значительно меньше, чем у препятствия, или, вернее, ловушки. Атом может постичь и иная участь: испарившись, он покинет поверхность и перейдет в газовую фазу, окружающую кристалл. В условиях, когда кристалл и газовая фаза находятся в равновесии, количества атомов, покидающих поверхность и падающих на нее из газовой фазы, равны.
Совокупность скачков — скольжений по поверхности — и является процессом двумерной поверхностной диффузии атомов. Очевидно, как и в случае «бесцельной» объемной самодиффузии, среднее смещение атома, который по воле случая скользит по поверхности, подчиняется определенному закону.
А вот другая аналогия, которую развивал Я. И. Френкель. Исследуя закономерности поверхностной диффузии, он прибегал к образу «двумерного газа». Мы привыкли к обычному, трехмерному газу, а у него двумерный газ: совокупность адатомов, хаотически движущихся по поверхности (рис. 20). Ступеньки па поверхности кристалла по отношению к двумерному газу (а) играют ту же роль, что и поверхность кристаллов для трехмерного газа (б). Эти атомы, скользя, могут сталкиваться друг с другом, и, если их миграция бесцельна, в среднем число атомов на единице поверхности будет на всех участках одинаково, как одинакова плотность трехмерного газа в сосуде. Двумерный газ, находящийся по одну сторону перегородки, должен оказывать «двумерное» давление на перегородку, и его поведение должно подчиняться «двумерному» закону Бойля-Мариотта. Эти две аналогии, видимо, создадут зримое представление о двумерной, «бесцельной» диффузии атомов, адсорбированных на поверхности кристаллов.
Рис. 20. Схема двумерного (а) и трехмерного (б) газа.
Теперь о коэффициенте поверхностной диффузии. Для того чтобы адсорбированный атом принял участие в диффузионной миграции вдоль поверхности, он, во-первых, должен образоваться, т. е. оторваться от излома на ступени, и, во-вторых, приобрести энергию, необходимую для совершения элементарного скачка. Таким образом, вероятность наблюдать случайное событие — элементарный скачок адатома в данной точке на поверхности — есть произведение вероятностей двух случайных событий: образования адатома и приобретения им надлежащей энергии для скачка. Последующие рассуждения подобны тем, которые излагались в очерке о «бесцельной» самодиффузии с помощью вакансионного механизма. Эти рассуждения приведут к почти очевидной формуле, которая устанавливает связь между коэффициентом поверхностной диффузии D), коэффициентом диффузии адатомов () и их концентрацией ():
Формула, совершенно подобная уже известной нам формуле, которая связывает коэффициент объемной диффузии атомов, вакансий и концентрацию вакансий. Подобна, но
Соседние файлы в папке Волошко
Механизмы и формы роста кристаллов
После образования центров кристаллизации рост кристаллов осуществляется путем последовательного присоединения атомных слоев на поверхности образовавшихся зародышей (рис. 2.9).
Рост кристалла происходит за счет появления на поверхности кристалла двухмерного зародыша (рис. 2.9, а), который может иметь размеры меньше или больше критического.
Рис. 2.9. Рост кристалла на атомно-гладкой поверхности: а – одиночный атом на поверхности; б – присоединение атома к ступеньке; в – присоединения атома к излому на ступеньке.
Механизм роста зависит от атомного строения границы раздела кристалл–жидкость. Используют представление о двух крайних типах этого строения: атомно-гладкой и атомно-шероховатой границе.
При образовании двухмерного зародыша происходит изменение свободной энергии системы за счет фазового перехода и увеличения ее за счет образования дополнительной поверхности раздела, т.е.
Таким образом, эта функция оказывается аналогичной для рассмотренного выше трехмерного зародыша, т.е. для условий роста кристалла путем присоединения двухмерного зародыша на плоскость ранее образовавшегося кристалла существует такой размер двухмерного зародыша, меньше которого он оказывается неустойчивым и растворяется. Такой слой называется критическим двумерным зародышем.
При малых степенях переохлаждения размер критического двумерного зародыша велик, поэтому возникающих двумерных зародышей весьма мало, и рост кристаллов в этих условиях происходит очень медленно.
Чем больше степень переохлаждения, тем меньше линейные размеры двумерного зародыша и тем меньшее значение энергии требуется для его образования, с увеличением степени переохлаждения скорость роста кристаллов возрастает, т.е. кривая линейного роста кристаллов аналогична кривой количества центров кристаллизации, возникающих в единицу времени.
В случае атомно-гладкой границы все позиции атомов поверхностного слоя кристалла заняты. Одиночный атом на гладкой поверхности слабо связан с кристаллом. После возникновения двумерных зародышей рост кристалла протекает с наименьшими энергетическими затратами. Наиболее благоприятным участком является тройной пространственный угол, где для присоединения новых решеток требуется минимальная площадь дополнительно образующейся границы кристалла. Такое присоединение происходит до полной достройки атомного слоя; дальнейший рост возможен только после появления нового двумерного зародыша.
Важную роль в процессе роста кристалла играют дефекты кристаллов, в частности винтовая дислокация. При этом рост кристалла происходит путем заполнения ступеньки по винтовой линии, когда ступенька в течение всего цикла не исчезает, а только перемещается, обеспечивая непрерывный рост кристалла без образования двумерных зародышей.
Рис. 2.10. Строение атомно-шероховатой поверхности раздела кристалл–жидкость (d – граница раздела).
На атомно-шероховатой границе раздела происходит постепенный переход от структуры расплава к структуре кристалла. На схеме (рис. 2.10) пунктир условно отделяет атомы, принадлежащие жидкой фазе, от атомов твердой фазы. Фактически же граница является размытой и имеет ширину несколько атомных диаметров.
На атомно-шероховатой границе имеется множество мест, где атомы из жидкости могут присоединяться к кристаллу. Рост кристалла с атомно шероховатой поверхностью называют непрерывным (он идет во множестве точек по всей поверхности кристалла) или нормальным (граница раздела перемещается в направлении нормали к ней, без участия тангенциального роста каждого слоя).
Степень шероховатости кристалла связана с энтропией плавления. У металлов энтропия плавления низкая, граница кристалл–расплав является атомно-шероховатой и основной механизм роста кристалла непрерывный (нормальный). У висмута и сурьмы, большинства карбидов и многих других химических соединений энтропия плавления высокая, граница кристалл–расплав атомно-гладкая и основной механизм роста кристалла ступенчатый.
Кинетика кристаллизации, т.е. изменение количества закристаллизовавшегося металла во времени (рис. 2.11) зависит от количества возникающих центров кристаллизации и скорости их роста.
Рис. 2.11. Кинетические кривые развития кристаллизации в зависимости от степени переохлаждения: 1 – минимальная степень переохлаждения; 5 – максимальная.
Чем больше количество зародышей и линейная скорость их роста, тем больше количество закристаллизовавшегося вещества.
Величина кристаллизационных параметров зависит от степени переохлаждения (рис. 2.11). При очень малых степенях переохлаждения кристаллизация протекает очень медленно, и начинается не сразу, а по прохождению некоторого промежутка времени, называемого инкубационным периодом (кривая 1).
Увеличение степени переохлаждения приводит к уменьшению длительности инкубационного периода и увеличению скорости кристаллизации (кривые 2, 3, 4, 5). Скорость кристаллизации в начальный период минимальна, увеличивается со временем, достигает максимума и затем понижается (рис. 2.11, нижняя часть).
Факторы, оказывающие влияние на кинетику кристаллизации и размер зерен, оказывают влияние и на их форму. В условиях, близких к равновесию, образуются правильно ограненные кристаллы. Они растут медленно, поверхность их гладкая, хотя и содержит необходимые для застройки граней ступеньки (рис. 2.12).
С увеличением степени переохлаждения межфазная поверхность становится неровной, на поверхности металла появляется множество ячеек, средняя часть которых несколько выдвигается в расплав (рис. 2.12, б).
Рис. 2.12. Формы роста кристаллов в расплаве при кристаллизации: а – плоский (ограненный) кристалл; б – столбчатый ячеистый; в – дендритный: цифры у осей – соответственно, оси первого, второго и третьего порядков
Появление ячеистой структуры зависит от наличия в расплаве примесей и их перераспределения. При постоянном теплоотводе от поверхности отливки в первую очередь кристаллизуются наиболее чистые (по содержанию примесей) участки жидкого металла, в связи с чем наблюдается выдвижение фронта кристаллизации в расплав. Объемы жидкого металла, наиболее загрязненные примесями, оттесняются в появившиеся впадинки на фронте кристаллизации, затвердевают в последнюю очередь и образуют границы ячеек. Выращенный в таких условиях кристалл приобретает столбчатую, вытянутую в направлении теплоотвода форму, напоминающую связку карандашей, боковые поверхности которых соответствуют обогащенным примесями границам зерен.
При еще большем увеличении степени переохлаждения, что достигается увеличением теплоотвода от кристаллизирующейся жидкости, выступы на межфазной границе становятся настолько большими, что жидкость между выступами значительно отстает по темпу затвердевания от выступающих частей кристалла. Наступает так называемый дендритный тип кристаллизации.
Образовавшиеся длинные выступы становятся осями первого порядка. При возникновении на поверхности этих осей неровностей (выступов) появляются новые направления возможного роста кристалла, т.е. оси второго, третьего порядка и т.д. Кристалл в процессе роста напоминает дерево в среде жидкого металла. Если обеспечить слив металла, не закристаллизовавшегося к данному моменту времени, то можно получить дендрит в чистом виде – иллюстрацию для изучения дендритного роста кристаллов (дендрит Чернова).
Наслаивание металла на образовавшиеся оси первого, второго и т.д. порядков при последующей кристаллизации приводит к заполнению всего междендритного пространства и образованию сплошного кристалла. Однако образующие сплошной кристалл слои металла, появившиеся в различные моменты кристаллизации, отличаются по содержанию примесей. Оси формируются наиболее чистым металлом, участки, закристаллизовавшиеся в междендритном пространстве в последнюю очередь, наиболее сильно загрязнены примесями.
Дендритный рост кристаллов объясняется следующим образом. Наиболее стабильным кристаллом, например металла с ГЦК-решеткой, является кристалл, образованный наиболее плотно упакованными плоскостями (111).
Такой кристалл имеет форму октаэдра (рис. 2.13).
Рис. 2.13. Начальные этапы дендритного роста кристаллов: а – рост совершенного ограненного кристалла в виде октаэдра;
б – образование отростков (дендритных осей первого порядка).
Грани октаэдра обладают минимальной свободной энергией. Вершины октаэдра, как правило, обладают значительным количеством дефектов кристаллического строения, повышенной свободной энергией. В связи с этим уже на ранних этапах роста октаэдрический кристалл отбрасывает шесть отростков в трех взаимно перпендикулярных направлениях. Эти отростки превращаются в оси первого порядка, ответвления от которых образуют оси второго, третьего и т.д. порядков.
Ускоренный рост выступающих участков дендрита обусловлен несколькими причинами: во-первых, особенности упаковки атомов и преимущественное расположение выходов дефектов кристаллического строения на поверхности этих участков влияют на их рост.
Во-вторых, выступающие участки кристалла соприкасаются с большим объемом жидкости, приходящейся на единицу их поверхности. За счет этого быстрее рассеивается теплота кристаллизации, выделяющаяся на фронте затвердевания. При этом оказывается, что острие соприкасается с более охлажденным металлом, чем около боковых поверхностей, в связи с чем кристаллизация оказывается более выгодной у острия.
В-третьих, сказывается влияние примесей. Накапливаясь в жидком металле у вогнутых участков кристалла, примесь тормозит их рост. Рост же острых выступов, соприкасающихся с расплавом исходного состава, не задерживается.

