В
заместительной номенклатуре соединение
рассматривается как полученное в
результате
замещения атома водорода в исходной
структуре на функциональную
(характеристическую)
группу.
При
составлении названия соединения с
известной структурой следует
последовательно решать следующие
задачи:


СН3-СН2-СН2-СН2-СOOH
пентановая кислота

СН3-CН2-СN
пропаннитрил

—
СN
бензолкарбонитрил
СН3-С=O
этаналь

-C=O
фуранкарбальдегид
2.
Определить
главную характеристическую группу,
руководствуясь разработанной ИЮПАК
их иерархией (в таблице 1 они размещены
по уменьшению старшинства).
Эта
главная группа, и только она одна,
указывается в суффиксе, все остальные
называются
в префиксе в порядке алфавита.
Главная группа лежит в основе всего
названия и нумерации, поэтому она
выбирается прежде всего.
Некоторые классы
соединений, расположенные в порядке
уменьшения
старшинства групп,
используемых
в качестве главной
группы.
Ряд
групп (табл. 2) всегда указывается в
префиксе. Они не могут выступать в
качестве главных групп.
Если таких заместителей несколько, их
названия в префиксе располагаются по
алфавиту, причем в общем алфавитном
ряду перечисляются неглавные
характеристические группы и боковые
цепи (углеводородные радикалы).
Некоторые
группы, указываемые только
в префиксах.
3.
Определить родоначальную структуру,
т.е. главную цепь в алифатической
молекуле, циклическую или гетероциклическую
систему, лежащие в основе называемого
соединения. Родоначальную
структуру нужно выбрать из той части
скелета, к которой непосредственно
примыкает старшая характеристическая
группа.

5
— фенилнафталинкарбоновая кислота

Определение
родоначальной структуры не всегда
проходит гладко, иногда приходится
учитывать дополнительные факторы.
Например, для алифатических соединений
нужно придерживаться следующих критериев
(по их старшинству):
1) Максимальное
число старших характеристических групп.
НО
— СН2
— СН2
— CH — CH2
ОН
2-(2-хлорэтил)бутандиол-1,4
2) Максимальная
суммарная ненасыщенность
1
2 3 4 5 6
7 8 9 10
СН2
= СН — СН = СН — СН — С
С — СН = СН — СН3
1
2 3 4 5
6
СН2
— СН2
— СН2
— СН2
— СН = СН2
3) Максимальная
длина цепи
НООС
— СН2
— С — СН2
— СООН
лимонная кислота
3-гидрокси-3-карбоксипентандиовая
СООН
кислота
Отметим,
что этот признак занимает весьма скромное
место.
4.
Определить порядок нумерации.
Нумеруют
так, чтобы старшая
характеристическая группа получила
наименьший
из
возможных номеров.
Вообще же, для алифатических соединений
рекомендуется давать наименьшие номера
следующими элементам структуры,
последовательно используя ниже
перечисляемые признаки:
— атомы и
неглавные группы, обозначаемые префиксами
— префиксные
группы в порядке перечисления по
алфавиту.
При
этом нужно еще придерживаться правила
наименьших локантов.
5.
Дать названия родоначальной структуре
и основным группам, затем названия
префиксам (таблица 3).
Принятые
ИЮПАК обозначения
в префиксах и суффиксах
некоторых
важнейших групп. ( Классы расположены
в порядке уменьшения старшинства
групп,
используемых в качестве главной
группы)
*
Заключенный в скобки атом
углерода входит в название родоначального
соединения
( углеродный скелет ), а не в префикс
или суффикс ( характеристическую
группу ).
6.
Объединить частичные названия в общее
полное название, придерживаясь общего
алфавитного
порядка для всех отделяемых префиксов;
локанты
ставятся перед
префиксом,
но после суффикса.
Причем
для двух возможных последовательностей
локантов считается меньшей та, в которой
первой (первое различающееся место)
встречается цифра меньшая, чем в другой
последовательности.
10
9 8 7 6
5 4 3 2 1
СН3
— СН2
— СН — СН — СН2
— СН2
— СН2
— СН2
— СН — СН3
СН3
СН3
СН3
Составными
частями заместительных названий
являются также известные умножающие
приставки
(ди-, три-, тетра-, пента- и т. д. для простых
фрагментов и бис-, трис-, тетракис- — для
сложных), суффиксы
-ан, -ен, -ин
— для обозначения степени ненасыщенности,
названия
радикалов
(метил-, этил-, пропил-, изопропил-,
бутил-, изобутил-, втор-бутил-,
трет
-бутил-,изопентил-, неопентил-, трет-пентил-,
изогексил-).
Умножающие
приставки не учитываются при расстановке
префиксов в алфавитном порядке. Не
учитываются также при этом курсивы
(цис-,
транс-, экзо-, эндо-, эритро-, трео-, втор-,
трет- и
др.)
1
2 3 4 5
Н2N
— СН2
— СН — СН — СН2
— СН2
— NН2
2,3-диметилпентандиамин-1,5
CH3
CH3
2
1
СН3
— СН2
— СН — СН2
ОН
3
4 5
2-этилпентанол-1
CH2
— CH2
— CH3
4 3
2 1
СН3
— СН = С — СН2
— ОН
2-пропилпентен-2-ол
-1
СН2
— СН2
— СН3
1 2
3 4 5 6
СН3
— СН2
— СН — СН2
— СН2
— СН3
гексанол-3
1 2
3 4 5 6
СН3
— СН2
— С — СН — СН2
— СН3
4-гидроксигексанон-3
О ОН
6
5 4 3 2 1
СН3
— СН2
— СН2
— СН2
— С = СН2
2-этилгексен-1
1
2 3 4 5
СН2
— СН = СН — СН2
— СН — СН3
6
7
5-метилгептен-2
1 2
3 4 5 6
СН3
— СН2
— СН — СН — СН2
— СН3
гександиол-3,4
ОН ОН

СН3
— СН2
— СН2
— СН2
— СН — СН2
ОН
3
4 5
СН2
— СН — СН3
2-бутилпентандиол-1,4
8
7 6 5 4 3
2 1
НО
— СН2
— СН2
— СН2
— СН2
— СН — СН = СН — СН2
ОН
СН2
— СН2
— СН2
— СН2
ОН
2
1
СН3
— СН2
— СН2
— СН2
— СН — СOOH бутилянтарная
3
4
2-бутилбутандиовая-1,4
СН2
— СOOH кислота




1 2
3 4 5 6
СН3
— С — С = СН — СН — СН2
ОН
6-гидрокси-5-метил-3-хлорогексен-3-он-2
О
Сl СН3
1
2 3 4 5 6
7 8
НОСН2
— СН = СН — СН = СН — СН = СН — СН2
ОН

2-метилпропанол-2
СН3
— С — СН3
(название
трет-бутанол-некорректно,
так как нет соединения
трет-бутана.
Можно использовать название из другой
СН3
номенклатуры (трет-бутиловый
спирт ). То же-изопропанол)
1
2
3
4
5
НО-СН2
— СН — СН — СН — СН2
Сl
3-изопропил-2-метил-4,5-дихлорпентанол-1
СН3
СН — СН3
- Номенклатура карбоновых кислот
- Примеры названия карбоновых кислот
- Для вещества, имеющего строение CH3 – CH (СН3) – CH3, составьте формулы одного изомера и двух гомологов. Дайте всем веществам названия по систематической номенклатуре.
- Для вещества, имеющего строение CH3 – CH(СН3)– CH2 – CH(СН3) – CH3, составьте формулы одного изомера и двух гомологов. Дайте всем веществам названия по систематической номенклатуре.
- 1,2-дибромпропана; 3,4-дибром-3,4-диметилгексана; 2,4-дибромпентана; 2-бром-З-хлорбутана.
- А)окислить в соответствующую карбоновую кислоту; б) превратить в эфир уксусной кислоты; в) превратить в йодистый алкил и последний восстановить до углеводорода?
- Напишите графические формул пяти изомерных аминов, содержащих бензольное ядро, состава C7H9N. Назовите их.
- Напишите графические формулы изомерных ароматических кислот состава С8Н8О2. Назовите эти соединения.
- Напишите графические формулы первичных, вторичных и третичных спиртов состава C6H13OH. Назовите их по номенклатуре ИЮПАК.
- Сколько изомерных гомологов бензола может отвечать формуле C9H12? Напишите структурные формулы изомеров и назовите их.
- Номенклатура оснований и амфотерных гидроксидов
- Номенклатура кислот и солей
- Номенклатура комплексных солей*
- Основные принципы заместительной номенклатуры органических соединений
- Определение заместительной номенклатуры
- Что такое заместительная номенклатура
- История развития заместительной номенклатуры
- Значение заместительной номенклатуры в современной химии
- Приоритет заместителей в номенклатурном префиксе
- Исключения и особенности в заместительной номенклатуре
- Положение заместителя
- Нумерация атомов
- Исторические названия
- Исключения для некоторых групп соединений
- Примеры заместительной номенклатуры
- Admin
- Правила составления названий по систематической международной номенклатуре ИЮПАК
Номенклатура карбоновых кислот
По систематической (заместительной) номенклатуре IUPAC названия карбоновых кислот образуют из названий соответствующих углеводородов с добавлением суффикса -и слова .
Правила составления названий карбоновых кислот по систематической (заместительной) номенклатуре ИЮПАК
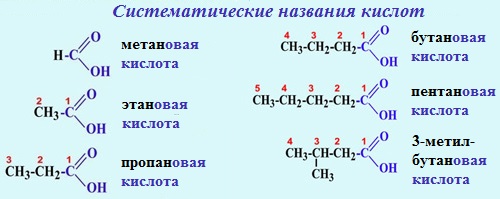
По систематической номенклатуре названия непредельных кислот образуются от названия соответствующего алкена (алкина, диена), добавляя к нему суффикса –и цифрой указывают положение двойной связи. Нумерацию углеродной цепи начинают с атома углерода карбоксильной группы.
Названия многоосновных кислот производят от названия соответствующего углеводорода с добавлением суффиксов «», — и т.д. и слова «»:
Часто карбоксильную группу рассматривают как заместитель в молекуле углеводорода. При этом в названии употребляют словосочетание «» и в нумерацию атомов углерода цепи атом углерода карбоксильной группы не включают.
Данный способ чаще применяют в случаях, когда карбоксильная группа связана с циклической структурой.
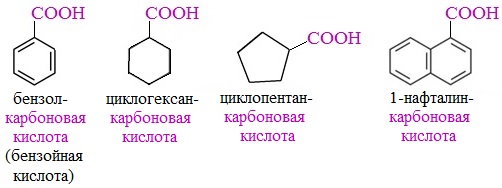
Для органических кислот широко используют тривиальные названия, которые обычно отражают природный источник, где были впервые обнаружены эти соединения (H-COOH — муравьиная кислота, CH3-COOH — уксусная кислота, CH3-CH2-CH2-COOH – масляная).
Положение заместителей по отношению к карбоксильной группе в тривиальных названиях обозначают греческими буквами, начиная с атома углерода, соседнего с карбоксильной группой: α, β, γ и др.:
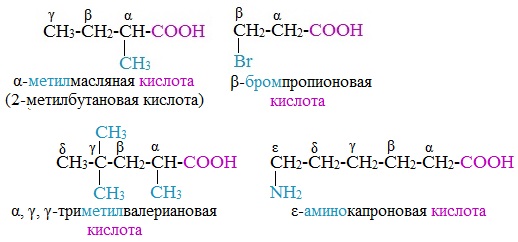
Формулы и названия важнейших карбоновых кислот по тривиальной и международной номенклатуре
По рациональной номенклатуре насыщенные монокарбоновые кислоты рассматривают как производные , ароматические – :
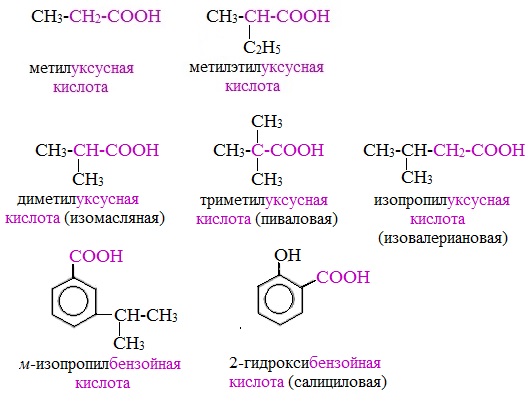
Примеры названия карбоновых кислот
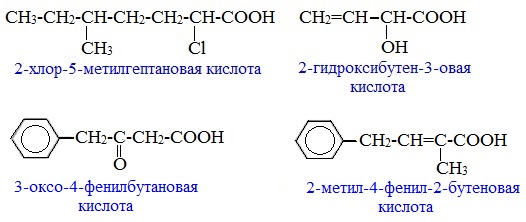
Здесь представлены типовые задачи к разделу изомерия и номенклатура органических соединений.
Для вещества, имеющего строение CH3 – CH (СН3) – CH3, составьте формулы одного изомера и двух гомологов. Дайте всем веществам названия по систематической номенклатуре.
Показать решение »
Изомеры – вещества, обладающие одинаковой молекулярной формулой, но имеющие различное строение и, вследствие этого, различные химические и физические свойства.
Гомологи – вещества, принадлежащие одному гомологическому ряду. Имеют схожее однотипное строение, и каждый последующий член гомологического ряда отличается от предыдущего на – СН2 группу.
Для вещества, имеющего строение CH3 – CH(СН3)– CH2 – CH(СН3) – CH3, составьте формулы одного изомера и двух гомологов. Дайте всем веществам названия по систематической номенклатуре.
![]()
1,2-дибромпропана; 3,4-дибром-3,4-диметилгексана; 2,4-дибромпентана; 2-бром-З-хлорбутана.
![]()
А)окислить в соответствующую карбоновую кислоту; б) превратить в эфир уксусной кислоты; в) превратить в йодистый алкил и последний восстановить до углеводорода?
Среди органических соединений есть оптически активные вещества, обладающие способностью вращать плоскость поляризации света. Такие вещества существуют в виде двух изомеров (оптических антиподов), вращающих плоскость поляризации в противоположные стороны. Пространственные формы оптических антиподов не совпадают и их совмещение невозможно. Оптическая изомерия возможно только для молекул, имеющих асимметрический атом углерода (т.е. атом углерода, связанный с четырьмя различными заместителями).
Все продукты реакций, кроме, 2-метилбутана, будут проявлять оптическую активность, связанную с наличием в молекуле асимметрического атома углерода (*С)
![]()
Напишите графические формул пяти изомерных аминов, содержащих бензольное ядро, состава C7H9N. Назовите их.
![]()
Напишите графические формулы изомерных ароматических кислот состава С8Н8О2. Назовите эти соединения.
![]()
Напишите графические формулы первичных, вторичных и третичных спиртов состава C6H13OH. Назовите их по номенклатуре ИЮПАК.
![]()
Сколько изомерных гомологов бензола может отвечать формуле C9H12? Напишите структурные формулы изомеров и назовите их.
![]()
В соответствии с номенклатурой ИЮПАК любое бинарное соединение, в котором присутствует кислород со степенью окисления -2, называют словом «оксид», затем указывают название элемента в родительном падеже. Если для элемента характерна постоянная валентность, то больше ничего указывать не нужно. Если для элемента характерна переменная валентность, то после названия необходимо указать в скобках его валентность в данном оксиде; валентность указывают римскими цифрами.
: WO3 — оксид вольфрама (VI); Li2O — оксид лития.
Если вы не знаете, что такое валентность, и как ее определять, то необходимо изучить соответствующую статью.
Номенклатура оснований и амфотерных гидроксидов
Названия оснований и амфотерных гидроксидов строятся аналогично, только вместо слова «оксид» используют слово «гидроксид«, затем указывают название металла в родительном падеже. Если для металла (или металлоподобного иона) характерна постоянная валентность, то больше ничего указывать не нужно. Если для металла характерна переменная валентность, то после названия необходимо указать в скобках его валентность в данном гидроксиде; валентность указывают римскими цифрами.
: KOH – гидроксид калия; Fe(OH)3 – гидроксид железа (III).
Номенклатура кислот и солей
Название кислот строятся так: к корню названия центрального элемента на русском языке добавляют постфиксы -ная, -нистая или -водородная, в зависимости от степени окисления центрального элемента.
Если вы не помните, что такое степень окисления, и как ее определять, то сначала необходимо изучить соответствующую статью.
Названия солей строятся так: к корню названия центрального элемента на латинском языке добавляют постфиксы -ат, -ит или -ид, в зависимости от степени окисления центрального элемента. Затем указывают название металла в родительном падеже. Если для металла (или металлоподобного иона) характерна постоянная валентность, то больше ничего указывать не нужно. Если для металла характерна переменная валентность, то после названия необходимо указать в скобках его валентность в данной соли; валентность указывают римскими цифрами.
Корни латинского названия у большинства элементов совпадают с корнями русского названия. Для некоторых элементов они отличаются. Их следует запомнить:
C – карб, S – сульф, N – нитр и др.

Рассмотрим основные случаи.
Если центральный элемент в кислоте имеет высшую степень окисления, т.е. в кислотном остатке этой кислоты содержится максимальное количество атомов кислорода, то к названию кислоты добавляют постфикс -ная или -вая.
: H2S+6O4 – серная кислота, H3P+5O4 – фосфорная кислота.
При этом в названии соли используют постфикс -ат.
Na2S+6O4 – сульфат натрия, K2C+4O3 – карбонат калия.
Если центральный элемент в кислоте имеет промежуточную степень окисления, т.е. в кислотном остатке этой кислоты содержится не максимальное количество атомов кислорода, то к названию кислоты добавляют постфикс -нистая.
: H2S+4O3 – сернистая кислота, H3P+3O3 – фосфористая кислота.
При этом в названии соли используют постфикс —ит.
, Na2S+4O3 – сульфит натрия, KN+3O2 – нитрит калия.
Если центральный элемент в кислоте имеет низшую степень окисления, т.е. в кислотном остатке этой кислоты не содержатся атомы кислорода, то к названию кислоты добавляют постфикс -водородная.
: H2S-2 – сероводородная кислота, HCl— – хлороводородная кислота.
При этом в названии соли используем постфикс -ид.
, Na2S-2 – сульфид натрия, KCl— – хлорид калия.

Номенклатура кислых солей.
Если в кислой соли на один кислотный остаток приходится один атом водорода, то к названию кислотного остатка добавляют префикс гидро-. Если на один кислотный остаток приходится два атома водорода, то добавляют префикс дигидро-.
, K2HPO4 – гидрофосфат калия, KH2PO4 – дигидрофосфат калия. Но: Ca(HCO3)2 – гидрокарбонат кальция.
Номенклатура основных солей.
Если в основной соли на один катион металла приходится одна гидроксо-группа, то к названию кислотного остатка добавляют префикс гидроксо-. Если на один катион металла приходится две гидроксо-группы, то добавляют префикс дигидроксо-.
, AlOHCl2 – гидроксохлорид алюминия, Al(OH)2Cl – дигидроксохлорид алюминия. Но: (CuOH)2CO3 – гидроксокарбонат меди (II).
В названии двойной соли катионы металлов перечисляют через дефис. В названии смешанных солей анионы кислотных остатков перечисляются через дефис.
, KAl(SO4)2 – сульфат алюминия-калия, CaClBr – бромид-хлорид кальция.

Также применяется тривиальная номенклатура. Тривиальные названия неорганических необходимо выучить наизусть.

Номенклатура комплексных солей*
Комплексное соединение может состоять из комплексного катиона, комплексного аниона или может быть нейтральным.
Комплексные соединения состоят из внутренней и внешней сферы. Центральная частица, вокруг которой расположены окружающие ее лиганды, называется комплексообразователем. Число лигандов комплексообразователя называется координационным числом. Как правило (но не обязательно!), число лигандов в 2 раза больше, чем степень окисления центральной частицы.
Соединения с комплексными катионами. Вначале называют анион внешней сферы, затем перечисляют лиганды, затем называют комплексообразователь в родительном падеже (ему дается русское название данного элемента). После названия комплексообразователя в скобках римской цифрой указывается его степень окисления.
К латинскому названию анионного лиганда добавляется окончание “о” (F— — фторо, Cl— -хлоро, ОН— — гидроксо, CN— — циано и т.д). Аммиак обозначают термином “аммин”, СО – карбонил, NO – нитрозил, H2O – аква.
Число одинаковых лигандов называют греческим числительным: 2 –ди, 3 – три, 4 – тетра, 5 – пента, 6 – гекса, 7 – гепта и т.д.
Вначале перечисляют лиганды анионные, затем нейтральные, затем катионные.
Если в комплексе имеются несколько лигандов одинакового знака заряда, то они называются в алфавитном порядке:
Соединения с комплексными анионами. Вначале называют комплексный анион в именительном падеже: перечисляют лиганды, затем комплексообразователь (ему дается латинское название и к названию добавляется окончание “ат”). После названия комплексообразователя указывается его степень окисления. Затем в родительном падеже называется внешнесферный катион.
Соединения без внешней сферы. Вначале называют лиганды, затем комплексообразователь в именительном падеже с указанием его степени окисления. Все название пишется слитно.
* материалы с портала onx.distant.ru
В органической химии одним из ключевых понятий является заместительная номенклатура. Заместители – это атомы или группы атомов, которые замещают один или несколько водородных атомов в органической молекуле. Заместители имеют свою номенклатуру, которая позволяет легко идентифицировать и классифицировать органические соединения.
Основной принцип заместительной номенклатуры заключается в указании положения заместителя относительно основной цепи углеродных атомов. Для этого используются числа, которые записываются перед названием заместителя. Например, если в молекуле есть заместитель в положении 2, то перед его названием ставится число 2. Таким образом, заместители нумеруются, начиная от наиболее простого углеродного атома, образующего основную цепь.
Примером заместительной номенклатуры может служить хлоробензол – органическое соединение, в котором атом водорода в молекуле бензола замещен атомом хлора. При нумерации цепи бензола ядро также получает число 1, поскольку оно является основной структурой. Значит, чтобы указать положение заместителя, мы должны поставить число 1 перед названием заместителя (хлора). Молекула хлоробензола следует назвать 1-хлоробензолом.
В заключении, заместительная номенклатура органических соединений является важной и неотъемлемой частью органической химии. Она позволяет точно идентифицировать и классифицировать органические соединения, а также легко указывать положение заместителей в молекуле. Понимание основных принципов заместительной номенклатуры позволяет более точно описывать и изучать свойства органических соединений.
Основные принципы заместительной номенклатуры органических соединений
Заместительная номенклатура органических соединений – это система правил и соглашений, используемая для наименования и классификации органических соединений на основе их структуры и химических свойств.
Основные принципы заместительной номенклатуры органических соединений включают:
Примеры заместительной номенклатуры включают:
Таким образом, заместительная номенклатура органических соединений позволяет точно и однозначно именовать различные типы соединений, основываясь на их структуре и функциональных группах.
Определение заместительной номенклатуры
Заместительная номенклатура – это система правил, которая используется для описания и классификации органических соединений на основе функциональных групп и их заместителей. Важным аспектом заместительной номенклатуры является учет всех атомов их упорядочение в молекуле. Это позволяет легче идентифицировать и категоризировать органические соединения.
Принципы заместительной номенклатуры:
Применение заместительной номенклатуры облегчает коммуникацию и понимание структур органических соединений. Она позволяет исследователям точно описывать состав и структуру молекул, а также классифицировать их по функциональным группам. Знание заместительной номенклатуры необходимо при изучении органической химии и использовании органических соединений в различных областях науки и промышленности.
Что такое заместительная номенклатура
Заместительная номенклатура – это система обозначения органических соединений, в которой каждый атом углерода в молекуле замещается другим атомом или функциональной группой. Номенклатура определяет способ именования заместителей и их расположение в молекуле.
Основной принцип заместительной номенклатуры заключается в том, что каждому заместителю в молекуле присваивается уникальное имя или номер, который указывает его положение в отношении других заместителей. Такие имена или номера называются локантами.
Примеры заместительной номенклатуры включают такие системы, как простая нумерация, группировка заместителей по алфавиту, случайная нумерация и многое другое. Каждый тип заместительной номенклатуры имеет свои правила и особенности, которые должны быть учтены при именовании органических соединений.
Знание заместительной номенклатуры является важной частью изучения органической химии, так как правильное именование соединений позволяет легче понять их структуру и свойства. Кроме того, заместительная номенклатура помогает представить сложные молекулы в виде удобных для анализа моделей и диаграмм.
История развития заместительной номенклатуры
Заместительная номенклатура в органической химии развивалась в течение многих веков, пройдя путь от простых описаний до сложных систем классификации и наименования соединений. Это было необходимо для облегчения коммуникации и систематизации знаний об органических соединениях.
Одной из первых попыток систематизации органических соединений было введение функциональных групп, что позволило классифицировать их по общим свойствам и реакциям. Это дало начало заместительной номенклатуре, где заместителями стали считать атомы или группы атомов, замещающие водородные атомы в молекуле.
В 19 веке французский химик Шарль Фридель предложил использовать приставки для обозначения заместителей. Например, приставка “клор-” указывала на замещение одного или нескольких атомов водорода атомами хлора. Это стало основой для развития системы приставок, которые до сих пор используются в заместительной номенклатуре.
В 20 веке номенклатура была дополнена и усовершенствована. В 1957 году было принято Международное правило номенклатуры, которое стало основой для современной заместительной номенклатуры. Оно устанавливает конкретные правила и соглашения для именования различных типов заместителей и их расположения в органических молекулах.
Система заместительной номенклатуры становится все более сложной, чтобы отразить разнообразие органических соединений. В настоящее время она позволяет точно определить структуру и состав молекулы на основе ее названия.
История развития заместительной номенклатуры показывает, каким образом важны систематизация и стандартизация в науке, особенно в такой сложной области, как органическая химия.
Значение заместительной номенклатуры в современной химии
Заместительная номенклатура органических соединений является одним из ключевых элементов в современной химии. Она позволяет систематизировать и описывать огромное количество органических соединений, учитывая их структуру и особенности.
Основным принципом заместительной номенклатуры является использование заместителей для обозначения различных функциональных групп и атомов, присутствующих в молекуле соединения. Это позволяет легко распознавать и классифицировать соединения, а также проводить синтез новых веществ с заданными свойствами.
Примеры использования заместительной номенклатуры включают такие ситуации, как обозначение группы метил (CH3) в молекуле метана (CH4), аминометиловой группы (-NHCH3) в аминометане (CH3NH2), или группы карбоксиловой кислоты (-COOH).
Кроме того, заместительная номенклатура позволяет учитывать различные изомеры, например, указывать положение заместителей на атомах углерода в циклических соединениях. Она также помогает определить химические свойства и реактивность соединений.
Заместительная номенклатура является важным инструментом в химической науке и применяется во многих ее областях, начиная от органического синтеза и разработки лекарств до проектирования полимерных материалов и катализа.
В итоге, заместительная номенклатура позволяет более эффективно и точно обозначать и описывать органические соединения, что является важным шагом в понимании и развитии химической науки.
Заместительная номенклатура – это система правил и соглашений, которые используются для описания органических соединений с помощью специальных заместителей. Заместительная номенклатура позволяет упростить и стандартизировать обозначение и название органических соединений.
Принципы заместительной номенклатуры включают:
Таким образом, принципы заместительной номенклатуры играют важную роль при составлении правильного названия и обозначения органических соединений, обеспечивая стандартизацию и удобство в обращении с ними.
Приоритет заместителей в номенклатурном префиксе
Заместительная номенклатура органических соединений – это система правил, которая позволяет назвать и классифицировать различные органические соединения в зависимости от их структурных особенностей. Одним из важных аспектов номенклатуры является присвоение заместителям соединения приоритета в номенклатурном префиксе.
В номенклатуре органических соединений использование заместителей в префиксе позволяет указать наличие функциональных групп, различных радикалов или атомов, замещающих водород в структуре соединения. При этом каждому заместителю присваивается свой приоритет, определяющий его положение в префиксе названия соединения.
Основные принципы определения приоритета заместителей в номенклатурном префиксе:
Ниже приведены примеры заместителей в номенклатурном префиксе с указанием их приоритета:
Это лишь некоторые примеры заместителей и их приоритетов в номенклатурном префиксе. При работе с конкретными соединениями необходимо учитывать дополнительные правила, которые могут быть применимы к определенным классам соединений.
Исключения и особенности в заместительной номенклатуре
В заместительной номенклатуре органических соединений существуют некоторые исключения и особенности, которые важно учитывать:
При назначении приоритета заместителями, первоочередное значение имеют:
Положение заместителя
Если заместителей в молекуле несколько, то их положение определяется следующими правилами:
Нумерация атомов
При нумерации атомов главной цепи измерение начинается с ближайшей к заместителю крайней точки главной цепи.
Исторические названия
В некоторых случаях, особенно при использовании исторической номенклатуры, могут применяться особые правила для называния заместителей. Например, для классификации аминоэфиров используются исторические названия аминов (триэтиламин, диэтиламин), а не их заместителей (этиловый эфир).
Также, когда рядом расположены две функциональные группы, для названия используются приставки “гидрокси-” и “окси-“, в отличие от заместительной номенклатуры, где используется приставка “гидрокси-” только для одной из групп.
Исключения для некоторых групп соединений
Для некоторых групп соединений допускаются исключения или особые правила. Например, в случае полициклических соединений, основное кольцо может рассматриваться как главное только в случаях, когда оно имеет максимальное число атомов.
Важно помнить, что заместительная номенклатура органических соединений является сложной и многогранной. Регулярное обновление и изучение номенклатурных правил поможет уверенно оперировать с ними в профессиональной деятельности.
Примеры заместительной номенклатуры
Заместительная номенклатура используется для обозначения замещенных атомов или групп в органических соединениях. Рассмотрим несколько примеров:
Эти примеры иллюстрируют основные принципы заместительной номенклатуры и позволяют нам легко определить и классифицировать замещенные атомы и группы в органических соединениях.
Тривиальные названия органических веществ (тривиальная номенклатура) — это названия органических веществ, которые присвоили тем или иным веществам, и которые не относятся ни к какой системе названия веществ (систематической номенклатуре и др.).
Тривиальные названия неорганических веществ (тривиальная номенклатура)
Admin
Систематическая номенклатура является научной и отражает состав, химическое и пространственное строение соединения.
В правилах ИЮПАК используется несколько типов номенклатур,наиболее универсальная и распространенная из них – заместительная. Для веществ несложного строения часто применяется радикально-функциональный способ.
В радикально-функциональной номенклатуре в основе названия лежит название функциональной группы, определяющей химический класс соединения, к которому присоединяют наименование органического радикала, например:
С2Н5ОН – этиловый спирт
С2Н5Cl – этилхлорид
СН3-О-С2Н5 – метилэтиловый эфир
В заместительной номенклатуре основой названия служит один углеводородный фрагмент, а другие рассматриваются как заместители водорода. Рассмотрим правила составления.
Правила составления названий по систематической международной номенклатуре ИЮПАК
В основе правил номенклатуры ИЮПАК лежат принципы заместительной номенклатуры.
1. Основу названия соединения составляет корень слова, обозначающий предельный углеводород с тем же числом атомов, что и главная цепь (мет- , эт- , проп- , бут- , пент- , гекс- и т.д.).
2. К корню добавляют суффикс, характеризующий степень насыщенности:
-ан (предельный, нет кратных связей);
-ен (при наличии двойной связи);
-ин (при наличии тройной связи).
Если кратных связей несколько, то в суффиксе указывается число таких связей ( -диен, триен и т.д.), а после суффикса обязательно указывается цифрами положение кратной связи, например:
СН3 –СН2 –СН=СН2 бутен-1
СН3 –СН=СН–СН3 бутен-2
СН2 =СН–СН=СН2 бутадиен-1,3
3. Далее в суффикс выносится название самой старшей характеристической группы в молекуле с указанием ее положения цифрой.
4. Прочие заместители обозначаются с помощью приставок в алфавитном порядке. Положение заместителей указывается цифрой перед приставкой, например: 3-метил, 2-хлор. Если в молекуле имеется несколько одинаковых заместителей, то перед названием этой группы словом указывается их количество (например, диметил- , трихлор- и т.д.).
5. Все цифры в названиях молекул отделяются от слов дефисом, а друг от друга запятыми.
6. Проводят нумерацию главной углеродной цепи так, чтобы старшая характеристическая группа имела наименьший порядковый номер.
Как назвать соединение?
Называем заместители в главной цепи
Нумеруем главную цепь
Строим название соединения
1. Выбрать самую длинную цепь (корень слова – пент). Далее следует суффикс –ен, указывающий на наличие кратной связи.
2. Порядок нумерации определяет старшая группа (-ОН) – наименьший номер.
3. Полное название соединения заканчивается суффиксом, обозначающим старшую группу (суффикс –ол указывает на налчие гидроксильной группы). Положение двойной связи и гидроксильной группы указывается цифрами.
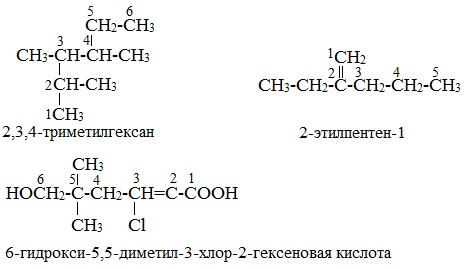
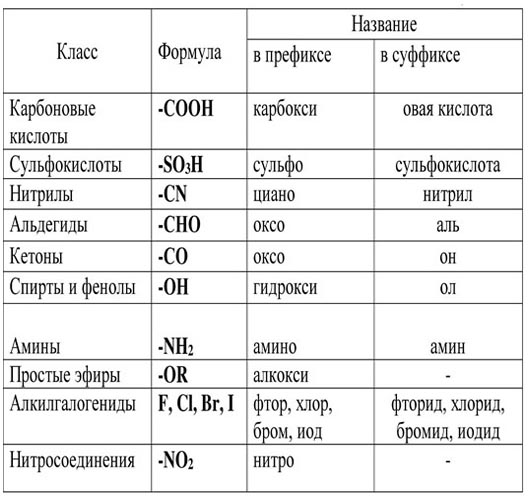
Названия характеристических групп (перечислены в порядке убывания старшинства)