Карбанионные соли
ацетилена называются ацетилени́дами
.
- Гомологический ряд алкинов
- Гомологический ряд алкинов
- 1.2. Галогенирование алкинов
- 1.3. Гидрогалогенирование алкинов
- 1.4. Гидратация алкинов
- Окисление алкинов
- 2.1. Горение алкинов
- 2.2. Окисление алкинов сильными окислителями
- Кислотные свойства алкинов
- Дегидрирование алканов
- Пиролиз метана
- Гидролиз карбида кальция
- Алкилирование соединений алкинов с металлами
- Реакции присоединения
- 1.2. Галогенирование алкинов
- 1.3. Гидрогалогенирование алкинов
- 1.4. Гидратация алкинов
- 1.5. Димеризация, тримеризация и полимеризация
- Окисление алкинов
- 2.1. Горение алкинов
- 2.2. Окисление алкинов сильными окислителями
- Кислотные свойства алкинов
- Гомологический ряд и изомерия
- Электронное строение двойной связи
- Нахождение в природе и физиологическая роль алкенов
- Реакции электрофильного присоединения
- Прочие реакции электрофильного присоединения
- Реакции радикального присоединения
- Реакции присоединения карбенов
- Гидрирование (реакция Сабатье — Сандеран)
- Реакции радикального замещения
- Окисление неорганическими окислителями
- Окисление в присутствии солей палладия
Открыт в 1836 году
Э. Дэви
, синтезирован из угля
и водорода
(дуговой разряд между двумя угольными электродами
в атмосфере водорода) М. Бертло
( 1862 год
).

Ацетилен обнаружен на Уране
и Нептуне
.

Ацетилен с водой, в присутствии солей ртути
и других катализаторов
, образует уксусный альдегид
( реакция Кучерова
). В силу наличия тройной связи, молекула
высокоэнергетична и обладает большой удельной теплотой сгорания — 14000 ккал/м 3
(50,4 МДж/кг). При сгорании в кислороде температура пламени достигает 3150 °C. Ацетилен может полимеризироваться
в бензол
и другие органические соединения ( полиацетилен
, винилацетилен
). Для полимеризации в бензол необходим графит
и температура в ~500 °C. В присутствии катализаторов, например, трикарбонил(трифенилфосфин)никеля, температуру реакции циклизации можно снизить до 60—70 °C.
Кроме того, атомы водорода
ацетилена относительно легко отщепляются в виде протонов
, то есть он проявляет кислотные свойства. Так, ацетилен вытесняет метан
из эфирного раствора магнийметилбромида (образуется содержащий ацетиленид-ион раствор), образует нерастворимые взрывчатые осадки с солями
серебра
и одновалентной
меди
.
Основные химические реакции ацетилена (реакции присоединения, сводная таблица 1.)
:
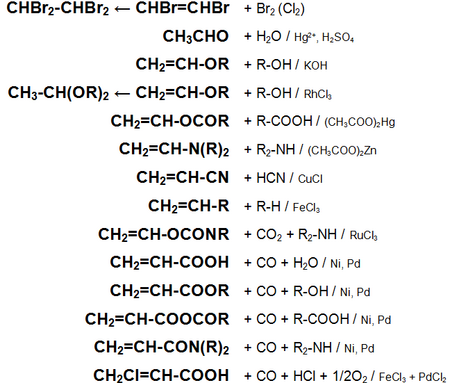
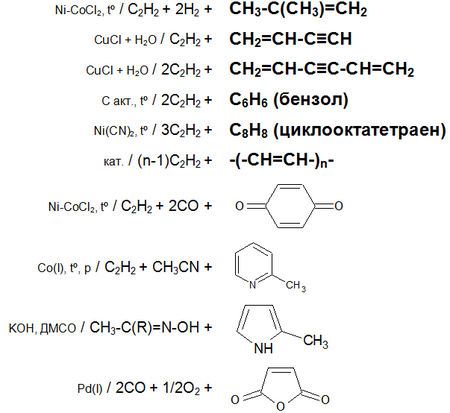
Основные химические реакции ацетилена (реакции присоединения, димеризации, полимеризации, цикломеризации, сводная таблица 2.)
:
Ацетилен обесцвечивает бромную воду
и раствор перманганата калия
.
Реагирует с аммиачными растворами солей Cu(I) и Ag(I) с образованием малорастворимых, взрывчатых ацетиленидов
— эта реакция используется для качественного определения ацетилена и его отличия от алкенов (которые тоже обесцвечивают бромную воду и раствор перманганата калия).
а также при дегидрировании
двух молекул метана
при температуре свыше 1400 °C:
Метан превращают в ацетилен и водород в электродуговых печах (температура 2000—3000 °С, напряжение между электродами 1000 В). Метан при этом разогревается до 1600 °С. Расход электроэнергии составляет около 13000 кВт•ч на 1 тонну ацетилена, что относительно много (примерно равно затрачиваемой энергии по карбидному методу) и потому является недостатком процесса. Выход ацетилена составляет 50 %.
Иное название — Вульф-процесс. Сначала разогревают насадку печи путём сжигания метана при 1350—1400 °С. Далее через разогретую насадку пропускают метан. Время пребывания метана в зоне реакции очень мало и составляет доли секунды. Процесс реализован в промышленности, но экономически оказался не таким перспективным, как считалось на стадии проектирования.
Метан смешивают с кислородом
. Часть сырья сжигают, а образующееся тепло расходуют на нагрев остатка сырья до 1600 °С. Выход ацетилена составляет 30—32 %. Метод имеет преимущества — непрерывный характер процесса и низкие энергозатраты. Кроме того, с ацетиленом образуется ещё и синтез-газ. Этот процесс (Заксе-процесс или BASF-процесс) получил наиболее широкое внедрение.
Является разновидностью окислительного пиролиза. Часть сырья сжигают с кислородом в топке печи, газ нагревается до 2000 °С. Затем в среднюю часть печи вводят остаток сырья, предварительно нагретый до 600 °С. Образуется ацетилен. Метод характеризуется большей безопасностью и надёжностью работы печи.
Пиролиз в струе низкотемпературной плазмы
Процесс разрабатывается с 1970-х годов, но, несмотря на перспективность, пока не внедрён в промышленности. Сущность процесса состоит в нагреве метана ионизированным газом. Преимущество метода заключается в относительно низких энергозатратах (5000—7000 кВт•ч) и высоких выходах ацетилена (87 % в аргоновой плазме и 73 % в водородной).
Этот способ известен с XIX века, но не потерял своего значения до настоящего времени. Сначала получают карбид кальция, сплавляя оксид кальция
(негашёную известь) и кокс
в электропечах при 2500—3000 °С:
Негашёную известь получают из карбоната кальция
:
Далее карбид кальция обрабатывают водой:
Получаемый ацетилен имеет высокую степень чистоты 99,9 %. Основным недостатком процесса является высокий расход электроэнергии: 10000—11000 кВт•ч на 1 тонну ацетилена.

- Для газовой сварки и резки
металлов
; - Как источник очень яркого, белого света в автономных светильниках, где он получается реакцией карбида кальция и воды (см. карбидная лампа
); - В производстве взрывчатых веществ (см. ацетилениды
); - Для получения уксусной кислоты
, этилового спирта
, растворителей
, пластических масс
, каучука
, ароматических углеводородов
; - Для получения технического углерода
; - В атомно-абсорбционной спектрофотометрии
при пламенной атомизации; - В ракетных двигателях (вместе с аммиаком
) [13]
; - В начале XX века широкое распространение имели автомобильные ацетиленовые фары, которые только в 1920-е были вытеснены электрическими.

:
справа — ацетиленовый газовый баллон
с ацетиленовым редуктором
,
слева кислородный
газовый баллон с кислородным редуктором
.
Поскольку ацетилен плохо растворим в воде, и его смеси с кислородом могут взрываться в очень широком диапазоне концентраций, его не следует собирать в газометры
.
Ацетилен взрывается при температуре около 500 °C или давлении выше 0,2 МПа; КПВ
2,3—80,7 %, температура самовоспламенения 335 °C. Взрывоопасность уменьшается при разбавлении ацетилена другими газами, например азотом
, метаном
или пропаном
.
При длительном соприкосновении ацетилена с медью и серебром образуются ацетилениды меди и серебра, которые взрываются при ударе или повышении температуры. Поэтому при хранении ацетилена не используются материалы, содержащие медь (например, вентили баллонов).
Ацетилен обладает незначительным токсическим действием. Для ацетилена нормирован ПДКм.р. = ПДК с.с. = 1,5 мг/м³ согласно гигиеническим нормативам ГН 2.1.6.1338-03 «Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населённых мест».
ПДКр.з. (рабочей зоны) не установлен (по ГОСТ 5457-75 и ГН 2.2.5.1314-03), так как концентрационные пределы распределения пламени в смеси с воздухом составляет 2,5—100 %.
Хранят и перевозят ацетилен в заполненных инертной пористой массой (например, древесным углём
) стальных баллонах белого цвета с красной надписью «АЦЕТИЛЕН» в виде раствора в ацетоне
. Баллон ёмкостью 40 л под давлением 15—16 кгс/см 2
вмещает около 5000 л газообразного ацетилена (взятого при нормальном атмосферном давлении).
- ГОСТ 5457-75. Ацетилен растворённый и газообразный технический. Технические условия
. Дата обращения: 8 февраля 2012.
Архивировано
19 июля 2017 года.
- ↑ 1
2
3
4
- David R. Lide, Jr.
Basic laboratory and industrial chemicals
: A CRC quick reference handbook — CRC Press
, 1993. — ISBN 978-0-8493-4498-5
- Словарь иностранных слов. — М.: « Русский язык
», 1989. — 624 с. ISBN 5-200-00408-8
- Acetylene — New World Encyclopedia
. www.newworldencyclopedia.org
. Дата обращения: 9 июля 2023.
- Корольченко. Пожаровзрывоопасность веществ, 2004
, с. 198. - Миллер. Ацетилен, его свойства, получение и применение, 1969
, с. 72. - Большая энциклопедия нефти и газа. Неприятный запах — ацетилен
. Дата обращения: 10 октября 2013.
Архивировано
29 октября 2013 года.
- . Дата обращения: 10 октября 2013.
Архивировано из оригинала
1 октября 2013 года.
- Видео данного процесса
. Дата обращения: 29 сентября 2017.
Архивировано
16 ноября 2015 года.
- Лапидус А. Л., Голубева И. А., Жагфаров Ф. Г.
Газохимия. Учебное пособие. — М.
: ЦентрЛитНефтеГаз, 2008. — 450 с. — ISBN 978-5-902665-31-1
.
- В России разработали ракетный двигатель на аммиаке — Известия
. Дата обращения: 7 мая 2012.
Архивировано
7 мая 2012 года.
- Миллер С. А.
Ацетилен, его свойства, получение и применение. — Л.
: Химия, 1969. — Т. 1. — 680 с. - Корольченко А. Я., Корольченко Д. А.
Пожаровзрывоопасность веществ и материалов и средства их тушения. Справочник: в 2-х частях. Часть 1. — М.
: Ассоциация «Пожнаука», 2004. — 713 с. — ISBN 5-901283-02-3
. - Хвостов И. В.
// Химическая энциклопедия
: в 5 т. / Гл. ред. И. Л. Кнунянц
. — М.
: Советская энциклопедия
, 1988. — Т. 1: А — Дарзана. — С. 226—228. — 623 с. — — ISBN 5-85270-008-8
.
1
. В ответе перечисляем через знак « +
» только продукты реакции с коэффициентами. Левую часть реакции писать не нужно. Например:
10 уксусная кислота + 4 K2SO4 + 8 MnSO4 + 12 вода
2
. Ответ должен учитывать только те реагенты, которые указаны в задаче, нельзя «брать» дополнительные реагенты. Например, если уравнение в задаче «CH 3
CHO + KMnO 4
», требуется дописать уравнение окисления именно в нейтральной среде, а не в кислой. Если без дополнительного реагента реакция не идет, пишем в ответ « не идет
».
Исключение:
если в задаче один из реагентов дан в растворе (индекс «p-р»), в уравнении реакции может дополнительно участвовать вода.
3
. Ответ должен учитывать условия реакции и формы реагента, если они есть. Если при данных условиях реакция не идет, в ответ пишем « не идет
».
4
. Если у реагентов нет коэффициентов, вы должны сами выбрать, в каком молярном соотношении могут вступить друг с другом эти реагенты в данных условиях, и в соответствии с этим уравнять реакцию. Например, в задаче «C 6
H 5
OH + Cl 2
» допустимо как моно-хлорпроизводное, так и конечный продукт. Если один из реагентов имеет коэффициент, его необходимо учесть, задача «C 6
H 5
OH + 1
Cl 2
» означает, что требуется именно моно-хлорпроизводное. Если в уравнении коэффициент одного из реагентов указан, а у другого реагента нет — значит у него подразумевается коэффициент 1.
5
. Вещества можно записывать систематическими или тривиальными названиями, а также формулой. Но название должно быть однозначным, например, ответ «хлорид железа» не будет засчитан, т.к. неясно, это FeCl 2
или FeCl 3
. Метилгексан тоже не будет засчитан, т.к. неоднозначен локант, а вот метилбутан — ок.
6
. Если реакция дает нестехиометрическую смесь продуктов, в ответе следует писать преобладающий продукт. Если при данных условиях преобладающий продукт неоднозначен (или это выходит за рамки школы) система примет любой допустимый вариант ответа.
7
. Коэффициенты и знаки « +
» можно отделять пробелами или не отделять, как вам удобнее. Но если название содержит радикал, стоит отделять коэффициент пробелом, чтобы система не спутала коэффициент с локантом и забытым дефисом.
8
. Коэффициенты в уравнении должны быть сокращены, но сокращать нужно лишь на общий множитель во всем уравнении. Нельзя сокращать общий множитель коэффициентов в правой части уравнения, если левая при этом окажется дробной. Коэффициент 1 писать не надо.
9
. Порядок перечисления продуктов на ваше усмотрение.
10
. Во время решения задачи можно пользоваться только химическими таблицами, справочником и графическим редактором. Если во время решения задачи вы сделаете запрос на любое вещество или реакцию, а потом отправите ответ, ваш рейтинг участника не будет повышен.
– это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна тройная связь между атомами углерода С≡С.
Остановимся на свойствах, способах получения и особенностях строения алкинов.
Строение, изомерия и гомологический ряд алкинов
Химические свойства алкинов
Гомологический ряд алкинов
Все алкины имеют общие или похожие физические и химические свойства. Схожие по строению алкины, которые отличаются на одну или несколько групп –СН 2
–, называют гомологами
. Такие алкины образуют гомологический ряд.
Первый представитель гомологического ряда алкенов – этин (ацетилен) C 2
H 2
, или СH≡СH.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН 2
– в углеводородную цепь.
Общая формула гомологического ряда алкинов C n
H 2n-2
.
Первые три члена гомологического ряда алкинов – газы, начиная с C 5
Н 8
по С 16
Н 30
– жидкости, начиная с С 17
Н 32
— твердые вещества.
Алкины плохо растворимы в воде и хорошо растворимы в органических растворителях.
Рассмотрим особенности строения алкинов на примере ацетилена.
В молекуле ацетилена присутствуют химические связи C–H и С≡С.
Связь C–H ковалентная слабополярная одинарная σ-связь. Связь С≡С – тройная, ковалентная неполярная, одна из связей σ, еще две: π-связи. Атомы углерода при тройной связи образуют по две σ-связи и две π-связи. Следовательно, гибридизация атомов углерода при тройной связи в молекулах алкинов – sp:

При образовании σ-связи между атомами углерода происходит перекрывание sp-гибридных орбиталей атомов углерода:

При образовании π-связи между атомами углерода происходит перекрывание негибридных орбиталей атомов углерода:

Две sp-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому две гибридные орбитали атомов углерода при тройной связи в алкинах направлены в пространстве под углом 180 о
друг к другу:

Изображение с сайта orgchem.ru
Это соответствует линейному строению молекулы.
молекуле ацетилена C 2
H 2
соответствует линейное строение.

Изображение с сайта orgchem.ru
Молекулам алкинов с большим числом атомов углерода соответствует пространственное строение
.
в молекуле пропина присутствует атом углерода в sp 3
-гибридном состоянии, в составе метильного фрагмента СН 3
. Такой фрагмент имеет тетраэдрическое строение.
Для алкинов характерна структурная и пространственная изомерия
.
Для алкинов характерна изомерия углеродного скелета, изомерия положения кратной связи и межклассовая изомерия
.
Структурные изомеры
— это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета
отличаются строением углеродного скелета.
Изомеры с различным углеродным скелетом и с формулой С 5
Н 8
— пентин-1 и 3-метилбутин-1
Межклассовые изомеры —
это вещества разных классов с различным строением, но одинаковым составом. Алкины являются межклассовыми изомерами с алкадиенами. Общая формула алкинов и алкадиенов — C n
H 2n-2
.
Межклассовые изомеры с общей формулой С 4
Н 6
— бутин-1 и бутадиен
Изомеры с различным положением тройной связи
отличаются положением тройной связи в углеродном скелете.
Изомеры положения тройной связи, которые соответствуют формуле С 5
Н 8
— пентин-1 и пентин-2
Для некоторых алкинов также характерна оптическая изомерия
.
Алкины, которые обладают достаточно большим углеродным скелетом, могут существовать в виде оптических изомеров
. В молекуле алкина должен присутствовать асимметрический
атом углерода
(атом углерода, связанный с четырьмя различными заместителями).
Цис-транс
-изомерия
для алкинов не характерна, так как по тройной связи вращение возможно.
В названиях алкинов для обозначения тройной связи используется суффикс -ИН.
Например,
алкин на рисунке называется бутин-2

Для простейших алкинов применяются также исторически сложившиеся (тривиальные) названия:
Радикалы, содержащие тройную связь, также носят тривиальные названия:
1
. В ответе перечисляем через знак « +
» только продукты реакции с коэффициентами. Левую часть реакции писать не нужно. Например:
10 уксусная кислота + 4 K2SO4 + 8 MnSO4 + 12 вода
2
. Ответ должен учитывать только те реагенты, которые указаны в задаче, нельзя «брать» дополнительные реагенты. Например, если уравнение в задаче «CH 3
CHO + KMnO 4
», требуется дописать уравнение окисления именно в нейтральной среде, а не в кислой. Если без дополнительного реагента реакция не идет, пишем в ответ « не идет
».
Исключение:
если в задаче один из реагентов дан в растворе (индекс «p-р»), в уравнении реакции может дополнительно участвовать вода.
3
. Ответ должен учитывать условия реакции и формы реагента, если они есть. Если при данных условиях реакция не идет, в ответ пишем « не идет
».
4
. Если у реагентов нет коэффициентов, вы должны сами выбрать, в каком молярном соотношении могут вступить друг с другом эти реагенты в данных условиях, и в соответствии с этим уравнять реакцию. Например, в задаче «C 6
H 5
OH + Cl 2
» допустимо как моно-хлорпроизводное, так и конечный продукт. Если один из реагентов имеет коэффициент, его необходимо учесть, задача «C 6
H 5
OH + 1
Cl 2
» означает, что требуется именно моно-хлорпроизводное. Если в уравнении коэффициент одного из реагентов указан, а у другого реагента нет — значит у него подразумевается коэффициент 1.
5
. Вещества можно записывать систематическими или тривиальными названиями, а также формулой. Но название должно быть однозначным, например, ответ «хлорид железа» не будет засчитан, т.к. неясно, это FeCl 2
или FeCl 3
. Метилгексан тоже не будет засчитан, т.к. неоднозначен локант, а вот метилбутан — ок.
6
. Если реакция дает нестехиометрическую смесь продуктов, в ответе следует писать преобладающий продукт. Если при данных условиях преобладающий продукт неоднозначен (или это выходит за рамки школы) система примет любой допустимый вариант ответа.
7
. Коэффициенты и знаки « +
» можно отделять пробелами или не отделять, как вам удобнее. Но если название содержит радикал, стоит отделять коэффициент пробелом, чтобы система не спутала коэффициент с локантом и забытым дефисом.
8
. Коэффициенты в уравнении должны быть сокращены, но сокращать нужно лишь на общий множитель во всем уравнении. Нельзя сокращать общий множитель коэффициентов в правой части уравнения, если левая при этом окажется дробной. Коэффициент 1 писать не надо.
9
. Порядок перечисления продуктов на ваше усмотрение.
10
. Во время решения задачи можно пользоваться только химическими таблицами, справочником и графическим редактором. Если во время решения задачи вы сделаете запрос на любое вещество или реакцию, а потом отправите ответ, ваш рейтинг участника не будет повышен.
– это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна тройная связь между атомами углерода С≡С.
Остановимся на свойствах, способах получения и особенностях строения алкинов.
Строение, изомерия и гомологический ряд алкинов
Химические свойства алкинов
Гомологический ряд алкинов
Все алкины имеют общие или похожие физические и химические свойства. Схожие по строению алкины, которые отличаются на одну или несколько групп –СН 2
–, называют гомологами
. Такие алкины образуют гомологический ряд.
Первый представитель гомологического ряда алкенов – этин (ацетилен) C 2
H 2
, или СH≡СH.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН 2
– в углеводородную цепь.
Общая формула гомологического ряда алкинов C n
H 2n-2
.
Первые три члена гомологического ряда алкинов – газы, начиная с C 5
Н 8
по С 16
Н 30
– жидкости, начиная с С 17
Н 32
— твердые вещества.
Алкины плохо растворимы в воде и хорошо растворимы в органических растворителях.
Рассмотрим особенности строения алкинов на примере ацетилена.
В молекуле ацетилена присутствуют химические связи C–H и С≡С.
Связь C–H ковалентная слабополярная одинарная σ-связь. Связь С≡С – тройная, ковалентная неполярная, одна из связей σ, еще две: π-связи. Атомы углерода при тройной связи образуют по две σ-связи и две π-связи. Следовательно, гибридизация атомов углерода при тройной связи в молекулах алкинов – sp:
При образовании σ-связи между атомами углерода происходит перекрывание sp-гибридных орбиталей атомов углерода:
При образовании π-связи между атомами углерода происходит перекрывание негибридных орбиталей атомов углерода:
Две sp-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому две гибридные орбитали атомов углерода при тройной связи в алкинах направлены в пространстве под углом 180 о
друг к другу:

Изображение с сайта orgchem.ru
Это соответствует линейному строению молекулы.
молекуле ацетилена C 2
H 2
соответствует линейное строение.

Изображение с сайта orgchem.ru
Молекулам алкинов с большим числом атомов углерода соответствует пространственное строение
.
в молекуле пропина присутствует атом углерода в sp 3
-гибридном состоянии, в составе метильного фрагмента СН 3
. Такой фрагмент имеет тетраэдрическое строение.
Для алкинов характерна структурная и пространственная изомерия
.
Для алкинов характерна изомерия углеродного скелета, изомерия положения кратной связи и межклассовая изомерия
.
Структурные изомеры
— это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета
отличаются строением углеродного скелета.
Изомеры с различным углеродным скелетом и с формулой С 4
Н 6
— бутин-1 и бутадиен-1,3
Межклассовые изомеры —
это вещества разных классов с различным строением, но одинаковым составом. Алкины являются межклассовыми изомерами с алкадиенами. Общая формула алкинов и алкадиенов — C n
H 2n-2
.
Межклассовые изомеры с общей формулой С 4
Н 6
— бутин-1 и бутадиен
Изомеры с различным положением тройной связи
отличаются положением тройной связи в углеродном скелете.
Изомеры положения тройной связи, которые соответствуют формуле С 5
Н 8
— пентин-1 и пентин-2
Для алкенов также характерна оптическая изомерия
.
Алкины, которые обладают достаточно большим углеродным скелетом, могут существовать в виде оптических изомеров
. В молекуле алкина должен присутствовать асимметрический
атом углерода
(атом углерода, связанный с четырьмя различными заместителями).
Цис-транс
-изомерия
для алкинов не характерна, так как по тройной связи вращение возможно.
В названиях алкинов для обозначения тройной связи используется суффикс -ИН.
Например,
алкин на рисунке называется бутин-2
Для простейших алкинов применяются также исторически сложившиеся (тривиальные) названия:
Радикалы, содержащие тройную связь, также носят тривиальные названия:
Химические свойства алкинов
– непредельные углеводороды, в молекулах которых есть одна тройная связь. Строение и свойства тройной связи определяют характерные химические свойства алкинов. Химические свойства алкинов схожи с химическими свойствами алкенов из-за наличия кратной связи в молекуле.
Для алкинов характерны реакции окисления. Окисление алкинов протекает преимущественно по тройной связи, хотя возможно и жесткое окисление (горение).
Реакции присоединения
Тройная связь состоит из σ-связи и двух π-связей. Сравним характеристики одинарной связи С–С, тройной связи СС и связи С–Н:
Таким образом, тройная связь короче, чем одинарная связь , поэтому π-электроны тройной связи прочнее удерживаются ядрами атомов углерода и обладают меньшей поляризуемостью и подвижностью. Реакции присоединения
по тройной связи к алкинам протекают сложнее, чем реакции присоединения по двойной связи к алкенам.
Для алкинов характерны реакции присоединения по тройной связи СС с разрывом π-связей.
Гидрирование алкинов протекает в присутствии катализаторов (Ni, Pt) с образованием алкенов, а затем сразу алканов.
Например,
при гидрировании бутина-2 в присутствии никеля образуется сначала бутен-2, а затем бутан.

При использовании менее активного катализатора (Pd, СaCO 3
, Pb(CH 3
COO) 2
) гидрирование останавливается на этапе образования алкенов.
Например,
при гидрировании бутина-1 в присутствии палладия преимущественно образуется бутен-1.

1.2. Галогенирование алкинов
Присоединение галогенов к алкинам происходит даже при комнатной температуре в растворе (растворители — вода, CCl 4
).
При взаимодействии с алкинами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на тройную связь.
Например,
при бромировании пропина сначала образуется 1,2-дибромпропен, а затем — 1,1,2,2-тетрабромпропан.


Аналогично алкины реагируют с хлором, но обесцвечивания хлорной воды при этом не происходит, потому что хлорная вода и так бесцветная)
Реакции протекают в присутствии полярных растворителей по ионному (электрофильному) механизму.
1.3. Гидрогалогенирование алкинов
Алкины присоединяют галогеноводороды. Реакция протекает по механизму электрофильного присоединения с образованием галогенопроизводного алкена или дигалогеналкана.
Например,
при взаимодействии ацетилена с хлороводородом образуется хлорэтен, а затем 1,1-дихлорэтан.


При присоединении галогеноводородов и других полярных молекул к симметричным алкинам образуется, как правило, один продукт реакции, где оба галогена находятся у одного атома С.
При присоединении полярных молекул к несимметричным алкинам образуется смесь изомеров. При этом выполняется правило Марковникова.
Правило Марковникова:
при присоединении полярных молекул типа НХ к несимметричным алкинам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода
при двойной связи.
Например,
при присоединении хлороводорода HCl к пропину преимущественно образуется 2-хлорпропен.


1.4. Гидратация алкинов
Гидратация (присоединение воды) алкинов протекает в присутствии кислоты и катализатора (соли ртути II).
Сначала образуется неустойчивый алкеновый спирт, который затем изомеризуется в альдегид или кетон.
Например,
при взаимодействии ацетилена с водой в присутствии сульфата ртути образуется уксусный альдегид.
Гидратация алкинов протекает по ионному (электрофильному) механизму.
Для несимметричных алкенов присоединение воды преимущественно по правилу Марковникова.
Например,
при гидратации пропина образуется пропанон (ацентон).
1.5. Димеризация, тримеризация и полимеризация
Присоединение одной молекулы ацетилена к другой (
димеризация
) протекает под действием аммиачного раствора хлорида меди (I). При этом образуется винилацетилен:

Тримеризация
ацетилена (присоединение трех молекул друг к другу) протекает под действием температуры, давления и в присутствии активированного угля с образованием бензола (реакция Зелинского):

Алкины также вступают в реакции полимеризации
— процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
Например,
при полимеризации ацетилена образуется полимер линейного или циклического строения.
Окисление алкинов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
2.1. Горение алкинов
Алкины, как и прочие углеводороды, горят с образованием углекислого газа и воды.
Уравнение сгорания алкинов в общем виде:
Например
, уравнение сгорания пропина:
2.2. Окисление алкинов сильными окислителями
Алкины реагируют с сильными окислителями (перманганаты или соединения хрома (VI)). При этом происходит окисление тройной связи С≡С и связей С-Н у атомов углерода при тройной связи
. При этом образуются связи с кислородом.
При окислении трех связей у атома углерода в кислой среде образуется карбоксильная группа СООН, четырех — углекислый газ СО 2
. В нейтральной среде — соль карбоновой кислоты и карбонат (гидрокарбонат) соответственно.
Таблица соответствия окисляемого фрагмента молекулы и продукта:
При окислении бутина-2 перманганатом калия в среде серной кислоты окислению подвергаются два фрагмента СН 3
–C, поэтому образуется уксусная кислота:

При окислении 3-метилпентина-1 перманганатом калия в серной кислоте окислению подвергаются фрагменты R–C и H–C , поэтому образуются карбоновая кислота и углекислый газ:

При окислении алкинов сильными окислителями в нейтральной среде углеродсодержащие продукты реакции жесткого окисления (кислота, углекислый газ) могут реагировать с образующейся в растворе щелочью в соотношении, которое определяется электронным балансом с образованием соответствующих солей.
Например
, при окислении бутина-2 перманганатом калия в воде при нагревании окислению подвергаются два фрагмента R–C, поэтому образуется соль уксусной кислоты – ацетат калия

Аналогичные органические продукты образуются при взаимодействии алкинов с хроматами или дихроматами.
Окисление ацетилена
протекает немного иначе, σ-связь С–С не разрывается, поэтому в кислой среде образуется щавелевая кислота:

В нейтральной среде образуется соль щавелевой кислоты – оксалат калия:

Обесцвечивание раствора перманганата калия — качественная реакция на тройную связь.
Кислотные свойства алкинов
Связь атома углерода при тройной связи (атома углерода в sp-гибридизованном состоянии) с водородом значительно более полярная. чем связь С–Н атома углерода при двойной или одинарной связи (в sp 2
и sp 3
-гибридном состоянии соответственно). Это обусловлено большим вкладом s-орбитали в гибридизованное состояние.
Повышенная полярность связи С–Н у атомов углерода при тройной связи в алкинах приводит к возможности отщепления протона Н +
, т.е. приводит к появлению у алкинов с тройной связью на конце молекулы (алкинов-1) кислотных свойств
.
Ацетилен и его гомологи с тройной связью на конце молекулы R–CC–H проявляют слабые кислотные свойства
, атомы водорода на конце молекулы могут легко замещаться на атомы металлов.
Алкины с тройной связью на конце молекулы взаимодействуют с активными металлами, гидридами, амидами металлов и т.д.
Например
, ацетилен взаимодействует с натрием с образованием ацетиленида натрия.

Например
, пропин взаимодействует с амидом натрия с образованием пропинида натрия.

Алкины с тройной связью на конце молекулы взаимодействуют с аммиачным раствором оксида серебра (I) или аммиачным раствором хлорида меди (I).
При этом образуются нерастворимые в воде ацетилениды серебра или меди (I):

Алкины с тройной связью на конце молекулы взаимодействуют с аммиачным раствором оксида серебра
или аммиачным раствором хлорида меди (I)
с образованием белого или красно-коричневого осадка
соответственно. Это качественная реакция
на алкины с тройной связью на конце молекулы.
Соответственно, алкины, в которых тройная связь расположена не на конце молекулы, не реагируют с аммиачными растворами оксида серебра или хлорида меди (I).

Дегидрирование алканов
При дегидрировании алканов, содержащих от двух до трех атомов углерода в молекуле, образуются двойные и тройные связи.
Например
, при дегидрировании этана может образоваться этилен или ацетилен:

Пиролиз метана
Пиролиз метана –
это промышленный способ получения ацетилена.

Реакцию проводят, очень быстро пропуская метан между электродами (электродуговой способ) — примерно 0,1-0,01 секунды при температуре 1500 о
С.
Если процесс проводить дольше, то метан разлагается на углерод и водород:

Гидролиз карбида кальция
Лабораторный способ получения ацетилена – водный или кислотный гидролиз карбида кальция CaC 2
.
СаС 2
+ 2Н 2
О = Са(ОН) 2
+ С 2
Н 2
В кислой среде образуется ацетилен и соответствующая соль:
CaC 2
+ 2HCl = CaCl 2
+ C 2
H 2
Карбид кальция можно получить, нагревая оксид кальция с углеродом:
Дигалогеналканы, в молекулах которых два атома галогена расположены у одного, либо у соседних атомов углерода, реагируют с избытком спиртового раствора щелочей с образованием алкинов.
Например,
1,2-дихлорпропан реагирует со спиртовым раствором гидроксида натрия

1,1-дихлорпропан реагирует со спиртовым раствором щелочи с образованием пропина.
Алкилирование соединений алкинов с металлами
Ацетилениды, пропиниды и прочие соединения алкинов с металлами реагируют с галогеналканами с образованием гомологов алкинов. При этом происходит удлиннение исходной молекулы алкина.
Например,
пропинид натрия реагирует с бромэтаном с образованием пентина-2

– это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна тройная связь между атомами углерода С≡С.
Остановимся на свойствах, способах получения и особенностях строения алкинов.
Строение, изомерия и гомологический ряд алкинов
Химические свойства алкинов
Химические свойства алкинов
– непредельные углеводороды, в молекулах которых есть одна тройная связь. Строение и свойства тройной связи определяют характерные химические свойства алкинов. Химические свойства алкинов схожи с химическими свойствами алкенов из-за наличия кратной связи в молекуле.
Для алкинов характерны реакции окисления. Окисление алкенов протекает преимущественно по тройной связи, хотя возможно и жесткое окисление (горение).
Реакции присоединения
Тройная связь состоит из σ-связи и двух π-связей. Сравним характеристики одинарной связи С–С, тройной связи СС и связи С–Н:
Таким образом, тройная связь короче, чем одинарная связь , поэтому π-электроны тройной связи прочнее удерживаются ядрами атомов углерода и обладают меньшей поляризуемостью и подвижностью. Реакции присоединения
по тройной связи к алкинам протекают сложнее, чем реакции присоединения по двойной связи к алкенам.
Для алкинов характерны реакции присоединения по тройной связи СС с разрывом π-связей.
Гидрирование алкинов протекает в присутствии катализаторов (Ni, Pt) с образованием алкенов, а затем сразу алканов.
Например,
при гидрировании бутина-2 в присутствии никеля образуется сначала бутен-2, а затем бутан.

При использовании менее активного катализатора (Pd, СaCO 3
, Pb(CH 3
COO) 2
) гидрирование останавливается на этапе образования алкенов.
Например,
при гидрировании бутина-1 в присутствии палладия преимущественно образуется бутен-1.

1.2. Галогенирование алкинов
Присоединение галогенов к алкинам происходит даже при комнатной температуре в растворе (растворители — вода, CCl 4
).
При взаимодействии с алкинами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на тройную связь.
Например,
при бромировании пропина сначала образуется 1,2-дибромпропен, а затем — 1,1,2,2-тетрабромпропан.


Аналогично алкины реагируют с хлором, но обесцвечивания хлорной воды при этом не происходит, потому что хлорная вода и так бесцветная)
Реакции протекают в присутствии полярных растворителей по ионному (электрофильному) механизму.
1.3. Гидрогалогенирование алкинов
Алкины присоединяют галогеноводороды. Реакция протекает по механизму электрофильного присоединения с образованием галогенопроизводного алкена или дигалогеналкана.
Например,
при взаимодействии ацетилена с хлороводородом образуется хлорэтен, а затем 1,1-дихлорэтан.


При присоединении галогеноводородов и других полярных молекул к симметричным алкинам образуется, как правило, один продукт реакции, где оба галогена находятся у одного атома С.
При присоединении полярных молекул к несимметричным алкинам образуется смесь изомеров. При этом выполняется правило Марковникова.
Правило Марковникова:
при присоединении полярных молекул типа НХ к несимметричным алкинам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода
при двойной связи.
Например,
при присоединении хлороводорода HCl к пропину преимущественно образуется 2-хлорпропен.


1.4. Гидратация алкинов
Гидратация (присоединение воды) алкинов протекает в присутствии кислоты и катализатора (соли ртути II).
Сначала образуется неустойчивый алкеновый спирт, который затем изомеризуется в альдегид или кетон.
Например,
при взаимодействии ацетилена с водой в присутствии сульфата ртути образуется уксусный альдегид.

Гидратация алкинов протекает по ионному (электрофильному) механизму.
Для несимметричных алкенов присоединение воды преимущественно по правилу Марковникова.
Например,
при гидратации пропина образуется пропанон (ацентон).

1.5. Димеризация, тримеризация и полимеризация
Присоединение одной молекулы ацетилена к другой ( димеризация
) протекает под действием аммиачного раствора хлорида меди (I). При этом образуется винилацетилен:

Тримеризация
ацетилена (присоединение трех молекул друг к другу) протекает под действием температуры, давления и в присутствии активированного угля с образованием бензола (реакция Зелинского):

Алкины также вступают в реакции полимеризации
— процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
Например,
при полимеризации ацетилена образуется полимер линейного или циклического строения.
Окисление алкинов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
2.1. Горение алкинов
Алкины, как и прочие углеводороды, горят с образованием углекислого газа и воды.
Уравнение сгорания алкинов в общем виде:
Например
, уравнение сгорания пропина:
2.2. Окисление алкинов сильными окислителями
Алкины реагируют с сильными окислителями (перманганаты или соединения хрома (VI)). При этом происходит окисление тройной связи С≡С и связей С-Н у атомов углерода при тройной связи
. При этом образуются связи с кислородом.
При окислении трех связей у атома углерода в кислой среде образуется карбоксильная группа СООН, четырех — углекислый газ СО 2
. В нейтральной среде — соль карбоновой кислоты и карбонат (гидрокарбонат) соответственно.
Таблица соответствия окисляемого фрагмента молекулы и продукта:
При окислении бутина-2 перманганатом калия в среде серной кислоты окислению подвергаются два фрагмента СН 3
–C, поэтому образуется уксусная кислота:

При окислении 3-метилпентина-1 перманганатом калия в серной кислоте окислению подвергаются фрагменты R–C и H–C , поэтому образуются карбоновая кислота и углекислый газ:

При окислении алкинов сильными окислителями в нейтральной среде углеродсодержащие продукты реакции жесткого окисления (кислота, углекислый газ) могут реагировать с образующейся в растворе щелочью в соотношении, которое определяется электронным балансом с образованием соответствующих солей.
Например
, при окислении бутина-2 перманганатом калия в воде при нагревании окислению подвергаются два фрагмента R–C, поэтому образуется соль уксусной кислоты – ацетат калия

Аналогичные органические продукты образуются при взаимодействии алкинов с хроматами или дихроматами.
Окисление ацетилена
протекает немного иначе, σ-связь С–С не разрывается, поэтому в кислой среде образуется щавелевая кислота:

В нейтральной среде образуется соль щавелевой кислоты – оксалат калия:

Обесцвечивание раствора перманганата калия — качественная реакция на тройную связь.
Кислотные свойства алкинов
Связь атома углерода при тройной связи (атома углерода в sp-гибридизованном состоянии) с водородом значительно более полярная. чем связь С–Н атома углерода при двойной или одинарной связи (в sp 2
и sp 3
-гибридном состоянии соответственно). Это обусловлено большим вкладом s-орбитали в гибридизованное состояние.
Повышенная полярность связи С–Н у атомов углерода при тройной связи в алкинах приводит к возможности отщепления протона Н +
, т.е. приводит к появлению у алкинов с тройной связью на конце молекулы (алкинов-1) кислотных свойств
.
Ацетилен и его гомологи с тройной связью на конце молекулы R–CC–H проявляют слабые кислотные свойства
, атомы водорода на конце молекулы могут легко замещаться на атомы металлов.
Алкины с тройной связью на конце молекулы взаимодействуют с активными металлами, гидридами, амидами металлов и т.д.
Например
, ацетилен взаимодействует с натрием с образованием ацетиленида натрия.

Например
, пропин взаимодействует с амидом натрия с образованием пропинида натрия.

Алкины с тройной связью на конце молекулы взаимодействуют с аммиачным раствором оксида серебра (I) или аммиачным раствором хлорида меди (I).
При этом образуются нерастворимые в воде ацетилениды серебра или меди (I):

Алкины с тройной связью на конце молекулы взаимодействуют с аммиачным раствором оксида серебра
или аммиачным раствором хлорида меди (I)
с образованием белого или красно-коричневого осадка
соответственно. Это качественная реакция
на алкины с тройной связью на конце молекулы.
Соответственно, алкины, в которых тройная связь расположена не на конце молекулы, не реагируют с аммиачными растворами оксида серебра или хлорида меди (I).
Запрос «Алкен» перенаправляется сюда; см. также другие значения
.

Алке́ны
( этиле́новые углеводоро́ды
) — ациклические
непредельные
углеводороды
, содержащие одну двойную связь
между атомами углерода
, образующие гомологический ряд с общей формулой C n
H 2n
.
Атомы углерода при двойной связи находятся в состоянии sp 2
-гибридизации
и имеют валентный угол
120°.
Простейшим алкеном является этилен
(C 2
H 4
).
По номенклатуре IUPAC
, названия алкенов образуются от названий соответствующих алканов
заменой суффикса « -ан
» на « -ен
»; положение двойной связи указывается арабской цифрой после соответствующего атома углерода. Например: CH 2
=CH-CH 2
-CH 3 (Бутен-1)
Углеводородные радикалы, образованные от алкенов, имеют суффикс «-ени́л»
.
Тривиальные названия: CH 2
=CH—
«вини́л»
, CH 2
=CH—CH 2
—
«алли́л»
.
Гомологический ряд и изомерия
Алкены, число атомов углерода в которых больше двух, (то есть кроме этилена) имеют свои изомеры
. Для алкенов характерны изомерия углеродного скелета, положения двойной связи, межклассовая и геометрическая. Например, единственным изомером пропилена
является циклопропан
(C 3
H 6
) по межклассовой изомерии. Начиная с бутилена
, существуют изомеры по положению двойной связи (бутен-1 и бутен-2), по углеродному скелету (изобутилен или метилпропилен) и геометрические изомеры
(цис-бутен-2 и транс-бутен-2). С ростом числа атомов углерода в молекуле количество изомеров возрастает в геометрической прогрессии.

Гомологический ряд алкенов:
Алкены могут существовать в виде пространственных
или геометрических
изомеров.
- цис-
изомеры: заместители расположены по одну сторону от двойной связи; - транс-
изомеры: заместители расположены по разные стороны от двойной связи.
IUPAC
рекомендует называть геометрические изомеры по следующей номенклатуре:
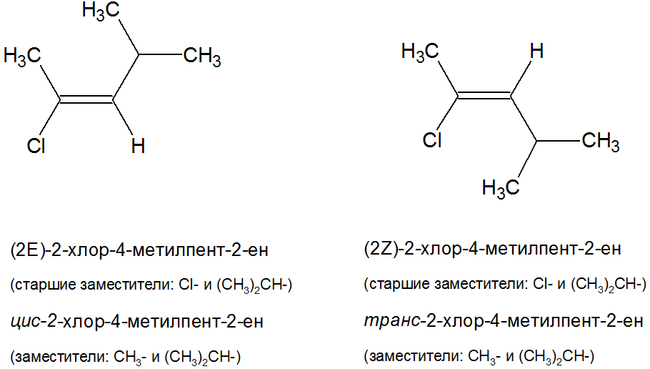
- Z-
изомеры: старшие заместители у углеродных атомов двойной связи находятся по одну сторону относительно двойной связи; - E-
изомеры: старшие заместители у углеродных атомов двойной связи находятся по разные стороны относительно двойной связи.
Электронное строение двойной связи
В соответствии с теорией гибридизации
двойная связь образуется за счёт перекрывания вдоль линии связи С-С
sp 2
-гибридных орбиталей атомов углерода ( σ
-связь) и бокового перекрывания углеродных p
-орбиталей ( π
-связь).

В состоянии sp 2
-гибридизации
электронное состояние атома углерода можно представить следующим образом:
Все атомы этилена лежат в одной плоскости, а величина валентного угла связи C-H
практически равна 120 °. Центры углеродных атомов в этилене находятся на расстоянии 0,134 нм, то есть длина двойной связи несколько короче, чем С-С
.

-орбиталей этилена
Нахождение в природе и физиологическая роль алкенов
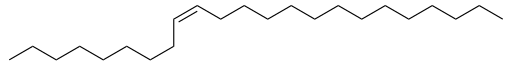
Один из немногих природных алкенов — мускалур
( цис
— трикозен-9) является половым аттрактантом
самки домашней мухи
( Musca domestica
).
Отдельные представители алкенов :
- Этилен
— вызывает наркоз, обладает раздражающим и мутагенным действием
. - Пропилен
— вызывает наркоз (сильнее, чем этилен), оказывает общетоксическое
и мутагенное
действие, а его межклассовый изомер- циклопропан также используется в качестве наркоза. - Бутен-2
— вызывает наркоз, обладает раздражающим действием [9]
.
- Температуры плавления и кипения алкенов (упрощённо) увеличиваются с молекулярной массой и длиной главной углеродной цепи.
- При нормальных условиях
алкены с C 2
H 4
до C 4
H 8
— газы; с пентена C 5
H 10
до гептадецена C 17
H 34
включительно — жидкости, а начиная с октадецена C 18
H 36
— твёрдые вещества. Алкены не растворяются в воде
, но хорошо растворяются в органических растворителях
.
* Значения измерены при температуре кипения.
Алкены химически активны. Их химические свойства во многом определяются наличием двойной связи.
Для алкенов наиболее характерны реакции электрофильного присоединения
и реакции радикального присоединения
. Реакции нуклеофильного присоединения
обычно требуют наличие сильного нуклеофила
и для алкенов не типичны.
Особенностью алкенов являются также реакции циклоприсоединения и метатезиса
.
Алкены легко вступают в реакции окисления
, гидрируются
с сильными восстановителями или водородом
под действием катализаторов
, а также способны к радикальному замещению
.
Реакции электрофильного присоединения
В данных реакциях
атакующей частицей является электрофил.
Галогенирование алкенов, проходящее в отсутствие инициаторов радикальных реакций — типичная реакция электрофильного присоединения
. Она проводится в среде неполярных инертных растворителей (например: CCl 4
):
Механизм реакций подобного типа в общем виде:

Электрофильное присоединение
галогенводородов к алкенам происходит по правилу Марковникова
:

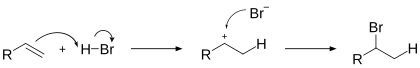

Это объясняется тем, что реакция в данном случае будет протекать по радикальному механизму
и присоединение радикала Br .
идёт по стерически наиболее доступному концевому атому углерода двойной связи:

Присоединение происходит многоступенчато с образованием промежуточного циклического активированного комплекса, причём присоединение бора происходит против правила Марковникова
— к наиболее гидрогенизированному атому углерода:
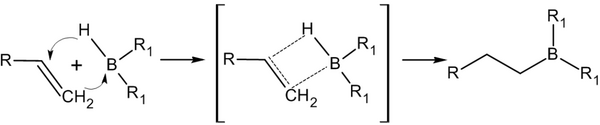
В синтезе обычно используется не сам диборан
, а его донорно-акцепторный комплекс с простым эфиром:

Алкилбораны легко расщепляются. Так под действием пероксида водорода в щелочной среде образуются спирты
:
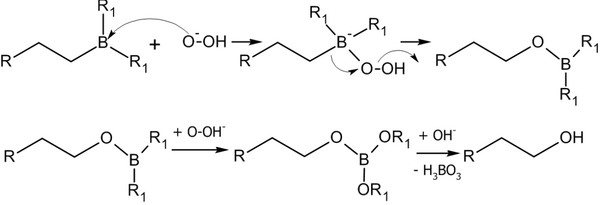
Реакция гидроборирования является реакцией син-присоединения — её результатом становятся цис
-аддукты.
Реакция протекает по правилу Марковникова.
Прочие реакции электрофильного присоединения
- Присоединение спирта
с образованием простого эфира
:
- Присоединение хлорангидридов
с дальнейшим получением ненасыщенных кетонов
( реакция Кондакова
, катализатор ZnCl 2
[15]
):
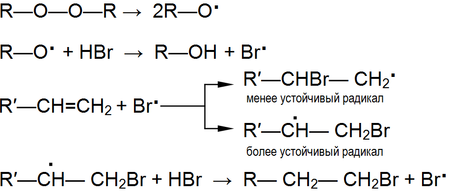
Реакции радикального присоединения
по правилу Марковникова.
Реакции присоединения карбенов


Подробнее о методах получения карбенов см. статью Карбены
.
Гидрирование (реакция Сабатье — Сандеран)
Реакции радикального замещения
При высоких температурах (более 400 °C) реакции радикального присоединения, носящие обратимый характер, подавляются.
В этом случае становится возможным провести замещение атома водорода, находящегося в аллильном положении при сохранении двойной связи:
Реакция носит радикальный характер
и протекает аналогично хлорированию алканов.

Окисление алкенов может происходить в зависимости от условий и видов окислительных реагентов как с разрывом двойной связи, так и с сохранением углеродного скелета.
Окисление неорганическими окислителями
На первом этапе происходит присоединение оксида осмия к алкену, затем под действием восстановителя ( Zn
или NaHSO 3
) образовавшийся комплекс переходит к диолу
( Реакция Криге
).
- При действии на алкены сильных окислителей ( KMnO 4
или K 2
Cr 2
O 7
в среде Н 2
SO 4
) при нагревании происходит разрыв двойной связи:
Окисление в присутствии солей палладия
Реакция идёт в кислой среде и является промышленным способом получения ацетальдегида.
Аналогично образуется ацетон
из пропена
.

Реакция эпоксидирования используется для промышленного получения этиленоксида
. Окислителем выступает кислород воздуха; процесс идёт на серебряном катализаторе при 200—250 °C под давлением.
- в мягких условиях
: алкен окисляется до альдегидов
(в случае монозамещённых вицинальных углеродов), кетонов
(в случае дизамещенных вицинальных углеродов) или смеси альдегида
и кетона
(в случае три-замещенного у двойной связи алкена).
На первой стадии происходит присоединение озона с образованием озонида
. Далее под действием восстановителя (например: Zn
+ CH 3
COOH
) озонид разлагается:
Если взять более сильный восстановитель, скажем — алюмогидрид лития
, продуктом реакции будут спирты
.
- в жёстких условиях
— алкен окисляется до кислоты
:
Полимеризация
алкенов может протекать как по свободнорадикальному
, так и катионно-анионному
механизму.
По первому методу получают полиэтилен
высокого давления:
Катализатором реакции выступают пероксиды.
Второй метод предполагает использование в качестве катализаторов кислот (катионная полимеризация), металлорганических соединений ( катализаторы Циглера-Натта
, анионная полимеризация). Преимуществом метода является возможность получения стереоселективных полимеров.
Реакции свободнорадикального присоединения
Впервые данный тип реакций был обнаружен в середине прошлого века при изучении полимеризации этилена
, а в затем был использован в 1966 году
для промышленного синтеза бутена-2.
В 1967 году
Н. Кальдерон, Х. Ю Чен и К. В. Скотт описали метатезис алкенов
(в российской литературе часто употребляется термин реакция дисмутации алкенов
, иначе говоря — реакцию обмена атомами при сохранении общей структуры алкена и его двойной связи) в условиях катализа хлоридом вольфрама (VI):
Технологические аспекты метатезиса алкенов рассмотрены в статье: Метатезис олефинов: современный путь к полипропилену
.





















![{\mathsf {R\!\!-\!\!CH\!\!=\!\!CH\!\!-\!\!R+[O]}}\rightarrow {\mathsf {2R\!\!-\!\!COOH}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5848e6203a9341c8ca9a8d6a7251d29c949dfdf5)
![{\mathsf {R\!\!-\!\!C(R)\!\!=\!\!CH\!\!-\!\!R+[O]}}\rightarrow {\mathsf {R\!\!-\!\!C(O)\!\!-\!\!CH(R)R}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ea802883018bd47662e62ca08a22b0db107be036)






![{\mathsf {n\ CH_{2}\!\!=\!\!CH_{2}}}\rightarrow {\mathsf {-[-\!CH_{2}\!\!-\!\!CH_{2}\!-]_{n}-}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1e97cdfc9a0a959098c6ee2d45a5bc394ba41aa9)

